- Дифторид ксенона
-
Дифторид ксенона 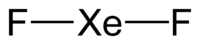
Общие Систематическое наименование Фторид ксенона (II) Химическая формула XeF2 Отн. молек. масса 169 а. е. м. Молярная масса 169.2968 г/моль Физические свойства Плотность вещества 4,32 г/см³ Термические свойства Температура плавления 129,03 °C Температура кипения 155 °C Температура разложения 600 °C Критическая точка 631°С, 9,3 МПа Классификация номер CAS 13709-36-9 XeF2 — твёрдое плотное кристаллическое соединение белого цвета, образованное атомами фтора и ксенона. Одно из самых устойчивых соединений ксенона. Содержание
Физико-химические свойства
Обладает характерным тошнотворным запахом.
В инфракрасных спектрах наблюдается чёткий дублет полос поглощения с волновыми числами 550 и 556 см−1.
Термодинамические величины
Свойство Значение Стандартная энтальпия образования (298К, в твёрдой фазе) −176 кДж/моль Стандартная энтальпия образования (298К, в газовой фазе) −107,5 кДж/моль Энтальпия плавления 16,8 кДж/моль Энтальпия возгонки 50,6 кДж/моль Энтропия образования (298К, в газовой фазе) 259,403 Дж/(моль·К) Теплоёмкость (298К, в газовой фазе) 54,108 Дж/(моль·К) Растворимость
Растворитель Значение Жидкий аммиак Не растворим Ацетонитрил Растворим Вода (при 0 °C) 2,5 г/100 мл Диоксид серы Растворим Пентафторид иода 153,8 г/100 мл Трифторид брома Растворим Фтороводород Растворим Строение
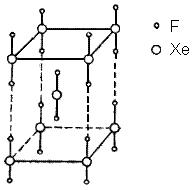
Кристаллическая ячейка XeF2Молекула дифторида ксенона линейная. Длины связей Xe—F равны 0,198 нм.
Получение
Впервые синтез XeF2 провёл Червик Виикс в 1962 году.
Синтез проводят из простых веществ при нагревании, ультрафиолетовом облучении или действии электрического разряда:
- Xe + F2 → XeF2↑.
Продукт конденсируют при −30 °C. Очистку проводят методом фракционной дистилляции.
Механизм данной реакции достаточно интересный, и, по видимому, в нём как-то участвуют молекулы водорода, которыми обычно загрязнён газообразный фтор. Это обнаружили Шмарк и Лютар, которые для синтеза использовали неочищенный от водорода фтор, и при этом скорость реакции выросла в 4 раза по сравнению с использованием чистого фтора.
Также существует метод получения дифторида ксенона из фторида кислорода (II) и ксенона. Для этого смесь газов помещают в никелевый сосуд и нагревают до 300 °C под давлением:
- 2Xe + 2OF2 → 2XeF2 + O2.
В России налажено производство дифторида ксенона в Сибирском химическом комбинате.
Химические свойства
При возгонке дифторид ксенона диспропорционирует на свободный ксенон и тетрафторид ксенона:
- 2XeF2 → Xe + XeF4.
В холодной подкисленной воде разлагается достаточно медленно, зато в щелочной среде разложение идёт быстро:
- 2XeF2 + 4NaOH → 2Xe↑ + O2↑ + 4NaF + 2H2O.
Менее активный окислитель, чем молекулярный фтор.
Образование координационных соединений
XeF2 может выступать в качестве лиганда в комплексных соединениях. Например, в фтороводородном растворе возможна следующая реакция:
- Mg(AsF6)2 + 4 XeF2 → [Mg(XeF2)4](AsF6)2.
Кристаллографический анализ показывает, что атом магния координирован 6 атомами фтора, 4 из которых являются мостиками между атомами магния и ксенона.
Известно множество реакций такого типа [Mx(XeF2)n](AF6)x, в которых в качестве атома M могут выступать Ca, Sr, Ba, Pb, Ag, La или Nd, а атомом A могут быть As, Sb или P.
Такие реакции требуют большого избытка дифторида ксенона.
В твердофазной системе в присутствии фторида цезия некоторые металлы (Ce, Pr, Nd, Tb, Dy, Tu) могут образовывать комплексные соединения типа Cs3[CeF7].
С пентафторидом мышьяка образуется гексафторарсенат трифтордиксенона, в котором в качестве катиона выступает частичка Xe2F3+. Также известны соединения где катионов выступает частица Xe2+.
- AsF5 + 2XeF2 → Xe2F3[AsF6].
Реакции фторирования с простыми веществами
XeF2 фторирует Mn, W, Nb, Sb, Sn, Ti, S, P, Te, Ge, Si до высших фторидов в интервале температур от −10 до +30 °C. Нагревание реакционной смеси до 50 °C приводит к взаимодействию дифторида ксенона с оксидами и солями многих металлов.
В твердофазной системе при нагревании окисляет Ce, Pr и Tb до тетрафторидов.
Реакции окисления
Водный раствор дифторида окисляет броматы до перброматов:
- KBrO3 + XeF2 + H2O → KBrO4 + Xe↑ + 2HF.
Окислительное фторирование
Пример окислительного фторирования для теллур-органического соединения (тут атом теллура меняет степень окисления от +4 до +6):
- Ph3TeF + XeF2 → Ph3TeF3 + Xe↑
Восстановительное фторирование
Пример восстановительного фторирования (тут атом хрома меняет степень окисления от +6 до +4):
- 2CrO2F2 + XeF2 → 2CrOF3 + Xe +O2
Фторирование ароматических соединений
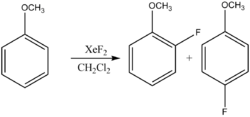
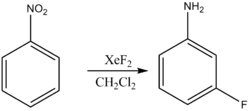
Фторирование ароматических соединений идёт по механизму электрофильного замещения:
При этом возможно и восстановительное фторирование:
Фторирование непредельных соединений
Достаточно селективно можно проводить фторирование диеновых производных в 1,2-положения:
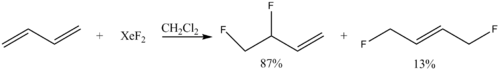 .
.Фторирующее декарбоксилирование
Дифторид ксенона декарбоксилирует карбоновые кислоты, при этом образуются соответствующие фторалканы:
- RCO2H + XeF2 → RF + CO2↑ + Xe↑ + HF↑
Применение
- Один из самых мощных фторирующих агентов.
- Применяют для получения высокотемпературных сверхпроводников на основе сложных слоистых оксофторидов меди [1]
- Является достаточно перспективным для дезинфекции труднодоступных мест[2]
- Дифторид ксенона используется для травление кремния в микроэлектромеханических системах:
- 2XeF2 + Si → 2Xe + SiF4
Примечания
- ↑ Успехи химии, 2002, Том 71, Номер 5, Страницы 442—460.
- ↑ Экстремальная дезинфекция — выбор дезинфектанта
См. также
Литература
- Джолли У. И. Синтезы неорганических соединений. М:Мир., 440 с — 1967 г.
- Некрасов Б. В. Основы общей химии. В 2-ух томах., М:Химия, 1973 г.
- Tius, M. A., Tetrahedron, Volume 51, Issue 24, 12 June 1995, Pages 6605-6634.
- Weeks, J., Matheson, M. Xenon Difluoride. Inorganic Syntheses. № 8, 1966
- Williamson, S. Xenon Difluoride. Inorganic Syntheses № 11, 1968
- Šmalc,A., Lutar, K. Xenon Difluoride (Modification). Inorganic Syntheses № 29, 1992
- D.F. Halpem. «Xenon(II) Fluoride» in Encyclopedia of Reagents for Organic Synthesis. 2004, J.Wiley & Sons, New York.
Wikimedia Foundation. 2010.
Полезное
Смотреть что такое "Дифторид ксенона" в других словарях:
Дифторид криптона — Общие Систематическое наименование Фторид криптона (II) Химическая … Википедия
Дифторид-хлорид азота — Общие Систематическое наименование Дифторид хлорид азота Традиционные названия Хлородифторамин Химическая формула NClF2 Физические свойства Сос … Википедия
КСЕНОНА ФТОРИДЫ — ХеР n (п=2,4,6), бесцв. кристаллы с резким спсцифич. запахом (см. табл.). К. ф. сильные окислители. окислит. способность уменьшается в ряду: XcF6>XeF4>XeF2, донорная способность (К. ф. доноры F в р циях комплексообразования) в ряду:… … Химическая энциклопедия
Фторид ксенона(II) — Фторид ксенона(II) … Википедия
Фторид ксенона(IV) — Фторид ксенона(IV) … Википедия
Фторид ксенона(VI) — Общие … Википедия
Триоксид ксенона — Триоксид ксенона … Википедия
Тетраоксид ксенона — Тетраоксид ксенона … Википедия
Оксид-тетрафторид ксенона — Оксид тетрафторид ксенона … Википедия
Гексафторид ксенона — Общие Систематическое наименование Фторид ксенона (VI) Химическая формула XeF6 Отн. молек. масса 245 а. е. м … Википедия