- Трифторид брома
-
Трифторид брома 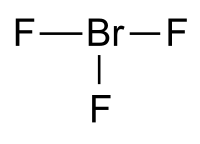
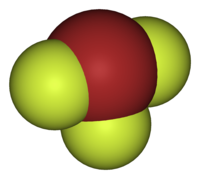
Общие Систематическое наименование Фторид брома (III) Химическая формула BrF3 Отн. молек. масса 137 а. е. м. Молярная масса 136,90 г/моль Физические свойства Плотность вещества (тв.) 3,2 г/см3 ,(жидк) 2,8 г/см³ Термические свойства Температура плавления 8,8 °C Температура кипения 125,8 °C Классификация номер CAS 7787-71-5
Трифтори́д бро́ма (фторид брома(III), трёхфтористый бром) — соединение брома с фтором, представляющее собой при комнатной температуре подвижную бесцветную жидкость, иногда окрашенную желтовато-серым или соломенным цветом (за счёт разложения вещества с образованием бурого брома), дымящую на воздухе. Обладает сильным раздражающим запахом.Содержание
Строение
 Строение молекулы BF3
Строение молекулы BF3Гибридизация атома брома в молекуле sp3d, а строение молекулы полностью аналогичное строению молекулы трифторида хлора, то есть Т-образное, с одной длинной связью и двумя более короткими.
Для трифторида брома также изучена кристаллическая решётка. Кристаллическая ячейча — орторомбическая. Параметры ячейки: [1]
Параметр Значение a 534 пм b 735 пм c 661 пм Предположительно, в узлах кристаллической решётки находятся ионы [BrF2]+ и [BrF4]-.
Физико-химические свойства
Дипольный момент молекулы составляет 1.19 Дебая.
Термодинамические величины
Свойство Значение Стандартная энтальпия образования (в жидкой фазе) -300,8 кДж/моль Стандартная энтальпия образования (в газовой фазе) -255,6 кДж/моль Энтропия образования (в жидкой фазе) 178,2 Дж/(моль·К) Энтропия образования (в газовой фазе) 292,5 Дж/(моль·К) Теплоёмкость (в жидкой фазе) 124,6 Дж/(моль·К) Теплоёмкость (в газовой фазе) 66,6 Дж/(моль·К) Энтальпия плавления 12,03 кДж/моль Энтальпия кипения 42,68 кДж/моль[2] Растворимость
Растворитель Значение Жидкий бром Не смешивается Вода Реагирует Серная кислота Растворим Фтороводород Неограничено смешиваются
(при температуре выше 292К).Хорошо растворяет фториды некоторых металлов, например NaF, KF, AgF, SnF2, BaF2, SbF2.
Химические свойства
- Воспламеняет многие органические соединения (в частности, бумагу и древесину).
- В жидком состоянии подвергается автопротолизу по следующей схеме:
- BrF3 ⇌ BrF2+ + BrF4−
- Многие фториды металлов при расторении образуют двойные соединения, которые в большинстве своём устойчивы к нагреванию, и теряют BrF3 лишь при температурах выше 200°С. Например при растворении в трифториде брома фторида калия выделяется следующее соединение:
- KF + BrF3 → KBrF4.
Получение
- Трифторид брома можно получить из прочтых веществ при комнатной температуре (20°C)
- Br2 + 3F2 → 2BrF3
- Также, трифторид брома является продуктом диспропорционирования монофторида брома. При этом таккже образуется свободный бром:
- 3BrF → BrF3 + Br2[3]
Применение
BrF3 нашел достаточно большой спектр различных вариантов применения. Вот некоторые из них:
- Трифторид брома — очень хороший фторирующий агент. Он используется во все возможных органических синтезах. Например в реакции с сукциннитрилом (NCCH2CH2CN) образуется 1,1,1,4,4,4-гексафторбутана, который не просто получить используя другие фторирующие агенты.[4]
- На основе системы литий/трифторид брома разрабатывается достаточно перспективный источник тока.[5]
- Также трифторид можно использовать для травления кристаллов кремния в газовой фазе, что может успешно применяться для производства различных полупроводниковых приборов.[6]
- Успешно применяется в ядерной промышленности для получения и разделения фторидов урана, а также является перспективным для переработки ядерного топлива:
- 2U + 5BrF3 → 2UF6 + 3BrF + Br2.
- Для некоторых синтезов, трифторид брома выступает одновременно в роли растворителя, фторирующего агента и окислителя. Например реакция с трихлоридами металлов, в которой получаются соли фторпроизводных кислот (тут М — трёхвалентный металл):
- МCl3 + 3KHF2 → K3MF6↓ + 3НCl
Опасности
Трифторид брома является достаточно опасным веществом. Среди опасностей связанных с применением этого вещества можно выделить слудующие:[7]:
- Вероятность взрыва от удара, трения или искры.
- Токсичен для вдыхания и попадание внутрь организма.
- Оставляет серьёзные плохозаживающие ожоги при попадании на кожу.
Примечания
- ↑ X-Ray investigation of the structure of liquid Bremine Trifluoride. V.N. Mitkin, G.S. Yurev, S.V. Zemskov, V.I. Kazakova. Journal of Structural Chemistry Volume 28, Number 1, 1987.
- ↑ Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977
- ↑ Simons JH (1950). "Bromine (III) Fluoride - Bromine Trifluoride". Inorganic Synthesis 3: 184–186
- ↑ Max T. Baker, Jan A. Ruzicka, John H. Tinker. Journal of Fluorine Chemistry Volume 94, Issue 2, Pages 123-126
- ↑ Патент США №5188913
- ↑ Патент США №6436229
- ↑ Данные о опасности соединения
См. также
Литература
- Джолли У.И. Синтезы неорганических соединений. М:Мир., 440 с. - 1967 г.
- Некрасов Б.В. Основы общей химии. В 2-ух томах., М:Химия, 1973 г.
Wikimedia Foundation. 2010.
