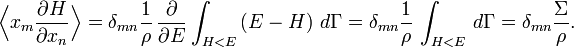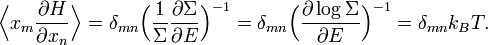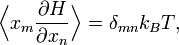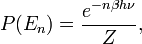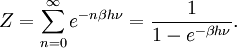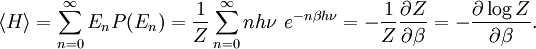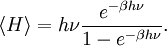- Эквипарциальная теорема
-
 Тепловое движение α-пептида. Сложное дрожащее движение атомов, составляющих пептид, случайно, и энергия отдельного атома флуктуирует в широких пределах, но с помощью закона равнораспределения вычисляют как среднюю кинетическую энергию каждого атома так и среднюю потенциальную энергию многих колебаний. Серые, красные и синие шары обозначают атомы углерода, кислорода и азота, соответственно; маленькие белые шарики представляют атомы водорода.
Тепловое движение α-пептида. Сложное дрожащее движение атомов, составляющих пептид, случайно, и энергия отдельного атома флуктуирует в широких пределах, но с помощью закона равнораспределения вычисляют как среднюю кинетическую энергию каждого атома так и среднюю потенциальную энергию многих колебаний. Серые, красные и синие шары обозначают атомы углерода, кислорода и азота, соответственно; маленькие белые шарики представляют атомы водорода.В классической статистической механике теорема о равнораспределении кинетической энергии по степеням свободы позволяет связать температуру системы с её средней энергией. Эта теорема также известна под названиями закон равнораспределения и теорема о равнораспределении. В первоначальном виде теорема равнораспределения утверждала, что при тепловом равновесии энергия разделена одинаково между её различными формами, например, средняя кинетическая энергия поступательного движения молекулы должна равняться средней кинетической энергии её вращательного движения.
С помощью теоремы о равнораспределении можно делать количественные предсказания. Как и вириальная теорема, она даёт полные средние кинетические и потенциальные энергии для системы при данной температуре, из которых можно вычислить теплоёмкость системы. Однако теорема о равнораспределении также позволяет определить средние значения отдельных компонентов энергии, такие как кинетическая энергия одной частицы или потенциальная энергия отдельной пружины. В теореме утверждается, что каждая молекула в идеальном газе обладает средней кинетической энергией равной (3/2)kBT при термодинамическом равновесии, где kB — постоянная Больцмана, T — температура. В общем случае её можно применять к любой классической системе находящейся в состоянии теплового равновесия независимо от того насколько она сложна. Теорема о равнораспределении может использоваться для вывода уравнения состояния идеального газа и закона Дюлонга — Пти, для определения удельной теплоёмкости твёрдых тел. Её также используют в предсказании свойств звёзд, даже таких как белые карлики и нейтронные звезды, поскольку закон равнораспределения остаётся верен даже даже когда следует учитывать релятивистские эффекты.
Хотя теорема о равнораспределении делает очень точные предсказания при определённых условиях, она теряет применимость, когда квантовые эффекты начинают играть существенную роль. Равнораспределение действителено только тогда, когда тепловая энергия kBT намного больше чем интервал между соседними квантовыми уровнями энергии, потому что в противном случае средние значения энергии и теплоёмкости приходящиеся на определённые степени свободы меньше чем величины полученные с использованием теоремы о равнораспределении. Говорят, что степень свободы выморожена, если тепловая энергия намного меньше чем этот интервал. Например, теплоёмкость твёрдого тела уменьшается при низких температурах, поскольку различные типы движения становятся вымороженными, вместо того, чтобы остаться постоянными как получается по теореме о равнораспределении. Такое уменьшение теплоёмкости было первым знаком физикам 19-ого столетия, что классическая физика теряет применимость при низкой температуре и новые законы должны быть сформулированы для объяснения этих различий. Наряду с другим противоречием, несостоятельностью закона равнораспределения для описания электромагнитного излучения — также известного как ультрафиолетовая катастрофа — привели Альберта Эйнштейна к идеи, что свет сам состоит из квантов (фотонов). Эта революционная гипотеза предвосхитила появление квантовой механики и квантовой теории поля.
Содержание
Основная идея и простые примеры
-
См. также: Кинетическая энергия и Теплоёмкость
 Распределение плотности вероятности скоростей молекул для четырёх благородных газов при температуре 298.15 К (25 °C). Показаны гелий (4He), неон (20Ne), аргон (40Ar) и ксенон (132Xe) (индекс обозначает их массовые числа). Функции распределения плотности вероятности имеют размерность обратной скорости, поскольку вероятность величина безразмерная, и её можно выразить в единицах секунда на метр.
Распределение плотности вероятности скоростей молекул для четырёх благородных газов при температуре 298.15 К (25 °C). Показаны гелий (4He), неон (20Ne), аргон (40Ar) и ксенон (132Xe) (индекс обозначает их массовые числа). Функции распределения плотности вероятности имеют размерность обратной скорости, поскольку вероятность величина безразмерная, и её можно выразить в единицах секунда на метр.Первоначально термин «равнораспределение» означал, что полная кинетическая энергия системы разделена одинаково среди всех её независимых частей в среднем, как только система достигла теплового равновесия. Теорема о равнораспределении также даёт количественные предсказания для этих энергий. Например, она предсказывает, что каждый атом благородного газа, находящегося в тепловом равновесии при температуре T, обладает средней кинетической энергией поступательного движения равной (3/2)kBT. Как следствие, более тяжёлые атомы ксенона обладают более низкой средней скоростью чем лёгкие атомы гелия при той же самой температуре. Рисунок показывает распределение Максвелла — Больцмана для скоростей атомов четырёх газов.
В этом примере важно отметить, что кинетическая энергия является квадратичной функцией скорости. Закон равнораспределения показывает, что при тепловом равновесии, любая степень свободы (компоненты векторов положения или скорость частицы), которая появляется только как квадратичная функция в энергии, обладает средней энергией равной ½kBT и поэтому вносит вклад ½kB в теплоёмкость системы. У этого утверждения существует много практических приложений.
Энергия поступательного движения частиц идеальных газов
-
См. также: Идеальный газ
Кинетическая энергия частицы газа с массой m и обладающая скоростью v задаётся в виде
где vx, vy и vz — декартовы компоненты вектора скорости v. Здесь символ H обозначает гамильтониан системы и используется как символ энергии в гамильтоновом формализме. Он играет центральную роль в большинстве обобщений закона равнораспределения.
Поскольку кинетическая энергия является квадратичной функцией компонент скорости, из закона равнораспределения следует, что каждая из этих компонент вносит одинаковый вклад ½kBT в среднюю кинетическую энергию газа находящегося в тепловом равновесии. Отсюда следуеи, что средняя кинетическая энергия частицы равна (3/2)kBT, как в примере для благородных газов сверху.
В общем случае, полная энергия идеального газа состоит из (поступательной) кинетической энергии отдельных частиц, в соответствии с предположением, что частицы не имеют никаких внутренних степеней свободы и перемещаются независимо от друг друга. Равнораспрееление означает, что средняя полная энергия идеального газа из N частиц равна (3/2)N kBT.
Отсюда следует, что теплоёмкость газа составляет (3/2)N kB и, в частности, теплоёмкость одного моля газа таких частиц равна (3/2)NAkB=(3/2)R, где NA — число Авогадро и R — газовая постоянная. Поскольку R ≈ 2 кал/(моль·К), закон равнораспределения предсказывает что молярная теплоёмкость идеального газа приблизительно равна 3 кал/(моль·К). Это предсказание проверено экспериментально.[1]
Средняя кинетическая энергия позволяет оценить корень квадратный из среднего квадрата скорости vrms частиц в газе:
где M = NAm — молярная масса газа. Этот результат полезен для многих практических приложений, таких как закон Грэхема для эффузии, который используется в методе обогащения урана[2]
Энергия вращательного движения
-
См. также: Угловая скорость
Похожий пример можно найти при рассмотрении вращающейся молекулы с главными осями инерции I1, I2 и I3. Вращательная энергия такой молекулы задана выражением
где ω1, ω2, и ω3 — главные компоненты угловой скорости. Точно по тем же самым рассуждениям как и в случае поступательного движения равнораспределение подразумевает, что при тепловом равновесии средняя вращательная энергия каждой частицы: (3/2)kBT. Аналогично, теорема о равнораспределении позволяет вычислить среднюю (более точно, корень квадратный из среднего квадрата) угловую скорость молекул.[3]
Потенциальная энергия и гармонические осцилляторы
Равнораспределение применимо не только к кинетической энергии, но и к потенциальной энергии. Важные примеры включают гармонические осцилляторы такие как пружина, которая обладает квадратичной по координатам потенциальной энергией
где постоянная a описывает жёсткость пружины и q — отклонение от равновесного положения. Если такая одномерная система имеет массу m, тогда её кинетическая энергия Hkin: ½mv² = p²/2m, где v и p = mv обозначают скорость и импульс осциллятора. Суммируя эти вклады получим полную энергию системы[4]
Равнораспределение подразумевает, что при тепловом равновесии осциллятор обладает средней энергия, которая равна
где угольные скобки
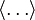 обозначают усреднение заключённой в них величины.[5]
обозначают усреднение заключённой в них величины.[5]Этот результат остаётся верен для любого типа гармонического осциллятора, таких как маятник, колеблющаяся молекула или пассивный электрический генератор. Системы таких осцилляторов возникают во многих случаях. По закону равнораспределения, каждый такой осциллятор обладает средней полной энергией kBT и следовательно даёт вклад kB в теплоёмкость системы. Этот вывод можно использовать для вывода формулы для теплового шума[6] и закона Дюлонга — Пти для удельной теплоёмкости твёрдых тел. Последнее сыграло важную роль в истории теоремы о равнораспределении.
 Атомы в кристалле могут колебаться около их равновесных положений в решётке. Такие колебания считаются (наряду c электронами) в значительной степени ответственными за теплоёмкость кристаллических диэлектриков и металлов.
Атомы в кристалле могут колебаться около их равновесных положений в решётке. Такие колебания считаются (наряду c электронами) в значительной степени ответственными за теплоёмкость кристаллических диэлектриков и металлов.Теплоёмкость твёрдых тел
Закон равнораспределения применяется для определения удельной теплоёмкости кристаллических тел. Поскольку каждый атом из такого тела может колебаться в трёх независимых направлениях, то кристалл можно рассматривать как систему 3N независимых гармонических осцилляторов, где N обозначает число атомов в решётке. Каждый гармонический осциллятор обладает средней энергией kBT, поэтому средняя полная энергия тела равна 3NkBT, а его удельная теплоёмкость 3NkB.
Если взять за N — число Авогадро (NA), то, используя соотношение R = NAkB между газовой постоянной (R) и постоянной Больцмана (kB), получим выражение для закона Дюлонга — Пти, который описывает молярную теплоёмкость твёрдых тел. Он гласит, что удельная теплоёмкость одного моля атомов кристаллической решётки составляет 3R ≈ 6 кал/(моль·К).
Следует отметить, что этот закон неверен при низких температурах, где важно принять во внимание квантовые эффекты. Он также вступает в противоречие с экспериментально подтверждённым третьим началом термодинамики, согласно которому удельная теплоёмкость любого вещества стремится к нулю при стремлении температуры к абсолютному нулю.[6] Более точная теория, которая принимает во внимание квантовые эффекты была разработана Альбертом Эйнштейном (1907 год) и Петером Дебаем (1911 год).[7]
Многие физические системы можно смоделировать в виде системы связанных гармонических осцилляторов. Движения таких осцилляторов можно разложить на нормальные моды, которые можно представить как вибрационные моды струны фортепьяно или резонансы трубы органа. С другой стороны, теорема о равнораспределении становится неприменимой для таких систем из-за отсутствия обмена энергии между нормальными модами. В предельном случае моды независимы и, таким образом, их энергии сохраняются независимо. Это означает, что смешивание энергий, формально называемое эргодичностью, важно для выполнения закона равнораспределения.
Седиментация частиц
Потенциальная энергия не всегда является квадратичной функцией координат, но теорема о равнораспределении утверждает, что если степень свободы x входит с множителем xs (для фиксированной постоянной s) в полную энергию, то при тепловом равновесии средняя энергия этой части равна kBT/s.
Это обобщение используется при рассмотрении седиментации частиц под действием гравитации.[8] Например, взвесь иногда заметная в пиве может быть вызвана кусочками белков, которые рассеивают свет.[9] В течение долгого времени, эти кусочки скапливаются на дне под действием силы тяжести, приводя к более сильному рассеянию света около основания бутылки, чем у её вершины. Однако, благодаря диффузии работающей в противоположном направлении, частицы движутся вверх к вершине бутылки. Как только равновесие достигнуто, теорема о равнораспределении может использоваться, чтобы определить среднее положение определённого кусочка плавучей массы mb. Для бесконечно высокой бутылки пива гравитационная потенциальная энергия задана в виде
где z — положение белкового кусочка в бутылке по высоте и g — ускорение вызванное гравитацией. Поскольку s=1, то средняя потенциальная энергия белкового кусочка равна kBT. Если масса белкового кусочка составляет около 10 МДа (грубо это размер вируса), то при равновесии возникнет взвесь со средней высотой около 2 см. Процесс седиментации к равновесному положению описывается уравнением Масона — Вивера.[10]
История
Равнораспределение кинетической энергии по степеням свободы предложил в 1843 году (правильнее говорить о 1845 годе) Джон Джеймс Уотерстон.[11][12][13][14][15] В 1859, Джеймс Клерк Максвелл утверждал, что кинетическая энергия при высокой температуре газа одинаково разделена между энергией поступательного движения и вращательной энергией.[16] В 1876 году, Людвиг Больцман показал, что средняя энергия разделена одинаково между всех независимых компонент движения в системе.[17][18] Больцман применил закон равнораспредедления, чтобы теоретически объяснить закон Дюлонга — Пти для теплоёмкости твёрдых тел.
 Идеализированный график теплоёмкости двухатомного газа в зависимости от температуры. Значение (7/2)R согласуется с предсказанной из закона равнораспределения теплоёмкостью для высоких температур (где R газовая постоянная), но уменьшается до (5/2)R и затем до (3/2)R при более низких температурах, поскольку колебательные и вращательные степени свободы вымораживаются. Нарушение закона равнораспределения привело к парадоксу, который был разрешён только в квантовой механике. Для большинства молекул переходная температура Trot много меньше комнатной температуры, в то время как Tvib может быть в десять раз больше. (Типичный пример: монооксид углерода, CO, для которого Trot ≈ 2.8 К, а Tvib ≈ 3103 К.) Для молекул с длинными или слабыми связями между атомами, Tvib может быть близка к комнатной температуре (около 300 КK); например, Tvib ≈ 308 К для газа иода, I2.[19]
Идеализированный график теплоёмкости двухатомного газа в зависимости от температуры. Значение (7/2)R согласуется с предсказанной из закона равнораспределения теплоёмкостью для высоких температур (где R газовая постоянная), но уменьшается до (5/2)R и затем до (3/2)R при более низких температурах, поскольку колебательные и вращательные степени свободы вымораживаются. Нарушение закона равнораспределения привело к парадоксу, который был разрешён только в квантовой механике. Для большинства молекул переходная температура Trot много меньше комнатной температуры, в то время как Tvib может быть в десять раз больше. (Типичный пример: монооксид углерода, CO, для которого Trot ≈ 2.8 К, а Tvib ≈ 3103 К.) Для молекул с длинными или слабыми связями между атомами, Tvib может быть близка к комнатной температуре (около 300 КK); например, Tvib ≈ 308 К для газа иода, I2.[19]История теоремы о равнораспределении переплетена с исследованиями теплоёмкости, которые были проведены в 19-ом столетии. В 1819 году французские физики Пьер Дюлонг и Алексис Пти обнаружили, что удельные молярные теплоёмкости для твёрдых тел практически равны при комнатной температуре, и составляют приблизительно 6 кал/(моль·К).[20] Их закон использовался многие годы для измерения атомных весов.[7] Однако последующие исследования Джеймса Дьюара и Генриха Вебера показали, что закон Дюлонга-Пти выполняется только при больших температурах,[21][22][23] а при низких температурах или для очень твёрдых кристаллов, таких как алмаз, теплоёмкость меньше.[24][25][26]
Экспериментальные значения теплоёмкости газов также поставили вопросы о правильности эквипарциальной теоремы. Теорема предсказывает, что молярная удельная теплоёмкость моноатомных газов должна быть примерно 3 кал/(моль·К), а для двухатомных газов приблизительно 7 кал/(моль·К). Эксперименты подтвердили первое предсказание,[1] но для двухатомных газов эксперимент показал, что удельная молярная теплоёмкость составляет только 5 кал/(моль·К),[27] и падает до 3 кал/(моль·К) при очень низких температурах.[28] Максвелл заметил в 1875, что расхождение между эксперементом и законом равнораспределения даже хуже, если брать эти значения;[29] поскольку атомы имеют внутреннюю структуру, то тепловая энергия должна пойти на движение этих внутренних частей, приводя к предсказаниям для удельных молярных теплоёмкостей одноатомных и двухатомных газов много больших чем 3 кал/(моль·К) и 7 кал/(моль·К), соответственно.
Третье разногласие связано с теплоёмкостью металлов.[30] Согласно классической модели Друде, электроны в металле ведут себя как идеальный газ и соответственно должны давать вклад (3/2)Ne kB, где Ne — число электронов, в теплоёмкость металла по теореме о равнораспределении. Эксперементально, однако, вклад электронов в теплоёмкость невелик: молярные теплоёмкости различных проводников и диэлектриков практически совпадают.[30]
Были предложены несколько объяснений неточности теоремы о равнораспределении при опеределении теплоёмкостей. Больцман защищал доказательство своей теоремы как правильное, но предположил, что газы могут не быть в тепловом равновесии из-за их взаимодействия с эфиром.[31] Лорд Кельвин предположил, что вывод теоремы о равнораспределении должен быть неверен, поскольку её выводы расходятся с экспериментом, но не смог указать ошибку.[32] Лорд Рэлей вместо этого выдвинул более радикальную гипотезу, заключающуюся в том что и теорема о равнораспределении и экспериментальное предположение о тепловом равновесии верны, но чтобы согласовать их, он высказался о потребности нового принципа, который обеспечит побег от разрушительной простоты теоремы о равнораспределении.[33] Альберт Эйнштейн показал путь для разрешения этого противоречия, когда в 1907 году показал, что эти аномалии в теплоёмкости возникают из-за квантовых эффектов, в частности квантования энергии упругих колебаний твёрдого тела.[34][35][36][37][38] Эйнштейн использовал неточность закона равнораспределения как довод в пользу потребности новой квантовой теории вещества.[7] Эксперементы Нернста в 1910 году по измерению теплоёмкости при низких температурах[39] подтвердили теорию Эйнштейна и привели к широкой поддержке квантовой теории среди физиков.[40]
Общая формулировка теоремы о равнораспределении
-
См. также: Обобщённые координаты, Гамильтонова механика, Микроканонический ансамбль и Канонический ансамбль
Наиболее общая формулировка теоремы о равнораспределении[3][5][8] гласит, что при определённых условиях (смотрите ниже), для физической системы с гамильтонианом H и степенями свободы xn, выполняется следующее соотношение для любых индексов m и n:
Здесь δmn — символ Кронекера, который равен единице если m=n и нулю в других случаях. Угловые скобки обозначают усреднение
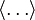 , которое может относиться как к усреднению по времени так и более общему усреднению по ансамблям в фазовом пространстве. Требования эргодичности используемое в теореме подразумевает, что эти два усреднения эквивалентны.
, которое может относиться как к усреднению по времени так и более общему усреднению по ансамблям в фазовом пространстве. Требования эргодичности используемое в теореме подразумевает, что эти два усреднения эквивалентны.Общая формулировка теоремы верна как в случае микроканонического ансамбля,[5] когда полная энергии системы постоянна, так и в случае канонического ансамбля,[3][41] когда система связана с тепловым резервуаром, с которым она может обмениваться энергией. Вывод общей формулы приведён ниже.
Общая формула эквивалентна следующим выражениям:
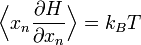 для всех n.
для всех n.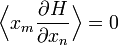 для всех m≠n.
для всех m≠n.
Если степень свободы xn появляется только в виде квадратичного слагаемого anxn² в гамильтониане H, то первая формула утверждает, что
в два раза больше вклада этой степени свободы в среднюю энергию
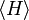 . Тогда рввнораспределение для системы с энергиями зависящими от квадратов координат следует из общей формулы. Аналогичный аргумент для степени s в общем случае применим для вклада вида anxns.
. Тогда рввнораспределение для системы с энергиями зависящими от квадратов координат следует из общей формулы. Аналогичный аргумент для степени s в общем случае применим для вклада вида anxns.Степени свободы xn — координаты в фазовом пространстве системы и поэтому они обычно разделяют на обобщённые координаты qk и обобщённые импульсы pk, где pk — сопряжённый импульс к qk. В этом случае формула 1 означает, что для всех k
Используя уравнения гамильтоновой механики,[4] эти формулы можно также переписать в виде
Формула 2 утверждает, что средние
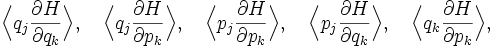 и
и 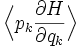
равны нулю для j≠k.
Связь с вириальной теоремой
Общая теорема о равнораспределении является обобщением теоремы о вириале (предложена в 1870[42]) и гласит
где t обозначает время.[4] Два ключевых различия между ними заключаются в том, что вириальная теорема связывает «суммированные», а не «индивидуальные» средние друг с другом, и первая не связывает их с температурой «T». Другое различие — то, что традиционные доказательства вириальной теоремы используют усреднение в течение длительного периода времени, тогда как эквипарциальная теорема также использует усреднение по фазовому пространству.
Применения
Уравнение состояния идеального газа
-
См. также: Идеальный газ и Уравнение состояния идеального газа
Теорема о равнораспределении используется для вывода уравнения состояния идеального газа из классической механики.[3]. Формула для средней кинетической энергии на одну частицу, принимая во внимание только три поступательных степени свободы запишется в виде
Если q = (qx, qy, qz) и p = (px, py, pz) обозначают координаты и импульс частицы в газе, а F — сила действующая на эту частицу, тогда
где первое равенство представляет собой второй закон Ньютона, а вторая строчка использует уравнения Гамильтона и равнораспределение. Суммирование по системе из N частиц приводит к выражению
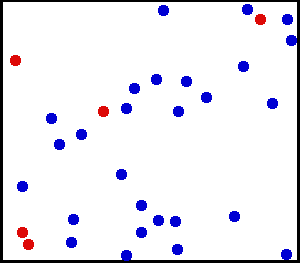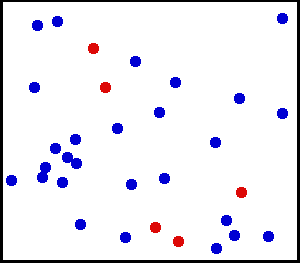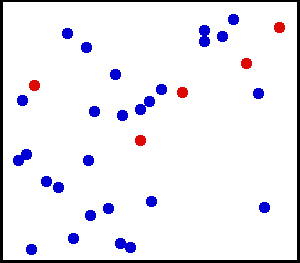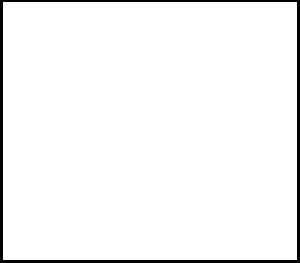 Кинетическая энергия одной молекулы может сильно варьироваться, но закон равнораспределения позволяет вычислить её «среднюю» энергии при любой температуре. Равнораспределение по степеням свободы также приводит к уравнению состояния идеального газа, которое связывает давление, объём и температуру идеального газа. (На этом рисунке пять из молекул изображены красным, чтобы было легче отслеживать их движение среди других частиц.)
Кинетическая энергия одной молекулы может сильно варьироваться, но закон равнораспределения позволяет вычислить её «среднюю» энергии при любой температуре. Равнораспределение по степеням свободы также приводит к уравнению состояния идеального газа, которое связывает давление, объём и температуру идеального газа. (На этом рисунке пять из молекул изображены красным, чтобы было легче отслеживать их движение среди других частиц.)Используя третий закон Ньютона и предположение об идеальности газа, получим полную силу в системе — силу, которая действует со стороны стенок контейнера на систему, и эта сила задаётся давлением P газа. Следовательно
где dS — бесконечно малый элемент площади стенок контейнера. Поскольку дивергенция радиус-вектора q равняется
то из теоремы о дивергенции получаем
где dV — бесконечно малый объём внутри контейнера, V — его полный объём.
Собирая уравнения вместе получаем
которое приводит к уравнению состояния для идеального газа для N частиц:
где n=N/NA — число молей газа и R=NAkB — газовая постоянная.[43]
Двухатомные газы
Двухатомный газ можно представить как соединённые между собой посредством пружины с жёсткостью a, две массы m1 и m2.[19] Классическая энергия этой системы записывается в виде суммы кинетических энергий движения отдельных масс и потенциальной энергии деформации пружины:
где p1 и p2 — импульсы двух атомов, q — отклонение от положения равновесия. Каждая степень свободы является квадратичной функцией, и поэтому должна давать вклад равный ½kBT к полной средней энергии и ½kB к удельной теплоёмкости. Таким образом, удельная теплоёмкость газа из N двухатомных молекул должна равняться 7N · ½kB: импульсы p1 и p2 дают каждый по три степени свободы и отклонение q добавляет седьмую. Отсюда следует, что удельная теплоёмкость одного моля газа двухатомных молекул без каких-либо отличных от упомянутых выше степеней свободы должна составить (7/2)NAkB=(7/2)R и, таким образом, предсказанная молярная удельная теплоёмкость составит 7 кал/(моль·К). В то же время, как показали измерения, молярная удельная теплоёмкость газа двухатомных молекул равняется 5 кал/(моль·К)[27] и уменьшается до 3 кал/(моль·К) при очень низких температурах.[28] Это расхождение между предсказанным значением по закону равнораспределения и экспериментом нельзя объяснить, используя более сложную структуру молекулы, поскольку с добавлением степеней свободы увеличивается и предсказанное значение теплоёмкости.[29] Это разногласие было одним из ключевых, которые требовали более правильных, а именно квантовых представлений о структуре материи.
 Совмещённое рентгеновское и оптическое изображения крабовидной туманности. В центре этой туманности находится быстро вращающаяся нейтронная звезда, которая в полтора раза тяжелее нашего Солнца, но только 25 км в диаметре. Теорема о равнораспределении оказывается полезной для изучения свойств таких звёзд.
Совмещённое рентгеновское и оптическое изображения крабовидной туманности. В центре этой туманности находится быстро вращающаяся нейтронная звезда, которая в полтора раза тяжелее нашего Солнца, но только 25 км в диаметре. Теорема о равнораспределении оказывается полезной для изучения свойств таких звёзд.Ультрарелятивистские идеальные газы
Закон равнораспределения использовался выше, чтобы получить классическое уравнение состояния идеального газа из ньютоновской механики. Однако релятивистские эффекты становятся доминирующими в некоторых системах, таких как белые карлики и нейтронные звезды,[5] и уравнение состояния идеального газа нужно изменить. Теорема о равнораспределении даёт удобный способ получить соответствующие законы для ультрарелятивистского идеального газа.[3] В этом случае, кинетическая энергия отдельной частицы задана формулой
Дифференцируя H по px компоненте импульса, получим
и аналогично для py и pz компонент. Складывая три компоненты вместе прийдём к выражению для средней кинетической энергии
где последнее равенство следует из равнораспределения. Таким образом, средняя полная энергия ультрарелятивистского газа в два раза больше полной энергии газа в нерелятивистском случае: для N частиц, получим 3 N kBT.
Неидеальные газы
-
См. также: Вириальное разложение и Вириальный коэффициент
В идеальном газе частицы взаимодействуют только через соударения. Закон равнораспределения можно использовать для получения выражения для давления и энергии «неидеальных газов», в которых частицы взаимодействуют друг с другом посредством консервативных сил. Потенциал взаимодействия U(r) этих частиц зависит только от расстояния r между частицами.[3] Эта ситуация описывается в модели одной частицы, где остальные частицы в газе образуют сферически-симметричное распределение. Удобно ввести радиальную функцию распределения g(r), такую что плотность вероятности найти частицу на расстоянии r от данной равна 4πr²ρ g(r), где ρ=N/V — средняя плотность газа.[44] Отсюда следует, что средняя потенциальная энергия взаимодействия частицы с её окружением равна
Полная средняя потенциальная энергия газа равна
 , где N — число частиц в газе, и множитель ½ необходим поскольку суммирование по всем частицам включает каждое взаимодействие дважды. После суммирования потенциальной и кинетической энергии и применения равнораспределения получим энергетическое уравнение
, где N — число частиц в газе, и множитель ½ необходим поскольку суммирование по всем частицам включает каждое взаимодействие дважды. После суммирования потенциальной и кинетической энергии и применения равнораспределения получим энергетическое уравнениеПохожие рассуждения,[3] приводят к уравнению для давления
Ангармонические осцилляторы
-
См. также: Ангармонический осциллятор
Для ангармонического осциллятора (в противоположность простому гармоническому осциллятору) потенциальная энергия не является квадратичной функцией смещения q (обобщённая координата, которая показывает отклонение от положения равновесия). Такие осцилляторы позволяют более широко взглянуть на закон равнораспределения.[45][46] в качестве простого примера рассмотрим функции потенциальной энергии вида
где C и s произвольные реальные постоянные. В этом случае закон равнораспределения приводит к выыражению
Таким образом, средняя потенциальная энергия равна kBT/s, а не kBT/2 как для квадратичного потенциала гармонического осциллятора (где s=2).
Более обще, типичная функция энергии одномерной системы представима в виде разложения Тейлора по q:
для неотрицательных целых чисел n. Слагаемое с n=1 отсутствует, поскольку в точке равновесия отсутствует результирующая сила и первая производная энергии обращается в ноль. Слагаемое с n=0 нужно включить, поскольку потенциальная энергия в точке равновесия может быть выбрана произвольным образом (ноль для простоты). В этом случае из равнораспределения следует что[45]
В противоположность с другими примерами приведёнными здесь, закон равнораспределения
для средней потенциальной энергии не может быть записан в терминах известных постоянных.
Броуновское движение
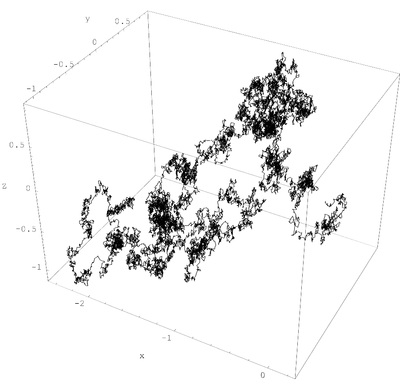 Типичное броуновское движение частицы в трёх измерениях.
Типичное броуновское движение частицы в трёх измерениях.-
См. также: Броуновское движение
Закон равнораспределения используют для вывода среднеквадратичного отклонения броуновской частицы, используя уравнение Ланжевена.[3] Согласно этому уравнению движение частицы с массой m и скоростью v управляется вторым законом Ньютона
где Frnd — случайная сила, которая описывает случайные соударения частицы с окружающими молекулами, и где постоянная времени τ отражает существование силы трения которая направлена в противоположную движению сторону. Сила трения часто записывается в виде пропорциональном скорости частицы Fdrag = — γv, и тогда постоянная времени τ равна m/γ.
Скалярное произведение этого уравнения и вектора местоположения частицы r после усреднения (по времени) приводит к уравнению
для броуновского движения (поскольку случайная сила Frnd некоррелирована с вектором r). Используя математические соотношения
и
основное уравнение для броуновского движения можно записать в виде
где последнее равенство следует из закона равнораспределения для кинетической энергии поступательного движения:
Тогда дифференциальное уравнение для
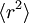 (с подходящими начальными условиями) можно решить точно:
(с подходящими начальными условиями) можно решить точно:Если время мало по сравнению с постоянной времени (t << τ), то частицу можно рассматривать как свободно движущуюся, и используя разложение Тейлора для экспоненциальной функции, поскольку квадрат смещения растёт приблизительно квадратично получим
При временах много больших постоянной времени (t >> τ) экспоненциальное слагаемое и константа пренебрежимо малы и квадрат смещения растёт линейно:
Это выражение описывает диффузию частицы во времени. Аналогичное уравнение для вращательной диффузии жёсткой молекулы выводится аналогичным методом.
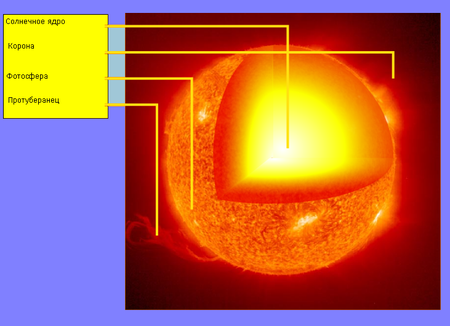 Эквипарциальная теорема даёт правильную оценку для температуры внутри ядра Солнца.
Эквипарциальная теорема даёт правильную оценку для температуры внутри ядра Солнца.Физика звёзд
-
См. также: Астрофизика и Структура звезды
Теорема о равнораспределении и вириальная теорема давно используется в астрофизике.[47] Например, вириальную теорему используют для оценки температур звёзд или предела Чандрасекара для массы белых карликов.[48][49]
Средняя температура звезды оценивается из теоремы о равнораспределении.[50] Поскольку большинство звёзд сферически симметричны, то полная гравитационная потенциальная энергия оценивается интегралом
где M(r) — масса внутри радиуса r, ρ(r) — звёздная плотность на радиусе r, G — гравитационная постоянная, R — полный радиус звезды. Предполагая постоянную плотность звезды интегрирование по радиусу приводит к выражению
где M — полная масса звезды. отсюда следует, что средняя потенциальная энергия одной частицы равна
где N — число частиц в звезде. Большинство звёзд состоит главным образом из ионизированного водорода, тогда N равно приблизительно (M/mp), где mp — масса протона. Применение закона о равнораспределении даёт оценку температуры звезды
Если подставить в это выражение массу и радиус Солнца, то оценочная солнечная температура T составит 14 миллионов градусов Кельвина, очень близко к температуре ядра Солнца (15 миллионов градусов Кельвина).Правда здесь надо отметить, что Солнце по структуре гораздо сложнее чем принято в этой упрощённой модели и её температура как и плотность изменяются сильно как функция радиуса, а такое хорошее согласие (≈7 % относительная ошибка) частично наше везение.[51]
Звездообразование
Полученные выше формулы можно использовать для определения условий для звездообразования из гигантских молекулярных облаков.[52] Местные колебания плотности в таких облаках могут привести к нестабильному состоянию, в котором облако сожмётся под собственной тяжестью. Такой коллапс происходит, когда теорема о равнораспределении или, эквивалентно, теорема о вириале больше не применимы, то есть, когда гравитационная потенциальная энергия в два раза превышает кинетическую энергию
Предполагая постоянную плотность ρ для облака формула
даёт оценку минимальной массы для зарождения звёзды , которая называется массой Джинса MJ
Подставляя значения типичных масс в таких наблюдаемых облаках (T=150 К, ρ = 2×10-16 г/см³) даёт оценку минимальной массы равную 17 солнечным массам, которая согласуется с наблюдаемым звёздообразованием. Этот эффект известен как нестабильность Джинса. Он назван в честь британского физика Джеймса Джинса, который опубликовал описание этой нестабильности в 1902 году.[53]
Выводы
Кинетическая энергия и распределение Максвелла—Больцмана
Первоначальная формулировка тероемы о равнораспределении гласит, что в физической системе при термодинамическом равновесии каждая частица обладает одинаковой средней кинетической энергией, (3/2)kBT.[54] Это можно показать используя распределение Максвелла — Больцмана (см. выше рисунок распределения плотности вероятности скоростей молекул), которое является распределением вероятности
для скорости частицы с массой m в системе, где скорость v — амплитуда
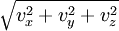 вектора скорости
вектора скорости 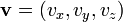 .
.Распределение Максвелла — Больцмана применимо для системы состоящей из атомов и предполагает только что система частиц представляет собой канонический ансамбль, в частности, что кинетические энергии распределены в соответствии с множителем Больцмана при температуре T.[54] Средняя кинетическая энергия для частицы массы m задаётся интегральной формулой
как и гласит теорема о равнораспределении. Тот же результат можно получить усредняя энергии частиц используя вероятность найти частицу в некотором энергетическом квантовом состоянии[43].
Квадратичные энергии и статистическая сумма
Более обще, теорема о равнораспределении гласит, что любая степень свободы x, которая появляется в полной энергии H только как квадратичное слагаемое вида Ax², где A — постоянная, имеет среднюю энергию ½kBT в термодинамическом равновесии. В этом случае равнораспределение можно вывести из статистической суммы Z(β), где β=1/(kBT) — обычная обратная температура.[55] Интегрирование по переменной x даёт множитель
в формуле для Z. Средняя энергия связанная с этим фактором дана выражением
как гласит теорема о равнораспределении.
Общие доказательства
общие выводы теоремы о равнораспределении можно найти в многих учебниках по статистической механике как для микроканонического ансамбля[3][5] так и для канонического ансамбля[3][41] Эти методы предполагают усреднение в фазовом пространстве системы, которое представляет собой симплектическое многообразие.
Для объяснения этих выводом нужно ввести следующие обозначения. Во первых, фазовое пространство описано в терминах обобщённых координат qj вместе с их сопряжёнными импульсами pj. Величины qj полностью описывают конфигурацию системы, в тоже время величины (qj,pj) вместе полностью описывают ей состояние.
Во вторых, вводят инфинитезимальный объём
dΓ = ∏ dqidpi i фазового пространства и используют, чтобы определить объём Γ(E, ΔE) как часть фазового пространства, где энергия системы H принимает значение в диапазоне энергий между E и E+ΔE:
В этом выражении, ΔE очень мало, ΔE<<E. Аналогично, Σ(E) определён как полный объём фазового пространства, где энергия меньше чем E:
Σ(E) = ∫ dΓ. H < E Из-за малости ΔE, следующее интегрирования эквивалентны
где точки представляют собой интегрируемое выражение. Из этого следует, что Γ пропорционален ΔE
где ρ(E) — плотность состояний. По обычным определениям из статистической механики, энтропия S равна kB log Σ(E), и температура T определена как
Канонический ансамбль
В каноническом ансамбле, система находится в тепловом равновесии с бесконечным тепловым резервуаром при температуре T (в Кельвинах).[3][41] Вероятность каждого состояния в фазовом пространстве задаётся её множителем Больцмана умноженном на нормирующий множитель
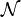 , который выбран таким образом, чтобы сумма вероятностей равнялась единице
, который выбран таким образом, чтобы сумма вероятностей равнялась единицегде β = 1/kBT. Интегрирование по частям для переменной в фазовом пространстве xk (которая может быть либо qk либо pk) между двумя пределами a и b приводит к уравнению
где dΓk = dΓ/dxk, то есть, первое интегрирование не производиться по xk. Первое слагаемое обычно равно нулю, потому, что xk равен нулю на пределах, или потому что энергия расходится на пределах. В этом случае теорема о равнорапределении немедленно следует из этого
Здесь, символ обозначающий усреднение
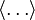 — усреднение по каноническому ансамблю.
— усреднение по каноническому ансамблю.Микроканонический ансамбль
В микроканиническом ансамбле, система изолирована от остального мира, или по крайней мере слабо связана.[5] Отсюда следует, что её полная энергия постоянная величина. Пусть для определённости полная энергия H находиться между E и E+ΔE. Для данной энергии E и неопределённости ΔE, имеется область в фазовом пространстве Γ когда система имеет эту энергию, и вероятности каждого состояния в этой области фазового пространства равны, по определнию микроканонического ансамбля. Из этих определений следует, что усреднение по переменным в фазовом пространстве xm (которые могут быть либо qk или pk) и xn задано в виде
где последнее равенство следует из того, что E не зависит от xn. Интегрирование по частям приводит к соотношению
поскольку первое слагаемое справа в первой строчке равно нулю (его можно записать как интеграл H — E по гиперпространству, где H = E).
Подставляя этот результат в предыдущее уравнение даёт
Поскольку
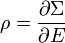 закон о равнораспределении гласит:
закон о равнораспределении гласит:Таким образом мы получили общую формулировку эквипарциальной теоремы
которая была использована в применениях показанных выше.
Применимость
 Энергия не делится между различными нормальными модами в изолированной системе идеальных связанных осцилляторов. Энергия в каждой моде является постоянной величиной и не зависит от энергии в других модах. Следовательно, теорема о равнораспределении не выполняется для такой системы в микроканоническом ансамбле (изолирована от теплового резервуара), хотя она выполняется для канонического ансамбля (соединена с тепловым резервуаром). Однако, добавляя достаточно сильное нелинейное взаимодействие между модами, энергия будет перераспределяться и теорема о равнораспределении станет выполняться в обоих ансамблях.
Энергия не делится между различными нормальными модами в изолированной системе идеальных связанных осцилляторов. Энергия в каждой моде является постоянной величиной и не зависит от энергии в других модах. Следовательно, теорема о равнораспределении не выполняется для такой системы в микроканоническом ансамбле (изолирована от теплового резервуара), хотя она выполняется для канонического ансамбля (соединена с тепловым резервуаром). Однако, добавляя достаточно сильное нелинейное взаимодействие между модами, энергия будет перераспределяться и теорема о равнораспределении станет выполняться в обоих ансамблях.Требование эргодичности
Закон равнораспределения выполняется только для эргодичных систем находящихся в термодинамическом равновесии, что подразумевает, что все состояния с равной энергией должны быть заполнены с равной вероятностью.[5] Следовательно, должен быть возможен обмен энергией между различными её формами в пределах системы, или с внешним тепловым резервуаром в каноническом ансамбле. Число физических систем, для которых известно строгое доказательство эргодичности мало. Наиболее известный пример — система твёрдых шаров Якова Синая.[56] Изученные требования для изолированных систем с гарантированной эргодичностью и, таким образом, равнораспределение, обеспечили предпосылки для современной теории хаоса динамических систем. Хаотическая гамильтова система не обязательно должна быть эргодичной, хотя это обычно хорошее приближение.[57]
Система связанных гармонических осцилляторов — обычно цитируемый контрпример, поскольку энергия не делится между различными её формами и равнораспределение не выполняется в микроканоническом ансамбле.[57] Если система изолирована от остального мира, энергия в каждой нормальной моде постоянна и энергия не передаётся от одной моды к другой. Следовательно, закон равнораспределения не выполняется для такой системы, поскольку количество энергии в каждой нормальной моде определяется её начальным значением. Если присутствуют достаточно сильные нелинейные слагаемые в энергии, то она может перераспределяться между нормальными модами, приводя к тому что закон равнораспределения выполняется. Однако, теорема Колмогорова — Арнольда — Мозера утверждает, что если нелинейные возмущения должны быть достаточно сильны для перераспределения энергии; в противном случае, когда они малы, энергия останется сконцентрирована в, по крайней мере, некоторых из мод.
Ограничения накладываемые квантовой механикой
-
См. также: Ультрафиолетовая катастрофа, История квантовой механики и Неразличимые частицы
Закон равнораспределения нарушается, когда тепловая энергия kBT становится значительно меньше, чем расстояние между энергетическими уровнями. Равнораспределение не работает, потому что предположение о непрерывном спектре энергетических уровней, которое использовалось выше при выводе закона равнораспределения, больше не является хорошим приближением.[3][5] Исторически, невозможность объяснить с помощью классической теоремы о равнораспределении удельную теплоёмкость и излучение абсолютно чёрного тела послужила основной причиной осознания того факта, что необходима новые теории материи и излучения, а именно квантовая механика и квантовая теория поля.[7]
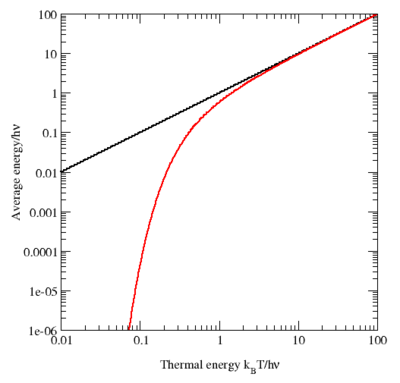 График средней энергии квантовомеханического осциллятора (красная кривая) в зависимости от температуры в логарифмическом масштабе. Для сравнения значение предсказанное теоремой о равнораспределении показаны чёрным. При высокой температуре две кривые имеют очень хорошее согласие, но при низких температурах, когда kBT << hν, квантовомеханическое значение уменьшается намного быстрее. Это приводит к решению проблемы ультрофиолетовой катастрофы: для данной температуры энергия высокочастотных мод (когда hν >> kBT) почти обращается в ноль.
График средней энергии квантовомеханического осциллятора (красная кривая) в зависимости от температуры в логарифмическом масштабе. Для сравнения значение предсказанное теоремой о равнораспределении показаны чёрным. При высокой температуре две кривые имеют очень хорошее согласие, но при низких температурах, когда kBT << hν, квантовомеханическое значение уменьшается намного быстрее. Это приводит к решению проблемы ультрофиолетовой катастрофы: для данной температуры энергия высокочастотных мод (когда hν >> kBT) почти обращается в ноль.Для иллюстрации нарушения теоремы о равнораспределении, рассмотрим среднюю энергию одиночного (квантового) гармонического осциллятора, который обсуждался выше для классического случая. Его квантовые уровни заданы в виде En = nhν, где h — постоянная Планка, ν — фундаментальная частота осциллятора, и n — целое положительное число. Вероятность того, что заданный уровень энергии окажется заполнен в каноническом ансамбле задаётся его множителем Больцмана
где β = 1/kBT и знаменатель Z — статистическая сумма, здесь геометрический ряд
Его средняя энергия задаётся в виде
Подставляя формулу для Z приводит к искомому результату[5]
При высоких температурах, когда тепловая энергия kBT много больше расстояния hν между энергетическими уровнями, экпоненциальный показатель βhν оказывается много меньше единицы и средняя энергия становится равной kBT, в соответствии с законом о равнораспределении (см. график). Однако, при низких температурах, когда hν >> kBT, средняя энергия стремится к нулю — высокочастотные уровни энергии «вымораживаются» (см. график). Другой пример, возбуждённые электронные состояния атома водорода не вносят вклада в удельную теплоёмкость газа при комнатной температуре, потому что тепловая энергия kBT (приблизительно 0.025 эВ) много меньше чем расстояние между основным состоянием и первым возбуждённым уровнем (приблизительно 10 эВ).
Аналогичные рассмотрения применимы в независимости от того больше ли расстояние между энергетическими уровнями чем тепловая энергия. Например, эта посылка была использована Альбертом Эйнштейном, чтобы разрешить ультрафиолетовую катастрофу излучения абсолютно чёрного тема.[58] Парадокс возникает из-за того, что имеется бесконечное число независимых мод электромагнитного поля в замкнутом контейнере, каждая из которых трактуется как гармонический осциллятор. Если каждая электромагнитная мода обладает средней энергией kBT, тогда в контейнере будет содержатся бесконечная энергия.[58][59] Однако, по причине обсуждаемой выше, средняя энергия в высокочастотных модах стремится к нулю когда частота стремится к бесконечности; более того, планковский закон излучения абсолютно чёрного тела, который следует из экспериментально найденного распределения энергии по модам следует из этой же причины.[58]
Есть более тонкие квантовые эффекты, которые могут привести к коррекциям теоремы равнораспределения, такие как тождественность частиц и непрерывные симметрии. Эффекты неразличимости частиц могут доминировать при больших концентрациях и низких температурах. Например, валентные электроны в металле могут иметь среднюю кинетическую энергию несколько электронвольт, которая соответствует температуре в десятки тысяч градусов. В состоянии, в котором плотность достаточно высокая, что принцип запрета Паули делает неприменимым классический подход, называется вырожденный ферми-газ. Такие газы важны в структуре белых карликов и нейтронных звёзд. При низких температурах формируется фермионный аналог конденсата Бозе — Эйнштейна (в котором много тождественных частиц занимают основное энергетическое состояние); такие сверхтекучие электроны ответственны за сверхпроводимость.
Примечания
- ↑ 1 2 Kundt, A.; Warburg E. (1876). "Über die specifische Wärme des Quecksilbergases (On the specific heat of mercury gases)". Annalen der Physik 157: 353–369. (нем.)
- ↑ Fact Sheet on Uranium Enrichment U.S. Nuclear Regulatory Commission. Accessed 30th April 2007
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 R. K. Pathria Statistical Mechanics. — Pergamon Press, 1972. — С. pp. 43–48, 73–74. — ISBN 0-08-016747-0
- ↑ 1 2 3 H. Goldstein Classical Mechanics. — 2nd. ed. — Addison-Wesley, 1980. — ISBN 0-201-02918-9
- ↑ 1 2 3 4 5 6 7 8 9 K. Huang Statistical Mechanics. — 2nd ed.. — John Wiley and Sons, 1987. — С. pp. 136–138. — ISBN ISBN 0-471-81518-7
- ↑ 1 2 F Mandl Statistical Physics. — John Wiley and Sons, 1971. — С. pp. 213–219. — ISBN ISBN 0-471-56658-6
- ↑ 1 2 3 4 A. Pais Subtle is the Lord. — Oxford University Press, 1982. — ISBN 0-19-853907-X
- ↑ 1 2 Tolman, R. C. (1918). "A General Theory of Energy Partition with Applications to Quantum Theory". Physical Review 11: 261–275.
- ↑ Miedl M, Garcia M, Bamforth C (2005). "Haze formation in model beer systems". J. Agric. Food Chem. 53 (26): 10161–5. DOI:10.1021/jf0506941. PMID 16366710.
- ↑ Mason, M; Weaver W (1924). "The Settling of Small Particles in a Fluid". Physical Review 23: 412–426. DOI:10.1103/PhysRev.23.412.
- ↑ S. G. Brush The Kind of Motion We Call Heat, Volume 1. — Amsterdam: North Holland, 1976. — С. 134–159. — ISBN 978-0444870094
- ↑ S. G. Brush The Kind of Motion We Call Heat, Volume 2. — Amsterdam: North Holland, 1976. — С. 336–339. — ISBN 978-0444870094
- ↑ Waterston, JJ (1846/1893). "On the physics of media that are composed of free and elastic molecules in a state of motion". Roy. Soc. Proc. 5: 604.(абстракт). Полностью не опубликован до (1893) "". Philos. Trans. R. Soc. London A183: 1–79. Переиздан The collected scientific papers of John James Waterston / J. S. Haldane. — Edinburgh: Oliver & Boyd, 1928.
- ↑ J. J. Waterston Thoughts on the Mental Functions. — 1843. (перепечатано в его Papers, 3, 167, 183.)
- ↑ Waterston, J. J. (1851). "". British Association Reports 21: 6. Основная статья Уотерстона была написана и подана в 1845 году в Королевское общество. После отказа напечатать работу общество также отказалось от возврата манускрипта и сохранило его среди других статей в архиве. Манускрипт был найден в 1891 году Лордом Рэлеем, который раскритиковал референта за то, что тот не распознал значительность работы Уотерстона. Уотерстону удалось опубликовать свои идеи в 1851 году, и поэтому он опередил Максвелла в изложении первой версии теоремы равнораспределения.
- ↑ J. C. Maxwell Illustrations of the Dynamical Theory of Gases // The Scientific Papers of James Clerk Maxwell / W. D. Niven. — New York: Dover, 2003. — С. Vol.1, pp. 377–409. — ISBN 978-0486495606 Read by Prof. Maxwell at a Meeting of the British Association at Aberdeen on 21 September 1859.
- ↑ Boltzmann, L. (1871). "Einige allgemeine Sätze über Wärmegleichgewicht (Some general statements on thermal equilibrium)". Wiener Berichte 63: 679–711. (нем.) В этой предварительной работе Больцман показал, что средняя полная кинетическая энергия равна средней полной потенциальной энергии, когда на систему действуют внешние гармонические силы.
- ↑ Boltzmann, L. (1876). "Über die Natur der Gasmoleküle (On the nature of gas molecules)". Wiener Berichte 74: 553–560. (нем.)
- ↑ 1 2 DA McQuarrie Statistical Mechanics. — revised 2nd ed.. — University Science Books, 2000. — С. pp. 91–128. — ISBN ISBN 978-1891389153
- ↑ Petit, A. T.; Dulong P. L. (1819). "Recherches sur quelques points importants de la théorie de la chaleur (Studies on key points in the theory of heat)". Annales de Chimie et de Physique 10: 395–413. (фр.)
- ↑ Dewar, J. (1872). "The Specific Heat of Carbon at High Temperatures". Philosophical Magazine 44: 461.
- ↑ Weber, HF (1872). "Die specifische Wärme des Kohlenstoffs (The specific heat of carbon)". Annalen der Physik 147: 311–319. (нем.)
- ↑ Weber, H. F. (1875). "Die specifische Wärmen der Elemente Kohlenstoff, Bor und Silicium (The specific heats of elemental carbon, boron, and silicon)". Annalen der Physik 154: 367–423, 553–582. (нем.)
- ↑ de la Rive, A.; Marcet F. (1840). "Quelques recherches sur la chaleur spécifique (Some research on specific heat)". Annales de Chimie et de Physique 75: 113–144. (фр.)
- ↑ Regnault, H. V. (1841). "Recherches sur la chaleur spécifique des corps simples et des corps composés (deuxième Mémoire) (Studies of the specific heats of simple and composite bodies)". Annales de Chimie et de Physique 1 (3me Série): 129–207. (фр.) Read at l’Académie des Sciences on 11 January 1841.
- ↑ Wigand, A. (1907). "Über Temperaturabhängigkeit der spezifischen Wärme fester Elemente (On the temperature dependence of the specific heats of solids)". Annalen der Physik 22: 99–106. (нем.)
- ↑ 1 2 A. Wüller Lehrbuch der Experimentalphysik (Textbook of Experimental Physics). — Leipzig: Teubner, 1896. — С. Vol. 2, 507ff. (нем.)
- ↑ 1 2 Eucken, A. (1912). "Die Molekularwärme des Wasserstoffs bei tiefen Temperaturen (The molecular specific heat of hydrogen at low temperatures)". Sitzungsberichte der königlichen Preussischen Akademie der Wissenschaften 1912: 141–151. (нем.)
- ↑ 1 2 J. C. Maxwell On the Dynamical Evidence of the Molecular Constitution of Bodies // The Scientific Papers of James Clerk Maxwell / WD Niven. — Cambridge: At the University Press, 1890. — С. Vol.2, pp.418–438. Лекция прочитанная профессором Максвеллом Химическому обществу 18 февраля 1875 года.
- ↑ 1 2 C. Kittel Introduction to Solid State Physics. — New York: John Wiley and Sons, 1996. — С. 151–156. — ISBN ISBN 978-0471111818
- ↑ Boltzmann, L. (1895). "On certain Questions of the Theory of Gases". Nature 51: 413–415.
- ↑ W. Thomson Baltimore Lectures. — Baltimore: Johns Hopkins University Press, 1904. — С. Sec. 27. Перепечатана в 1987 году издательством MIT Press под названием Kelvin’s Baltimore Lectures and Modern Theoretical Physics: Historical and Philosophical Perspectives (Robert Kargon and Peter Achinstein, editors). ISBN 978-0262111171
- ↑ Rayleigh, J. W. S. (1900). "The Law of Partition of Kinetic Energy". Philosophical Magazine 49: 98–118.
- ↑ Einstein, A. (1907). "Die Plancksche Theorie der Strahlung und die Theorie der spezifischen Wärme (The Planck theory of radiation and the theory of specific heat)". Annalen der Physik 22: 180–190.(нем.)
- ↑ Einstein, A. (1907). "Berichtigung zu meiner Arbeit: 'Die Plancksche Theorie der Strahlung und die Theorie der spezifischen Wärme' (Correction to previous article)". Annalen der Physik 22: 800. (нем.)
- ↑ Einstein, A. (1911). "Eine Beziehung zwischen dem elastischen Verhalten and der spezifischen Wärme bei festen Körpern mit einatomigem Molekül (A connection between the elastic behavior and the specific heat of solids with single-atom molecules)". Annalen der Physik 34: 170–174. (нем.)
- ↑ Einstein, A. (1911). "Bemerkung zu meiner Arbeit: 'Eine Beziehung zwischen dem elastischen Verhalten and der spezifischen Wärme bei festen Körpern mit einatomigem Molekül' (Comment on previous article)". Annalen der Physik 34: 590. (нем.)
- ↑ Einstein, A. (1911). "Elementare Betrachtungen über die thermische Molekularbewegung in festen Körpern (Elementary observations on the thermal movements of molecules in solids)". Annalen der Physik 35: 679–694. (нем.)
- ↑ Nernst, W. (1910). "Untersuchungen über die spezifische Wärme bei tiefen Temperaturen. II. (Investigations into the specific heat at low temperatures)". Sitzungsberichte der Königlich Preussischen Akademie der Wissenschaften 1910: 262–282. (нем.)
- ↑ Armin Hermann The Genesis of Quantum Theory (1899–1913). — original title: Frühgeschichte der Quantentheorie (1899–1913), translated by Claude W. Nash. — Cambridge, MA: The MIT Press, 1971. — С. pp. 124—145. — ISBN 0-262-08047-8, LCCN 73-151106
- ↑ 1 2 3 R. C. Tolman The Principles of Statistical Mechanics. — New York: Dover Publications, 1938. — С. pp. 93–98. — ISBN 0-486-63896-0
- ↑ Clausius, R. (1870). "Ueber einen auf die Wärme anwendbaren mechanischen Satz". Annalen der Physik 141: 124–130. (нем.)
Clausius, R. J. E. (1870). "On a Mechanical Theorem Applicable to Heat". Philosophical Magazine, Ser. 4 40: 122–127. - ↑ 1 2 L. Vu-Quoc, Configuration integral (statistical mechanics), 2008.
- ↑ D. A. McQuarrie Statistical Mechanics. — revised 2nd ed.. — University Science Books, 2000. — С. pp. 254–264. — ISBN 978-1891389153
- ↑ 1 2 R. C. Tolman Statistical Mechanics, with Applications to Physics and Chemistry. — Chemical Catalog Company, 1927. — С. pp. 76–77.
- ↑ Y. P. Terletskii Statistical Physics. — translated: N. Fröman. — Amsterdam: North-Holland, 1971. — С. pp. 83-84. — ISBN 0-7204-0221-2, LCCN 70-157006
- ↑ G. W. Collins The Virial Theorem in Stellar Astrophysics. — Pachart Press, 1978.
- ↑ S. Chandrasekhar An Introduction to the Study of Stellar Structure. — Chicago: University of Chicago Press, 1939. — С. pp. 49–53.
- ↑ V. Kourganoff Introduction to Advanced Astrophysics. — Dordrecht, Holland: D. Reidel, 1980. — С. pp. 59–60, 134–140, 181–184.
- ↑ H.-Y. Chiu Stellar Physics, volume I. — Waltham, MA: Blaisdell Publishing, 1968. — ISBN LCCN 67-17990
- ↑ R. W. Noyes The Sun, Our Star. — Cambridge, MA: Harvard University Press, 1982. — ISBN 0-674-85435-7
- ↑ D. A. Ostlie An Introduction to Modern Stellar Astrophysics. — Reading, MA: Addison-Wesley, 1996. — ISBN 0-201-59880-9
- ↑ Jeans, J. H. (1902). "The Stability of a Spherical Nebula". Phil. Trans. A 199: 1–53. DOI:10.1098/rsta.1902.0012.
- ↑ 1 2 D. A. McQuarrie Statistical Mechanics. — revised 2nd ed.. — University Science Books, 2000. — С. pp. 121–128. — ISBN 978-1891389153
- ↑ H. B. Callen Thermodynamics and an Introduction to Thermostatistics. — New York: John Wiley and Sons, 1985. — С. pp. 375–377. — ISBN 0-471-86256-8
- ↑ V. I. Arnold Théorie ergodique des systèms dynamiques. — Gauthier-Villars, Paris. (фр.) (English edition: Benjamin-Cummings, Reading, Mass. 1968), 1967.
- ↑ 1 2 L. E. Reichl A Modern Course in Statistical Physics. — 2nd ed.. — Wiley Interscience, 1998. — С. 326–333. — ISBN 978-0471595205
- ↑ 1 2 3 Einstein, A. (1905). "Über einen die Erzeugung und Verwandlung des Lichtes betreffenden heuristischen Gesichtspunkt (A Heuristic Model of the Creation and Transformation of Light)". Annalen der Physik 17: 132–148. DOI:10.1002/andp.19053220607. (нем.). An English translation is available from Wikisource.
- ↑ Rayleigh, J. W. S. (1900). "Remarks upon the Law of Complete Radiation". Philosophical Magazine 49: 539–540.
См. также
- Теорема о вириале
- Молекулярно-кинетическая теория
- Статистическая механика
- Квантовая статистическая механика
Ссылки
- Апплет, демонстрирующий закон равнораспределения в реальном времени для смеси одноатомных и двухатомных газов
- The equipartition theorem in stellar physics, written by Nir J. Shaviv, an associate professor at the Racah Institute of Physics in the Hebrew University of Jerusalem.
Литература
- K. Huang. Statistical Mechanics. — 2nd ed. — John Wiley and Sons, 1987. — P. 136—138. — ISBN 0-471-81518-7
- A. I. Khinchin. Mathematical Foundations of Statistical Mechanics / Пер. G. Gamow. — New York: Dover Publications, 1949. — P. 93—98. — ISBN 0-486-63896-0
- L. D. Landau, E. M. Lifshitz. Statistical Physics, Part 1. — 3rd ed. — Pergamon Press, 1980. — P. 129—132. — ISBN 0-08-023039-3
- F. Mandl Statistical Physics. — John Wiley and Sons, 1971. — P. 213—219. — ISBN 0-471-56658-6
- F. Mohling. Statistical Mechanics: Methods and Applications. — John Wiley and Sons, 1982. — P. 137—139, 270—273, 280, 285—292. — ISBN 0-470-27340-2
- R. K. Pathria. Statistical Mechanics. — Pergamon Press, 1972. — P. 43—48, 73—74. — ISBN 0-08-016747-0
- W. Pauli. Pauli Lectures on Physics: Volume 4. Statistical Mechanics. — MIT Press, 1973. — P. 27—40. — ISBN 0-262-16049-8
- R. C. Tolman. Statistical Mechanics, with Applications to Physics and Chemistry. — Chemical Catalog Company, 1927. — P. 72—81. ASIN B00085D6OO
- R. C. Tolman. The Principles of Statistical Mechanics. — New York: Dover Publications, 1938. — P. 93—98. — ISBN 0-486-63896-0
-
Wikimedia Foundation. 2010.

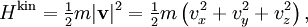
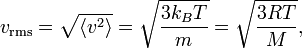
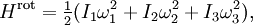
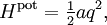
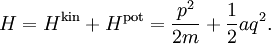
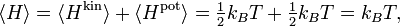
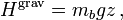
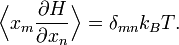
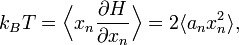
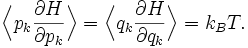
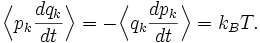
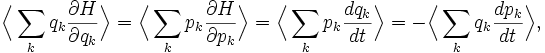
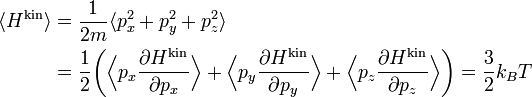
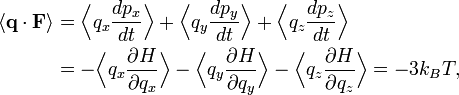
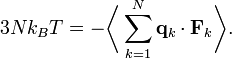
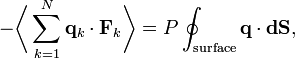
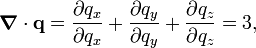

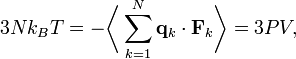
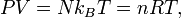
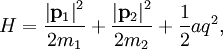
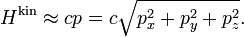
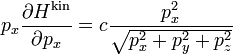
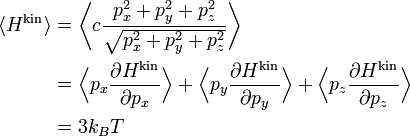
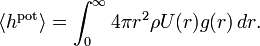
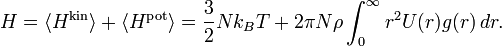
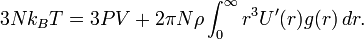
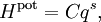
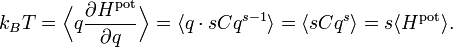
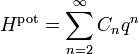
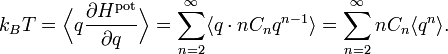
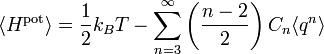
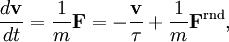
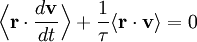
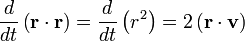
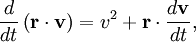
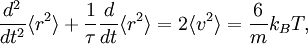
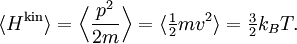
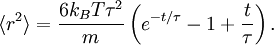
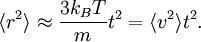
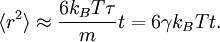
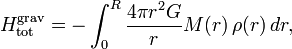
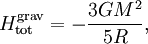
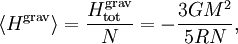
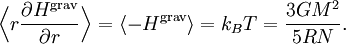
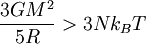
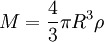
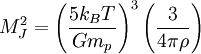
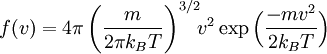
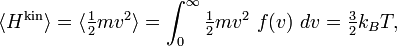
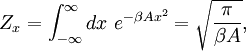
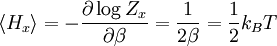
![\Gamma (E, \Delta E) = \int_{H \in \left[E, E+\Delta E \right]} d\Gamma .](/pictures/wiki/files/56/8271c8ebb7932467732895190cf75e2c.png)
![\int_{H \in \left[ E, E+\Delta E \right]} \ldots d\Gamma = \Delta E \frac{\partial}{\partial E} \int_{H &lt; E} \ldots d\Gamma,](/pictures/wiki/files/55/7bc53bad3dc34d9f27e63dab50234805.png)
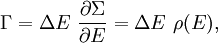
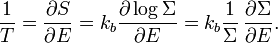
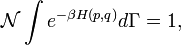
![\mathcal{N} \int \left[ e^{-\beta H(p, q)} x_{k} \right]_{x_{k}=a}^{x_{k}=b} d\Gamma_{k}+
\mathcal{N} \int e^{-\beta H(p, q)} x_{k} \beta \frac{\partial H}{\partial x_{k}} d\Gamma = 1,](/pictures/wiki/files/98/be8c97969d4fb474e30a9daa818f4327.png)
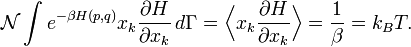
![\begin{align}
\Bigl\langle x_{m} \frac{\partial H}{\partial x_{n}} \Bigr \rangle &amp;=
\frac{1}{\Gamma} \, \int_{H \in \left[ E, E+\Delta E \right]} x_{m} \frac{\partial H}{\partial x_{n}} \,d\Gamma\\
&amp;=\frac{\Delta E}{\Gamma}\, \frac{\partial}{\partial E} \int_{H &lt; E} x_{m} \frac{\partial H}{\partial x_{n}} \,d\Gamma\\
&amp;= \frac{1}{\rho} \,\frac{\partial}{\partial E} \int_{H &lt; E} x_{m} \frac{\partial \left( H - E \right)}{\partial x_{n}} \,d\Gamma,
\end{align}](/pictures/wiki/files/49/171896bd98721d798bad87d4a7eec7e6.png)