- Хлорофилл a
-
Хлорофилл а 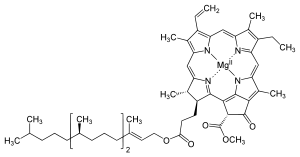
Общие Химическая формула C55H72N4O5Mg Физические свойства Молярная масса 893.49 г/моль Термические свойства Температура плавления 117-120 °C Температура кипения разлагается °C Классификация Рег. номер CAS 6433192 Безопасность NFPA 704
Хлорофилл a это особая форма хлорофилла, используемая для оксигенного фотосинтеза. Он поглощает максимальное количество энергии из фиолетово-голубой и оранжево-красной части спектра.[1] Этот пигмент жизненно необходим для фотосинтеза в клетках эукариот, цианобактерий и прохлорофитов из-за своей способности отдавать возбуждённые электроны в электрон-транспортную цепь.[2] Хлорофилл a также является частью антенного комплекса и передаёт резонансную энергию, которая затем поступает в реакционный центр, где расположены специальные хлорофиллы P680 и P700.[3]Содержание
Распространённость хлорофилла a
Хлорофилл a необходим большинству фотосинтезирующих организмов, для преобразования энергии света в химическую энергию, но это не единственный пигмент, который может быть использован для фотосинтеза. Все организмы с огсигенным типом фотосинтеза используют хлорофилл a, но имеют разные вспомогательные пигменты, как, например хлорофилл b.[2] В небольших количествах можно обнаружить хлорофилл a у зелёных серобактерий, — анаэробных фотоавтотрофов.[4] Эти организмы используют бактериохлорофиллы и некоторое количество хлорофилл a, но не производят кислород.[4] В отношении таких процессов употребляется термин аноксигенный фотосинтез.
Структура молекулы
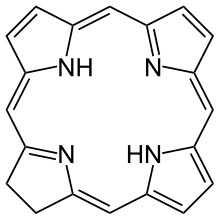
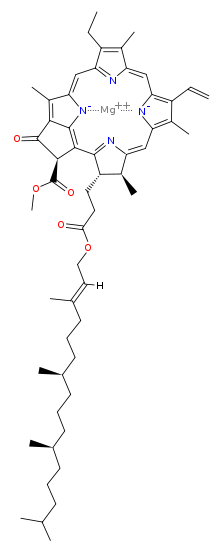
Молекула хлорофилла состоит из кольца хлорина с Mg в центре, радикалов-заместителей в кольце, и фитольного хвоста.
Кольцо хлорина
Хлорофилл a состоит из центрального иона магния, заключённого в кольцо из четырёх ионов азота, также известного, как хлорин. Хлориновое кольцо это гетероциклическое соединение, образованное из пирролов, окружающих атом металла. Именно Mg в центре однозначно отличает структуру молекулы хлорофилла от других молекул.[5]
Заместители
В кольце хлорофилла a есть заместители. Каждый тип хлорофиллов характеризуется своими заместителями, и, соответственно, своим спектром поглощения.[6]В качесте заместителей хлорофилл a содержит только метельные группы (CH3). В хлорофилле b метильная группа у третьего атома кольца (зелёная рамочка на картинке) замещена на альдегидную группу.[4] Порфириновое кольцо бактериохлорофиллов более насыщено — в нём не хватает чередования одинарной и двойной связи, что уменьшает спектр поглощаемого молекулами света.[7]
Фитольный хвост
К порфириновому кольцу присоединён длинный фитольный хвост.[2] Это длинный гидрофобный радикал, который прикрепляет хлорофилл a к гидрофобным белкам мембраны тилакоида.[2] Отсоединившись от порфиринового кольца, этот длинный гидрофобный хвост становится предшественником двух биомаркёров — пристана и фитана, оба из которых важны для геохимических исследований и определения качества нефти.
Биосинтез
В боиситнтезе хлорофилл a используется множество различных ферментов .[8] Любопытно заметить, что биосинтез бактериохлорофиллаa и хлорофилла a осуществляют схожие ферменты, которые, при некоторых условиях, могут взаимозаменять друг друга.[8] Всё начинается с глутаминовой кислоты, которая превращается в 5-аминолевулиновая кислота. Затем, две молекулы этой кислоты восстанавливаются до порфобилиногена, четыре молекулы которого формируют протопорфирин IX.[5] После формирования протопорфирина, фермент Mg-хелатаза катализирует включение иона Mg в структуру хлорофилла a .[8] Далее, происходит циклизация радикала в шестом положении кольца и образуется протохлорофиллид, у которого в ходе светозависимой реакции с участием фермента протохлорофиллид оксидоредуктаза происходит восстановление двойной связи в цикле D. [5] Завершается биосинтез хлорофилла присоединением фитольного хвоста.[9]
Реакции фотосинтеза
Поглощение света
Спектр Света
Хлорофилл a поглощает свет в фиолетовой, голубой и красной частях спектра, отражая в основном зелёный цвет, что и придаёт ему характерную окраску. Спектр его поглощения расширяется за счёт вспомогательных пигментов[2](например, совместное использование хлорофилла b вместе с хлорофиллом a). В условиях плохой освещённости, растения повышают соотношение хлорофилл b/хлорофилл a, синтезируя больше молекул первого чем второго, и, таким образом, увеличивают производительность фотосинтеза.[6]Светособирающая система
Кванты света, поглощённые пигментами, возбуждают их электроны, в результате чего энергия света преобразуется в энергию химической связи. Поскольку молекулы хлорофилла a могут поглощать только световые волны определённые длины, многие организмы используют вспомогательные пигменты (помечены на рисунке жёлтым цветом), что бы увеличить спектр поглощения.[3] Вспомогательные пигменты передают собранную энергию от одного пигмента к другому в виде резонансной энергии, до тех пор, пока она не достигнет специальной пары молекул хлорофилла a в реакционном центре[6] — P680 в фотосистеме II и P700 в фотосистеме I.[10] P680 и P700 основные доноры электронов для электрон-транспортной цепи.
См. также
- Хлорофилл
- Фотосистема I
- Фотосистема II
- P680
- P700
Источники
- ↑ PHOTOSYNTHESIS
- ↑ 1 2 3 4 5 Raven, Peter H.; Evert, Ray F.; Eichhorn, Susan E. Photosynthesis, Light, and Life // Biology of Plants. — 7th. — W.H. Freeman, 2005. — P. 119–127. — ISBN 0-7167-9811-5
- ↑ 1 2 Papageorgiou,G, and Govindjee (2004), Chlorophyll a Fluorescence, A Signature of Photosynthesis, vol. 19, Springer, p. 14,48,86
- ↑ 1 2 3 Eisen JA, Nelson KE, Paulsen IT, et al. (July 2002). «The complete genome sequence of Chlorobium tepidum TLS, a photosynthetic, anaerobic, green-sulfur bacterium». Proc. Natl. Acad. Sci. U.S.A. 99 (14): 9509–14. DOI:10.1073/pnas.132181499. PMID 12093901. See pages 9514,48,86.
- ↑ 1 2 3 Ch. 7: Topic 7.11: Chlorophyll Biosynthesis // Plant physiology. — 4th. — Sunderland, Mass: Sinauer Associates, 2006. — ISBN 0-87893-856-7
- ↑ 1 2 3 Lange, L.; Nobel, P.; Osmond, C.; Ziegler, H. Physiological Plant Ecology I – Responses to the Physical Environment. — Springer-Verlag, 1981. — Vol. 12A. — P. 67, 259.
- ↑ Biochemistry. — 6th. — Cengage Learning. — P. 647. — ISBN 978-0-495-39041-1
- ↑ 1 2 3 Suzuki JY, Bollivar DW, Bauer CE (1997). «Genetic Analysis of Chlorophyll biosynthesis.» (PDF). Annu. Rev. Genet 31 (1): 61–89. DOI:10.1146/annurev.genet.31.1.61.
- ↑ Zeiger & Taiz 2006, Figure 7.11.A: The biosynthetic pathway of chlorophyll
- ↑ Ishikita H, Saenger W, Biesiadka J, Loll B, Knapp EW (June 2006). «How photosynthetic reaction centers control oxidation power in chlorophyll pairs P680, P700, and P870». Proc. Natl. Acad. Sci. U.S.A. 103 (26): 9855–60. DOI:10.1073/pnas.0601446103. PMID 16788069.
Виды тетрапирроловБиланы
(Линейные)Билирубин · Биливердин · Стеркобилиноген · Стеркобилин · Уробилиноген · Уробилин Фитобилины Фитохромобилин Фикобилины Фикоэритробилин · Фикоцианобилин · Фикоуробилин · Фиковиолобилин Макроциклы Корриноиды Метилкобаламин · Аденозилкобаламин · Цианокобаламин · Гидроксокобаламин Порфирины Протопорфирины Протопорфирин IX · Гем (b, c, a, o) · Цинк-протопорфирин · Магний-протопорфирин Фитопорфирины Хлорофилл c1 · Хлорофилл c2 · Протохлорофиллид Редуцированные
порфириныПорфириногены Уропорфириноген (I, III) · Копропорфириноген (I, III) · Протопорфириноген IX Хлорины Хлорофиллид (a, Хлорофилл (a, b, d, f) · Феофитин (Феофорбид Бактериохлорины Бактериохлорофилл a Изобактериохлорины Сирогем · Сирогидрохлорин Корфины Кофактор F430 Категория:- Хлорофиллы
Wikimedia Foundation. 2010.