- Изолейцин
-
Изолейцин 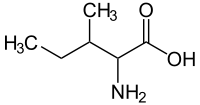
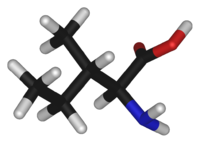
Общие Сокращения Иле, Ile, I
AUU,AUC,AUAХимическая формула HO2CCH(NH2)CH(CH3)CH2CH3 Эмпирическая формула C6H13O2N Физические свойства Молярная масса 131,17 г/моль Термические свойства Классификация SMILES CC[C@H](C)[C@H](N)C(O)=O Изолейцин (сокращенно Ile или I; 2-амино-3-метилпентановая кислота)[1] — это алифатическая α-аминокислота, имеющая химическую формулу HO2CCH(NH2)CH(CH3)CH2CH3 и входящая в состав всех природных белков. Является незаменимой аминокислотой, что означает, что изолейцин не может синтезироваться в организме человека и должен поступать в него с пищей. Участвует в энергетическом обмене. При недостаточности ферментов, катализирующих декарбоксилирование изолейцина, возникает кетоацидурия.
Кодоны изолейцина
AUU,AUCиAUA.Обладая углеводородной боковой цепью, изолейцин относится к числу гидрофобных аминокислот. Характерной особенностью боковой цепи изолейцина является её хиральность (второй такой аминокислотой является треонин). Для изолейцина возможно четыре стереоизомера, включая два возможных диастереоизомера L-изолейцина. В природе, однако, изолейцин присутствует лишь в одной энантиомерной форме — (2S,3S)-2-амино-3-метилпентановая кислота.
Содержание
Биосинтез
Как и другие незаменимые аминокислоты, изолейцин не синтезируется в организмах животных, и должен поступать извне, обычно в составе белков. В растениях и микроорганизмах изолейцин синтезируется посредством нескольких стадий, начиная от пировиноградной кислоты и альфа-кетоглутарата; процесс катализируется рядом ферментов[2].
Синтез
Изолейцин может быть синтезирован по многостадийной схеме, начиная с 2-бромбутана и диэтилмалоната. О получении изолейцина синтетическим путем впервые было сообщено в 1905.[3]
Примечания
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. Архивировано из первоисточника 21 августа 2011. Проверено 17 мая 2007.
- ↑ Nelson, D. L.; Cox, M. M. «Lehninger, Principles of Biochemistry» 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6
- ↑ Bouveault and Locquin, Compt. rend., 141, 115 (1905).
Ссылки
Аминокислоты Стандартные Нестандартные См. также  Категория:
Категория:- Аминокислоты
Wikimedia Foundation. 2010.
