- Спирты
-
Спирты́ (от лат. spiritus — дух; устар. алкого́ли) — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH), непосредственно связанных с насыщенным (находящемся в состоянии sp³ гибридизации) атомом углерода[1]. Спирты можно рассматривать как производные воды (H−O−H), в которых один атом водорода замещен на органическую функциональную группу: R−O−H.
В номенклатуре IUPAC для соединений, в которых гидроксильная группа связана с ненасыщенным находящемся в состоянии sp2 гибридизации атомом углерода, рекомендуются названия «енолы» (гидроксил связан с винильной C=C связью)[2] и «фенолы» (гидроксил связан с бензольным или другим ароматическим циклом)[3].
Спирты являются обширным и очень разнообразным классом органических соединений: они широко распространены в природе, имеют важнейшее промышленное значение и обладают исключительными химическими свойствами.
По мнению издания The 100 Most Important Chemical Compounds (Greenwood Press, 2007)[4], в сотне самых важных химических соединений четыре позиции занимают спирты (холестерин, этанол, глицерин и метанол).
Классификация спиртов
Спирты классифицируются следующим образом (в скобках приведены примеры)[5]:
- По числу гидроксильных групп:
— одноатомные спирты (метанол);
— двухатомные спирты (этиленгликоль);
— трехатомные спирты (глицерин);
— четырёхатомные спирты (пентаэритрит);
— многоатомные спирты (пятиатомный спирт: ксилит).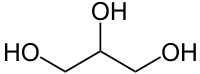
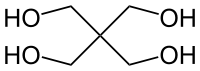
трёхатомный спирт глицерин четырёхатомный спирт пентаэритрит - В зависимости от насыщенности углеводородного заместителя:
— предельные или насыщенные спирты (бутанол);
— непредельные или ненасыщенные спирты (аллиловый спирт, пропаргиловый спирт);
— ароматические спирты (бензиловый спирт).- В зависимости от наличия или отсутствия цикла в углеводородном заместителе:
— алициклические спирты (циклогексанол);
— алифатические или ациклические спирты (этанол).- В зависимости от того, при каком атоме углерода находится гидроксильная группа:
— первичные спирты (пропанол);
— вторичные спирты (изопропиловый спирт);
— третичные спирты (2-метилпропан-2-ол).Номенклатура спиртов
Систематическая номенклатура
По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол», положение которого указывается арабской цифрой.
Правила построения названия спиртов (функциональная группа −OH)[6]:
1. Выбирается родительский углеводород по самой длинной непрерывной углеводородной цепи, содержащей функциональную группу. Он формирует базовое название (по числу атомов углерода).
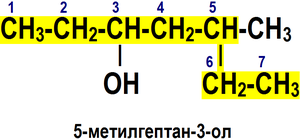
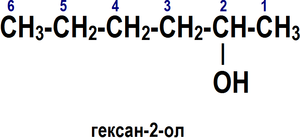
2. Родительский углеводород нумеруется в направлении, которое дает суффиксу функциональной группы самое низкое число.
3. Если в соединении помимо функциональной группы имеется другой заместитель, суффикс функциональной группы получает самое низкое число.
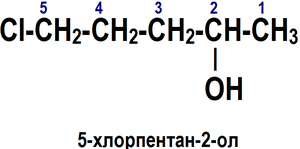
4. Если для суффикса функциональной группы получено одно и то же число в обоих направлениях, цепь нумеруется в направлении, которое дает другому заместителю самое низкое число.
5. Если имеется несколько заместителей, они перечисляются в алфавитном порядке.
Имена заместителей ставятся перед именем родительского углеводорода, а суффикс функциональной группы — после. ИЮПАК рекомендует цифру, характеризующую положение функциональной группы, писать сразу после имени углеводородного заместителя перед суффиксом функциональной группы.
Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, …) указывается количество гидроксильных групп (например: пропан-1,2,3-триол).
Рациональная и тривиальная номенклатура
Спирты, даже в научной литературе, часто называются по правилам, отличным от современной номенклатуры ИЮПАК. Очень распространённым является образование названия, как производного от соответствующего алкана, преобразованного в прилагательное с добавлением слова спирт:
Рациональная номенклатура спиртов рассматривает их как производные метанола CH3OH или по другому карбинола:
- (СH3)2CНOH → диметилкарбинол;
- (С6H5)3COH → трифенилкарбинол.
В популярной и научной литературе можно нередко встретить исторические или тривиальные названия спиртов, которые вследствие сложившейся традиции используются вместо официальной химической терминологии.
Систематические и тривиальные названия[5][7] некоторых спиртов приведены в таблице 1.
[T 1]Таблица 1. Систематические и тривиальные названия некоторых спиртов.Химическая формула спирта Название по номенклатуре ИЮПАК Тривиальное название Предельные одноатомные спирты CH3OH Метанол Древесный спирт C2H5OH Этанол Винный спирт C5H11OH Пентан-1-ол Амиловый спирт C16H33OH Гексадекан-1-ол Цетиловый спирт Предельные двух-, трех-, четырёхатомные спирты C2H4(OH)2 Этан-1,2-диол Этиленгликоль C3H5(OH)3 Пропан-1,2,3-триол Глицерин C5H8(OH)4 2,2-бис(Гидроксиметил)пропан-1,3-диол Пентаэритрит Предельные многоатомные спирты C5H7(OH)5 Пентан-1,2,3,4,5-пентол Ксилит C6H8(OH)6 Гексан-1,2,3,4,5,6-гексол Маннит, Сорбит Непредельные алифатические спирты C3H5OH Проп-2-ен-1-ол Аллиловый спирт C10H17OH 3,7-диметилокта-2,7-диен-1-ол Гераниол C3H3OH Проп-2-инол-1 Пропаргиловый спирт Алициклические спирты C6H6(OH)6 Циклогексан-1,2,3,4,5,6-гексол Инозит C10H19OH 2-(2-пропил)-5-метилциклогексанол-1 Ментол Этимология
Слово алкого́ль происходит из арабского языка الكحل (al-kuḥl) и означает «порошкообразная сурьма». В русский язык слово пришло через нем. Alkohol, нидерл. alkohol или порт. , исп. alcohol[8]. Однако в русском языке сохранился в виде архаизма, по всей видимости, и омоним слова «алкоголь» в значении «мелкий порошок».[9].
Слово спирт появилось в русском языке во времена Петра I через английское слово spirit, которое, в свою очередь, произошло от латинского spīritus — «дыхание, дух, душа»[10].
См. также об этимологии названий винного спирта (этанола)
История открытия спиртов
Этиловый спирт, вернее, хмельной растительный напиток, его содержащий, был известен человечеству с глубокой древности. Считается, что не менее чем за 8000 лет до нашей эры люди были знакомы с действием перебродивших фруктов, а позже — с помощью брожения получали хмельные напитки, содержащие этанол, из фруктов и мёда[11]. Археологические находки свидетельствуют, что в Западной Азии виноделие существовало ещё в 5400—5000 годах до н. э., а на территории современного Китая, провинция Хэнань, найдены свидетельства производства «вина», вернее ферментированных смесей из риса, мёда, винограда и, возможно, других фруктов, в эпоху раннего неолита: от 6500 до 7000 гг. до н. э.[12]
Впервые спирт из вина получили в VI—VII веках арабские химики, а первую бутылку крепкого алкоголя (прообраза современной водки) изготовил персидский алхимик Ар-Рази в 860 году[11]. В Европе этиловый спирт был получен из продуктов брожения в XI—XII веке, в Италии[13].
В Россию спирт впервые попал в 1386 году, когда генуэзское посольство привезло его с собой под названием «аква вита» и презентовало царскому двору[14].
В 1660 году английский химик и богослов Роберт Бойль впервые получил обезвоженный этиловый спирт, а также открыл его некоторые физические и химические свойства, в частности обнаружив способность этанола выступать в качестве высокотемпературного горючего для горелок[15]. Абсолютированный спирт был получен в 1796 году русским химиком Т. Е. Ловицем[13].
В 1842 году немецкий химик Я. Г. Шиль открыл, что спирты образуют гомологический ряд, отличаясь на некоторую постоянную величину. Правда, он ошибся, описав её как C2H2. Спустя два года, другой химик Шарль Жерар установил верное гомологическое соотношение CH2 и предсказал формулу и свойства неизвестного в те годы пропилового спирта[15]. В 1850 году английский химик Александр Вильямсон, исследуя реакцию алкоголятов с иодистым этилом, установил, что этиловый спирт является производным от воды с одним замещенным водородом, экспериментально подтвердив формулу C2H5OH[16]. Впервые синтез этанола действием серной кислоты на этилен осуществил в 1854 году французский химик Марселен Бертло[16].
Первое исследование метилового спирта было сделано в 1834 году французскими химиками Жаном-Батистом Дюма и Эженом Пелиго (англ.); они назвали его «метиловым или древесным спиртом», так как он был обнаружен в продуктах сухой перегонки древесины[17]. Синтез метанола из метилхлорида осуществил французский химик Марселен Бертло в 1857 году[18]. Им же был открыт в 1855 году изопропиловый спирт, действием на пропилен серной кислотой[19].
Впервые третичный спирт (2-метил-пропан-2-ол) синтезировал в 1863 году известный русский ученый А. М. Бутлеров, положив начало целой серии экспериментов в этом направлении[16].
Двухатомный спирт — этиленгликоль — впервые был синтезирован французским химиком А.Вюрцем в 1856 году[15]. Трехатомный спирт — глицерин — был обнаружен в природных жирах ещё в 1783 году шведским химиком Карлом Шееле, однако его состав был открыт только в 1836 году, а синтез осуществлен из ацетона в 1873 году Шарлем Фриделем[20].
Нахождение в природе
Спирты имеют самое широкое распространение в природе, особенно в виде сложных эфиров, однако и в свободном состоянии их можно встретить достаточно часто.
Метиловый спирт в небольшом количестве содержится в некоторых растениях, например: борщевике (Heracleum)[18].
Этиловый спирт — естественный продукт спиртового брожения органических продуктов, содержащих углеводы, часто образующийся в прокисших ягодах и фруктах без всякого участия человека. Кроме того, этанол является естественным метаболитом и содержится в тканях и крови животных и человека.
В эфирных маслах зелёных частей многих растений содержится 3(Z)-Гексен-1-ол («спирт листьев»), придающий им характерный запах[21]. Фенилэтиловый спирт — душистый компонент розового эфирного масла[22].
Очень широко представлены в растительном мире терпеновые спирты, многие из которых являются душистыми веществами, например:
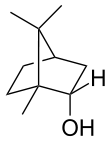
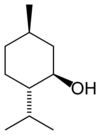
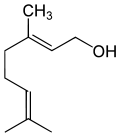
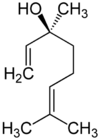
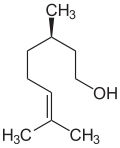
Борнеол — в древесине борнеокамфорного дерева[23]. Ментол — содержится в эфирном масле мяты и герани[24]. Гераниол — содержится во многих эфирных цветочных маслах[25]. Линалоол — содержится во многих цветочных эфирных маслах[26]. Цитронеллол — содержится во многих эфирных маслах[27]. 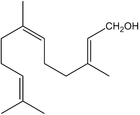
Фарнезол — содержится во многих эфирных цветочных маслах[28]. Терпинеол — содержится во многих эфирных маслах[29]. Бисаболол — входит в состав эфирного масла ромашки, тополя[30]. Санталол — входит в состав древесины сандалового дерева[31]. Фенхол — содержится в смоле хвойных деревьев и плодах фенхеля[32]. 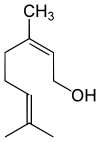
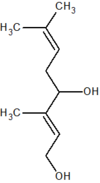
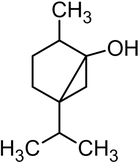
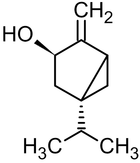
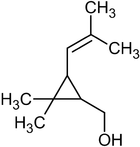
Нерол — содержится в эфирных маслах многих цветов[33]. Розиридол — содержится в эфирном масле родиолы розовой[33]. Туйол — содержится в эфирном масле шалфея[33]. Сабинол — содержится в эфирном масле тысячелистника[33]. Хризантемиловый спирт — в эфирном масле полыни однолетней[33]. В животном и растительном мире распространены конденсированные тетрациклические спирты (производные гонана), обладающие высокой биологической активностью и входящие в класс стероидов, например:

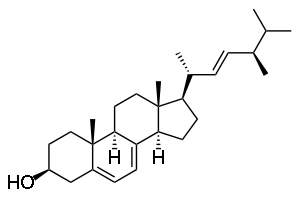
Холестерол (холестерин) — содержится в клетках практически всех живых организмов, особенно животных[34]. Эргостерол — содержится в некоторых водорослях и грибах[35]. Отдельную группу стероидов составляют жёлчные многоатомные спирты, находящиеся в жёлчи животных и человека: буфол, холестантетрол, холестанпентол, миксинол, сцимнол, химерол и пр.[36]
В природе находятся разнообразные многоатомные или сахарные спирты, например:
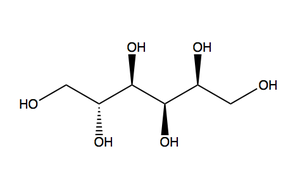

Сорбит — содержится в ягодах вишни и рябины[37]. Маннит — содержится в морских водорослях, грибах[38]. Физиологическая роль спиртов
Многие спирты являются незаменимыми участниками биохимических процессов, происходящих в живом организме.
Ряд витаминов можно отнести к классу спиртов:
- Витамин B8 — инозит или инозитол — витаминоподобное вещество, участвующее в липидном обмене[40].
Стероидные гормоны, среди которых имеются и спирты (например: холестерин или эргостерол), участвуют в регуляции обмена веществ и некоторых физиологических функциях организма[42].Полиизопреновый спирт долихол является липидным переносчиком полупродуктов при биосинтезе гликопротеинов[42].
Среди природных пигментов, участвующих в процессе фотосинтеза и поглощения света, каротиноидов, можно встретить множество соединений с гидроксильными группами.
Примеры фотосинтезирующих каротиноидов, сосредоточенных в хлоропластах растений[43]:
Примеры нефотосинтезирующих каротиноидов, сосредоточенных в клеточных мембранах или клеточной стенке бактерий[43]:
В 1959 году немецким химиком Адольфом Бутенадтом при изучении экстракта самки тутового шелкопряда впервые был открыто вещество, названное бомбиколом и вызывающее бурную реакцию самца[44].
Дальнейшее изучение феромонов насекомых привело к открытию, например, кодлелура (транс-8,транс-10-додекадиен-1-ол; другое название — кодлемон) — ненасыщенного спирта, являющегося половым аттрактантом яблонной плодожорки (Laspeyresia pomonella)[45]. Другой спирт — грандизол — половой аттрактант хлопкового долгоносика (Anthonomus grandis)[44]. Оказалось, что среди феромонов спирты занимают внушительное место; среди них, в частности: 9-додеценол, 11-гексадеценол, октадеканол, 3,7-октадиен-2-ол, производные циклогексанэтанола и циклобутанэтанола и пр[44].
Физиологическое действие и токсичность спиртов
Одноатомные предельные спирты вводят организм в наркозоподобное или гипнотическое состояние[46], а также оказывают токсическое действие. Эти эффекты усиливаются (токсический — начиная с этанола) с увеличением углеродной цепи, достигая максимума при С6—С8. Одноатомные спирты неразветвлённого строения с нечётным количеством атомов и спирты изо строения с чётным гораздо более токсичны за счёт образования опасных продуктов метаболизма — формальдегида и муравьиной кислоты.
Разветвленные, а также вторичные и третичные спирты обладают большей физиологической активностью. Введение в качестве заместителей галогенов значительно повышает наркотический эффект[47].
Пары спиртов оказывают раздражающее действие на слизистые оболочки; поражают зрение — метиловый, гексиловый, гептиловый, нониловый и дециловый спирты[48].
В связи с широким использованием простейших спиртов (метанол, этанол и изопропанол) в различных отраслях промышленности (подробнее см. раздел Промышленное применение спиртов) и, в частности, в качестве растворителей, опасным является их ингаляционное воздействие. Острое токсичное воздействие спиртов, испытанное на крысах, проявилось в следующих ингаляционных концентрациях:
- метиловый спирт: 3,16 % в течение 18—21 часов — 100 % летальность; 2,25 % в течение 8 часов — наркотический эффект; 0,8 % в течение 8 часов — летаргия;
- этиловый спирт: 3,2 % в течение 8 часов — частичная летальность; 2,2 % в течение 8 часов — глубокий наркоз; 0,64 % в течение 8 часов — летаргия;
- изопропиловый спирт: 1,2 % в течение 8 часов — 50 % летальность; 1,2 % в течение 4 часов — наркотический эффект[49].
Метиловый спирт — сильный яд (особенно при приеме внутрь) нервного и сердечно-сосудистого действия с выраженным кумулятивным эффектом; поражает органы зрения вплоть до полной слепоты. В больших дозах (30 грамм и более) вызывает смерть[50].
Этиловый спирт обладает токсическим эффектом. Быстро всасывается через слизистую оболочку желудка и тонкого кишечника, достигая максимальной концентрации в крови через 20—60 минут после его приёма, вызывая вначале возбуждение, а затем резкое угнетение центральной нервной системы (в том числе разрушает мозговую оболочку); его употребление приводит к нарушению важнейших функций организма, тяжелому поражению органов и систем. Оказывает эмбриотоксическое и тератогенное действие[50].
Изопропиловый спирт по своему токсическому воздействию напоминает этанол, вызывая угнетение центральной нервной системы и поражая внутренние органы. В высокой концентрации приводит к коме, конвульсиям и летальному исходу (около 3—4 г/кг)[51].
Аллиловый спирт — вызывает острое отравление, в больших количествах при приеме внутрь — потеря сознания, тяжёлая кома и смерть. Пары оказывают сильное раздражающее действие на глаза и верхние дыхательные пути[48].
Этиленгликоль — очень токсичен при пероральном попадании в организм; поражает ЦНС и почки, вызывает гемолиз эритроцитов; обладает мутагенным действием[50].
См. также: Токсикология этанолаФизические свойства и строение спиртов
Строение и особенности химической связи в спиртах
Спирты геометрически подобны молекуле воды. Угол R−O−H в молекуле метанола равен 108.5°[52]. Гидроксильный кислород находится в состоянии sp³ гибридизации:

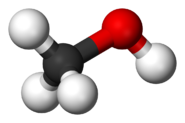
Подобно воде, спирты имеют существенно более высокие температуры плавления и кипения, чем можно было бы предполагать на основании физических свойств родственных соединений.
Так, из ряда монозамещённых производных метана, метанол имеет необычно высокую температуру кипения, несмотря на относительно небольшую молекулярную массу (см. таблицу 2.)[53]:
[T 2]Таблица 2. Зависимость температуры кипения некоторых монозамещённых метана от молекулярной массы.
Метан
CH4Метанол
CH3OHХлорметан
CH3ClНитрометан
CH3NO2Бромметан
CH3BrМолярная масса, г/моль 16,04 32,05 50,50 61,04 94,94 Температура кипения, °С −161,6 64,7 −24,2 25,0 3,6 Этот феномен объясняется наличием в спиртах водородных связей[52].
Энергия разрыва водородной связи значительно меньше, чем обычной химической связи, но тем не менее, она существенным образом влияет на физические свойства спиртов.
[T 3]Таблица 3. Энергия связей в метаноле.
Энергия связи, кДж/моль Водородная связь Связь С—H Связь С—O Связь O—H 16,7[54] 391,7[55][К 1] 383,5[55] 428,8[55] Молекулы спирта, имея две полярных связи C−O и O−H, обладают дипольным моментом (для алканолов: 5,3-6,0·10−30 Кл·м)[52]. Электростатические заряды в молекуле метанола составляют: на атоме углерода 0,297 e; на атоме гидроксильного водорода 0,431 e; на атоме кислорода −0,728 e[56]. Вместе с тем, энергия ионизации спиртов ниже, чем у воды[57], что объясняется электронодонорным эффектом алкильной группы:
- Вода: 12,61 эВ;
- Метиловый спирт: 10,88 эВ;
- Этиловый спирт: 10,47 эВ;
- Изопропиловый спирт: 10,12 эВ;
- Аллиловый спирт: 9,67 эВ.
Следует отметить, что влияние гидроксильной группы особенно велико на соединения с небольшой углеводородной цепочкой. Так, например, метанол и этанол неограниченно смешиваются с водой и имеют довольно высокие плотности и температуры кипения для своей молекулярной массы, в то время как высшие спирты гидрофобны и мало отличаются по свойствам от соответствующих углеводородов (см. таблицу 4.)[58]:[стр. 401].
[T 4]Таблица 4. Сравнение температур кипения и плотностей некоторых высших алканов и соответствующих алканолов.
Октан
C8H18Октанол
C8H17OHДекан
C10H22Деканол
C10H21OHДодекан
C12H26Додеканол
C12H25OHМолярная масса,
г/моль114,23 130,23 142,28 158,28 170,33 186,33 Температура кипения, °С[59][60] 125,7 195,1 174,1 231,0 216,3 263,5 Плотность при 20°С, кг/м3.[59][60] 702,5 822,7 730,0 826,0 748,7 830,9 Диссоциация и кислотно-основные свойства спиртов
Кислотные свойства спиртов
Спирты подобно воде способны проявлять как кислотные, так и основные свойства.
Как слабые кислоты, спирты способны диссоциировать по связи O−H с образованием алкоксид-иона:
Кислотные характеристики спиртов оценивают по константе кислотности
 :
:![K_\mathrm{a}=\frac{[\mathsf{R\!\!-\!\!O^-}]\cdot[\mathsf{H_3O^+}]}{[\mathsf{R\!\!-\!\!OH}]};](799f169f2327671c2fc9852c94871cc9.png)

В водном растворе кислотные свойства спиртов снижаются с увеличением молекулярной массы и разветвлённости углеводородной цепи[61]:
- CH3OH > CH3CH2OH > CH3CH2CH2OH > (CH3)2CHOH > (CH3)3COH
В газообразной фазе наблюдается обратный эффект (это связано с образованием межмолекулярной водородной связи в растворе и конденсированном состоянии)[61]:
- CH3OH < CH3CH2OH < CH3CH2CH2OH < (CH3)2CHOH < (CH3)3COH
Для оценки кислотности в газовой фазе используют энергию диссоциации
 .
.В таблице 5. представлены значения
 и
и  при 25 °C для некоторых спиртов и сравнительные данные по другим соединениям[62].
при 25 °C для некоторых спиртов и сравнительные данные по другим соединениям[62].[T 5]Таблица 5. Значения констант кислотности и энергии диссоциации некоторых гидроксильных соединений.
FCH2COOH CH3COOH CH3OH H2O C2H5OH (CH3)2CHOH (CH3)3COH C6H5CH3 Водный раствор, 
2,59 4,76 15,49 15,74 15,90 17,17 19,29 42[К 2]  ,
,
кДж/моль1383,4 1428,6 1560,1 352,5 1547,1 1538,7 1535,4 1558,8 Важным фактором, оказывающим влияние на кислотность спиртов, является индукционный эффект заместителя. Электроноакцепторные заместители (NO2−, CN−, F−, Cl−, Br−, I−, CH3O−) увеличивают кислотность спиртов (уменьшают
 ), в этом случае говорят, что они проявляют — I эффект (отрицательный индуктивный эффект); электронодонороные заместители (алкильные заместители, COO−) уменьшают кислотность спиртов (увеличивают
), в этом случае говорят, что они проявляют — I эффект (отрицательный индуктивный эффект); электронодонороные заместители (алкильные заместители, COO−) уменьшают кислотность спиртов (увеличивают  ), в этом случае говорят, что они проявляют + I эффект (положительный индуктивный эффект)[62].
), в этом случае говорят, что они проявляют + I эффект (положительный индуктивный эффект)[62].Так, например,
 2,2,2-трифторэтанола имеет значение 12,43 (против 15,9 у этанола), а нонафтор-трет-бутанола 5,4 (против 17,7 у трет-бутанола)[63]:[стр. 604, 658].
2,2,2-трифторэтанола имеет значение 12,43 (против 15,9 у этанола), а нонафтор-трет-бутанола 5,4 (против 17,7 у трет-бутанола)[63]:[стр. 604, 658].Следует помнить, что стерические препятствия заместителей могут оказывать влияние на образование водородных связей и существенно снижать кислотные свойства спиртов.
Осно́вные свойства спиртов
Спирты могут также вести себя как слабые основания Льюиса, образовывая с сильными минеральными кислотами соли алкоксония, а также давая донорно-акцепторные комплексы с кислотами Льюиса.
Обычно подобные реакции не останавливаются на указанной стадии и ведут к нуклеофильному замещению гидроксильной группы или отщеплению воды.
Спирты довольно слабые основания и их относительная основность, в отличие от кислотности, сохраняется как в растворе, так и газовой фазе[64]:[стр. 20]:
- CH3OH < CH3CH2OH < CH3CH2CH2OH < (CH3)2CHOH < (CH3)3COH
Основность спиртов оценивают по константе основности
 [65]:
[65]:![K_\mathrm{BH+}=\frac{[\mathsf{R\!\!-\!\!OH}]\cdot[\mathsf{H^+}]}{[\mathsf{R\!\!-\!\!OH_2^+}]};](35f69ceaa909c81c91c4e6eae320f7c7.png)

В таблице 6. представлены значения
 при 25 °C для воды и некоторых спиртов[64]:[стр. 19].
при 25 °C для воды и некоторых спиртов[64]:[стр. 19].[T 6]Таблица 6. Значения констант основности некоторых спиртов и воды.
H2O CH3OH C2H5OH C3H7OH (CH3)2CHOH (CH3)3COH CF3CH2OH Водный раствор, 
−3,43 −2,18 −1,94 −1,90 −1,73 −1,43 −4,35 Основные физические константы
[T 7]Таблица 7. Некоторые физические константы для алифатических предельных спиртов[60].
Наименование Формула Температура кипения, °С Температура плавления, °С Плотность, кг/м3 при 20°С Показатель преломления, nD20 Метанол CH3OH 64,7 −97,78 791,5 1,32855 Этанол C2H5OH 78,3 −114,65 789,5 1,36139 Пропан-1-ол C3H7OH 97,2 −124,10 803,5 1,38556 Пропан-2-ол CH3CH(CH3)OH 82,5 −87,95 786,2 1,37711 Бутан-1-ол C4H9OH 117,8 −88,64 808,6 1,39929 2-метилпропан-1-ол (СН3)2СНСН2ОН 108,0 −101,97 802,1 1,39549 Бутан-2-ол СН3СН2СН(ОН)СН3 99,5 −114,70 806,0 1,39240[К 3] 2-метилпропан-2-ол (СН3)2С(OH)СН3 82,9 25,82 765,2[К 4] 1,38779 Пентан-1-ол C5H11OH 138,0 −77,59 813,3 1,40999 Гексанол C6H13OH 157,1 -47,40 821,7 1,41816 Гептанол C7H15OH 176,3 −32,80 824,0 1,42351 Октанол C8H17OH 195,1 −16,30 822,7 1,42920 Нонанол C9H19OH 213,5 −5,00 827,0 1,43325 Деканол C10H21OH 231,0 6,00 826,0 1,43660 [T 8]Таблица 8. Некоторые физические константы для ряда алициклических, ароматических и непредельных спиртов[66]:
Наименование Формула Температура кипения, °С Температура плавления, °С Плотность, кг/м3 при 20°С Показатель преломления, nD20 2-пропен-1-ол CH2=CHCH2OH 96,9 −129 852,0 1,4133 2-пропин-1-ол CH≡CCH2OH 113,6 −48 948,5 1,4322 Циклогексанол C6H11OH 161,1 25,15 941,6 1,4648 Фенилкарбинол C6H5CH2OH 205,0 −15,3 1041,9 1,5396 2-Фенилэтанол C6H5CH2CH2OH 218,2 −27,0 1020,2 1,5325 3-Фенил-2-пропен-1-ол C6H5CH=CHCH2OH 256—258 34 1044,0 1,5819 2-Фуранкарбинол (C4H3O)CH2OH 155 — 1131,9 1,5324 Получение спиртов
Общие химические методы получения спиртов
Спирты могут быть получены из самых разных классов соединений, таких как углеводороды, алкилгалогениды, амины, карбонильные соединения, эпоксиды. Существует множество методов получения спиртов, среди которых выделим наиболее общие:
- реакции окисления — основаны на окислении углеводородов (реже — галогенпроизводных углеводородов), содержащих кратные или активированные C−H связи;
В качестве окислительных агентов для алканов и циклоалканов используются сильные неорганические окислители: озон, перманганат калия, оксид хрома (VI), хромовая кислота, диоксид селена, а также пероксид водорода и некоторые пероксикислоты. Из-за возможности более глубокого окисления, метод имеет значение, как правило, только для получения третичных спиртов[67]:[cтр. 57—59]:
Окисление алкенов значительно более распространено в лабораторной практике, особенно когда речь идёт о получении диолов. В зависимости от выбора реагента можно осуществить син-гидроксилирование (тетраоксид осмия, перманганат калия, хлорат натрия, иод с карбоксилатом серебра и пр.) или анти-гидроксилирование (пероксид водорода и пероксикислоты, оксиды молибдена(VI) и вольфрама(VI), оксид селена(IV) и пр.)[68]:
Алкены также могут гидроксилироваться в аллильное положение синглетным кислородом с миграцией двойной связи и образованием гидропероксидов, которые затем восстанавливаются до спиртов[69]:
Важным препаративным методом является окисление галогенпроизводных углеводородов надпероксидом калия[70].
- реакции восстановления — восстановление карбонильных соединений: альдегидов, кетонов, карбоновых кислот и сложных эфиров;
Для восстановления альдегидов или кетонов, обычно, пользуются борогидридом натрия или калия, а также алюмогидридом лития в протонном растворителе[69]:
Восстановление сложных эфиров и карбоновых кислот производится алюмогидридом или борогидридом лития, а также некоторыми другими комплексными гидридами[69]:
- реакции гидратации — кислотно-катализируемое присоединение воды к алкенам (гидратация);
Реакция имеет промышленное значение (например: синтез этанола), однако в лабораторной практике часто замещается реакцией оксимеркурирования-демеркурирования алкенов или гидроборированием алкенов с их последующим окислением[69]:
- реакции присоединения:
-
- присоединение синтез-газа, формальдегида, оксирана по кратным углеводородным связям;
Простейший пример такой реакции — промышленный синтез метанола[71]:
Среди других вариантов использования:
-
- присоединение нуклеофилов к карбонильным соединениям;
Общая схема реакций подобного типа:
Существует множество реакций присоединения, включая реакции гидратации, этинилирования и прочих, рассмотренных выше. Здесь приведём примеры некоторых важных препаративных методов.
Присоединение аллиборанов с последующим гидролизом[72]:
Реакция Бэйлиса — Хиллмана — Морита[73]:
- реакции замещения (гидролиза) — реакции нуклеофильного замещения, при которых имеющиеся функциональные группы замещаются на гидроксильную группу;
На практике для реакций замещения, как правило, используются галогенпроизводные:
- синтезы с использованием металлорганических соединений.
Использование металлорганических соединений для синтеза спиртов — мощный препаративный метод, позволяющий получить спирты из различных производных.
-
- синтез через реактивы Гриньяра[74]:
-
- реакция Циглера[75]:
-
- синтез с использованием органокупратов[76]:
Получение наиболее важных спиртов в промышленности
Промышленные способы получения спиртов можно разделить на две большие группы:
- химические методы производства;
- биохимические методы производства.
Использование этих методов для производства отдельных спиртов представлено в таблицах 9—11.
[T 9]Таблица 9. Основные современные процессы, используемые для промышленного получения спиртов[66][77].
№ Наименование (тип) процесса Получаемые спирты 1. Гидратация алкенов или эпоксидов Этанол, пропан-2-ол, бутан-2-ол, 2-метилпропан-2-ол, этиленгликоль 2. Щелочной гидролиз галогенпроизводных Аллиловый спирт, глицерин, бензиловый спирт 3. Щелочной гидролиз сложных эфиров Глицерин, октан-2-ол, высшие жирные спирты 4. Реакция гидроформилирования (оксосинтез) Метанол, пропан-1-ол, бутан-1-ол, пентан-1-ол, гексанол 5. Окислительные методы Пропан-1-ол, бутан-1-ол, высшие жирные спирты 6. Восстановительные методы Циклогексанол, ксилит, высшие жирные спирты 7. Реакция конденсации карбонильных соединений Бутан-1-ол, 2-этилгексанол, пентаэритрит 8. Биохимические методы Этанол, бутан-1-ол, глицерин [T 10]Таблица 10. Основные химические промышленные способы получения экономически наиболее важных спиртов.
Наименование и формула спирта Химическая реакция (схематично) Краткое описание процесса Краткие характеристики процесса Мировое производство Источники Метанол
CH3OHCO + 2H2 → CH3OH Каталитический синтез из оксида углерода и водорода Смешанный медно-цинково-хромовый катализатор, температура 250 °C, давление до 10 МПа 40,0 млн тонн[К 5] [71][78] Этанол
C2H5OHCH2=CH2 + H2O → C2H5OH Сернокислотная или прямая гидратация этилена Вариант 1: абсорбция этилена концентрированной серной кислотой (94—98 %) при температуре 80 °C и давлении 1,5 МПа и последующий гидролиз сульфоэфира. Вариант 2: прямая гидратация при 300 °C и давлении 7 МПа, катализатор: фосфорная кислота, нанесённая на оксид кремния(IV).
6 млн тонн[К 6] [79][80]:[стр. 69—73] Пропанол-1
C3H7OHCH2=CH2 + CO + 2H2 → C3H7OH Гидроформилирование этилена с последующим гидрированием Первый этап: температура 80—120 °С, давление 2 МПа, катализатор: карбонил родия. Второй этап: медно-хромовые или никель-хромовые катализаторы. 0,14 млн тонн[К 7] [81][82] Пропанол-2
CH3CH(OH)CH3CH3-CH=CH2 + H2O → CH3CH(OH)CH3 Сернокислотная или прямая гидратация пропилена Вариант 1: абсорбция пропилена серной кислотой (70—75 %) при комнатной температуре 80 °C и давлении 2—3 МПа и последующий гидролиз сульфоэфира. Вариант 2: прямая гидратация на фосфорнокислом (180 °C и 4 МПа) или вольфрамовом (250 °C и 25 МПа) катализаторе.
1,8 млн тонн[К 5] [83][84][80]:[стр. 76—79] Высшие жирные спирты 1. RCOOCH3 + 2H2 → RCH2OH + CH3OH
2. RCH=CH2 + CO + 2H2 → RCH2CH2CH2OH
3. Al(C2H5)3 + 3nC2H4 → Al[(C2H4)nC2H5]3 + O2 → 3C2H5(C2H4)nOH1. Гидрирование метиловых эфиров жирных кислот, получаемых переэтерификацией жиров и масел.
2. Гидроформилирование алкенов.
3. Метод Циглера.1. Гидрирование при высокой температуре (до 290 °C) и давление (до 20,7 МПа) на смешанных меднохромовых или других катализаторах.
2. Высокотемпературный газофазный процесс в присутствии модифицированного карбонила кобальта.
3. Многостадийный синтез в относительно мягких условиях.2,15 млн тонн[К 8] [85]:[стр. 18—20][86]. Этиленгликоль
HOCH2CH2OH(CH2CH2)O + H2O → HOCH2CH2OH Некаталитическая гидратация окиси этилена Температура 200 °C и давление 1,5—2 МПа 18,0 млн тонн[К 5] [87] Глицерин
HOCH2CH(OH)CH2OHCH2(OCOR)CH(OCOR)CH2OCOR + 3NaOH → HOCH2CH(OH)CH2OH + 3RCOONa Щелочной гидролиз растительных жиров и масел Температура 150—180 °С, давление 1 МПа, катализаторы. 1,5 млн тонн[К 5] [88][89]:[стр. 2.251][90]:[стр. 242] [T 11]Таблица 11. Получение спиртов биохимическими методами.
Наименование спирта Исходное сырьё Краткое описание процесса Этанол целлюлозное сырьё: древесина, солома, багасса, отходы деревообрабатывающего и целлюлозного производства Кислотный или энзимный гидролиз растительного сырья с последующей анаэробной спиртовой ферментацией (сбраживанием) образующихся моно- и олигосахаридов дрожжевыми грибами (Saccharomyces) или некоторыми видами бактерий[91]. крахмал- и сахарсодержащее сырьё: сахарная свекла, картофель, маниок, злаковые культуры (рис, ячмень, пшеница, сорго, кукуруза, сахарный тростник и др.) Бутанол крахмалсодержащее сырьё: сахарная свекла, картофель, маниок, злаковые культуры (рис, ячмень, пшеница, сорго, кукуруза, сахарный тростник и др.) Аналогично производству биоэтанола, но с применением бутанольной ферментации бактериями Clostridium[92]. Глицерин сыворотка, сахарная меласса, пшеничный гидролизат Ферментация сахаросодержащего сырья дрожжевыми грибами (Saccharomyces cerevisiae или Kluyveromyces fragilis) в присутствии сульфита натрия[93]. Химические свойства спиртов
Все химические реакции спиртов можно разделить на три условных группы, связанные с определёнными реакционными центрами и химическими связями:
- Разрыв связи O−H (реакционный центр — водород)
- Разрыв или присоединение по связи С−OH (реакционный центр — кислород)
- Разрыв связи −СOH (реакционный центр — углерод)
Образование алкоголятов
Спирты ведут себя как слабые кислоты, вступая в реакцию по связи O−H со щелочными и некоторыми другими металлами, и с сильными основаниями, например:
Вода имеет сравнимую с многими спиртами константу диссоциации кислоты, поэтому в реакции с сильными основаниями химическое равновесие, как правило, смещено влево (в сторону исходных продуктов):
- R−OH + NaOH ⇌ R−O-Na+ + H2O (равновесие смещено влево)
Кислотность спиртов зависит от стабильности алкоксидного аниона R−O−. Электроноакцепторные группы, связанные с атомом углерода, несущим гидроксильную группу, стабилизируют этот анион и таким образом повышают кислотность, а электонодонорные уменьшают его стабильность, в результате повышается вероятность обратного присоединения протона и кислотность снижается.
Нуклеофильное замещение
См. также: Превращение спиртов в галогеналканы и ЭтерификацияГидроксильная группа может подвергаться нуклеофильному замещению с разрывом связи C−O, например:
По тому же механизму происходит в условиях кислотного катализа реакция этерификации (взаимодействие спиртов с карбоновыми кислотами, приводящая к получению сложных эфиров):
В общем случае, гидроксильная группа не может быть уходящей группой в таких реакциях, но после протонирования (превращения в R−OH2+ под воздействием кислоты) она легко замещается с отщеплением воды.
Дегидратация
См. также: Реакции элиминирования спиртов и Межмолекулярная и внутримолекулярная дегидратация спиртовВ присутствии катализаторов (таких, как оксид алюминия или безводная серная кислота) спирты могут подвергаться реакции элиминирования по механизму E1, с разрывом связи C−O и образованием алкенов. Например, дегидратация этилового спирта приводит к образованию этилена (показан механизм элиминации под действием кислотного катализатора):
Реакция протекает в соответствии с правилом Зайцева, согласно которому образуется наиболее стабильный углеводород.
Спирты сами являются нуклеофильными агентами, поэтому протонированная гидроксигруппа R−OH2+ может реагировать с молекулой спирта R−OH с образованием простого эфира и отщеплением воды. Эта реакция используется в основном при получении диэтилового эфира.
Окисление
См. также: Реакции окисления спиртовПервичные спирты (R−CH2−OH) могут быть окислены до альдегидов (R−CHO), а дальнейшее окисление, которое часто бывает трудно приостановить, приводит к карбоновым кислотам (R−CO2H). Окисление вторичных спиртов (R1R2CH−OH) как правило заканчивается на стадии кетонов (R1R2C=O) без разрыва углеводородной цепи. Третичные спирты (R1R2R3C−OH) устойчивы к окислению, а при вступлении в реакцию образуют смесь карбоновых кислот.
Идентификация спиртов
Химические методы идентификации спиртов
Качественный анализ гидроксильных групп
Существует множество относительно простых тестов, позволяющих выявить в органическом соединении наличие гидроксильного фрагмента (−OH), однако все они имеют довольно ограниченное применение и не являются универсальными: часто присутствие прочих функциональных групп или кратных связей в веществе могут либо не проявить искомые свойства спирта, либо дать ложно положительный эффект на ту или иную реакцию.
Приведём примеры наиболее известных качественных реакций на спирты:
- Проба Лукаса: при реакции вторичного или третичного спирта при комнатной температуре (первичные спирты в реакцию, как правило, не вступают) с реактивом Лукаса (смесь концентрированной соляной кислоты и хлорида цинка) происходит образование галогенопроизводного, которое распознаётся по образованию характерного масла, образующего отдельную от исходного спирта фазу. При этом зафиксировав время реакции, можно различить вторичные (эффект наблюдается по истечение 5-ти минут) и третичные спирты (реакция протекает практически мгновенно или в течение не более 3-х минут)[94].
- Некоторые первичные спирты, например: аллиловый или бензиловый, дают положительную реакцию с реактивом Лукаса[94].
- Иодоформная проба: предназначена для идентификации спиртов вида R−CH(OH)−CH3 и кетонов вида R−C(O)−CH3[95].
- Идентификацию спиртов осуществляют по характерному жёлтому осадку иодоформа, обладающего специфическим запахом.
- Тест Виктора Мейера : позволяет дифференцировать первичные, вторичные и третичные спирты по реакции получаемых из них нитропроизводных с азотистой кислотой. На первой стадии спирты трансформируются в галогенопроизводные, которые, в свою очередь, превращаются в нитроалканы:
- Далее взаимодействие с HNO2 делает возможными три варианта развития событий[96]:

- раствор окрашивается в красный цвет (натриевая соль нитроловой кислоты — RC(NO2)=NONa)

- раствор окрашивается в синий цвет

- раствор остаётся бесцветным (реакция не идёт)
- Цератная проба: при взаимодействии спиртов с азотнокислым раствором гексанитратоцерата (IV) аммония, имеющим жёлтую окраску, образуются переходные комплексы красного цвета, которые затем обесцвечиваются вследствие окисления спирта и перехода Ce (IV) в анион Ce (III). Для спиртов, нерастворимых в воде, используют растворы в диоксане или ацетонитриле[97].
- Окислительная проба: при взаимодействии первичных или вторичных спиртов с реактивом Джонса (раствор оксида хрома (VI) в серной кислоте), имеющим оранжевую окраску, образуются продукты окисления (карбоновые кислоты или кетоны), а сам реактив меняет цвет на зелёный или голубой благодаря солям восстановленного хрома (III). Важной особенностью теста является время фиксации изменения окраски — 2 секунды, по истечении которого любые дальнейшие изменения в структуре или цвете раствора не принимаются во внимание[97].
- Сульфидная проба: вторичные спирты при нагревании с серой образуют сероводород, который идентифицируется по образованию чёрного осадка с ацетатом свинца[98]:
Реагенты для химической идентификации спиртов
Идентификацию конкретного спирта (наряду с другими методами) осуществляют по его производным, образующимся в результате его химического взаимодействия с различными реагентами: измеряя основные физические параметры получившегося производного (температура плавления, температура кипения и пр.) можно c различной степенью достоверности подтвердить формулу исходного соединения.
[T 12]Таблица 15. Перечень основных реагентов и образующихся производных при идентификации спиртов[99].
Реагент для идентификации Исследуемое производное спирта Примеры идентифицируемых спиртов фенилизоцианат, C6H5N=C=O C6H5NHCOOR этанол, аллиловый спирт, циклогексанол 1-нафтилизоцианат, C10H7N=C=O C10H7NHCOOR пропанол-2, 2,3-диметил-2-бутанол, мирициловый спирт 4-бифенилизоцианат, C6H5−C6H4N=C=O C6H5−C6H4NHCOOR 2,4-диметил-1-пентанол, 2-этил-1-пентанол 4-нитробензоил хлорид, O2NC6H4COCl O2NC6H4COOR пентанол-1, трихлорэтанол, циннамиловый спирт 3,5-динитробензоил хлорид, (O2N)2C6H4COCl O2NC6H3COOR пентанол-2, 2-хлорпропанол-1, бензиловый спирт фталевый ангидрид, C6H4(CO)2O C6H4(COOH)COOR гептанол, терпинеол 3-нитрофталевый ангидрид, O2NC6H3(CO)2O O2NC6H3(COOH)COOR 2-метоксиэтанол, гексанол, 2-фенилэтанол псевдосахарина хлорид, C6H4(SO2N=Cl) C6H4(SO2N=COR) метанол, бутанол, деканол циануровая кислота[К 9], (NHCO)3 H2NCONHCOOR 2-метил-2-пентанол, 5-нонанол Количественный анализ спиртов
Для количественного анализа спиртов, обычно, используют методы, основанные на реакции этерификации (реакция 1), реже — на определении активного водорода (реакция 2). Для гликолей также применим окислительно-восстановительный метод, где в качестве окислителя используется иодная кислота (реакция 3)[100].
Для этерификации чаще всего применяют уксусный и фталевый ангидриды, а также пиромеллитовый диангидрид. Содержание спирта определяется титрованием образующейся в результате реакции кислоты гидроксидом натрия[100]. В случае гликолей анализ проводят по реакции образующейся иодноватой кислоты (HIO3) с иодидом калия и последующим титрованием выделившегося иода тиосульфатом натрия:
Наконец, анализ на определении активного водорода сводится к анализу выделившегося в ходе реакции метана (метод Чугаева — Церевитинова).
Спектральные методы анализа спиртов
Масс-спектрометрические методы анализа спиртов
Масс-спектры алифатических спиртов имеют слабые M+ сигналы, а для высших и сильноразветвлённых соединений практически отсутствуют, поэтому для алканолов рассматривают характеристические распады с образованием оксониевых ионов или элиминирование с образованием алкенов[101].
Для первичных спиртов — m/z 31, для вторичных — m/z 45, 59, 73 …, для третичных — m/z 59, 73, 87 …[102]:[стр.333]
Характеристические пики, связанные с элиминированием воды и алкена: [M-46]+, [M-74]+, [M-102]+…[102]:[стр.333]
ИК-спектроскопические методы анализа спиртов
ИК-спектры спиртов характеризуются двумя типами интенсивных характеристических полос поглощения:
- полосы поглощения, связанные с валентными колебаниями O−H группы: 3650—3200 см−1;
- полосы поглощения, связанные с валентными колебаниями С−O−H группы: 1210—1000 см−1.
Также выделяют полосы поглощения средней интенсивности, как правило не имеющие определяющего значения: в диапазоне 1450—1250 см−1 (плоскостные деформационные колебания O−H группы) и 750—650 см−1 (внеплоскостные деформационные колебания O−H группы)[103]:[стр. 59].
[T 13]Таблица 16. Типичные полосы поглощения в инфракрасных спектрах спиртов[103]:[стр. 60].
Типы связей и колебания Диапазон, см−1 Описание полосы поглощения O−H, валентные колебания ROH, неассоциированные 3650—3580 Узкая полоса, наблюдаемая в разбавленных растворах или парах ROH•••HOR, димеры (водородная связь) 3550—3400 Широкая полоса, теряющая интенсивность при разбавлении ROH•••HOR•••, полимеры 3400—3200 Широкая полоса или ряд полос С−O, валентные колебания R3COH, третичные спирты 1210—1100 Полосы высокой интенсивности, уменьшающейся при разбавлении R2CHOH, вторичные спирты 1125—1000 RCH2OH, первичные спирты 1075—1000 O−H, деформационные колебания ROH 1450—1250
750—650Широкие полосы средней интенсивности, не имеющие практического значения При анализе ИК-спектров необходимо учитывать, что некоторые функциональные группы дают характеристические полосы в диапазонах, близких или совпадающих с диапазонами спиртов: валентные колебания O−H группы сходны с валентными колебаниями связей N-H, C-H алкинов и воды; валентные колебания связи C−O сходны с валентными колебаниями связей C−F, C−N, N−O, P−O, C=S, S=O, P=O, Si−O, Si-H[102]:[стр. 269—270].
ЯМР-спектроскопические методы анализа спиртов
ЯМР-спектроскопические методы для ядер 1H широко используются для анализа спиртов, однако на положение сигнала существенно влияет природа растворителя и другие внешние факторы, поэтому величины характеристических сдвигов протонов (δ, м. д. относительно тетраметилсилана) рассматривают либо для чистых веществ (если соединение не содержит несколько типов подвижных атомов H), либо для их растворов в диметилсульфоксиде (ДМСО) или трихлордейтерометане (CDCl3). Для алифатических и алициклических спиртов δ: 0,5—3,0 (в ДМСО: 4—6)[102]:[стр.208].
Химические сдвиги ядер 13С в спиртах (δ, м. д. относительно тетраметилсилана) составляют диапазон 50—100 (смещение примерно 50 м.д. по сравнению с сигналом C−H)[102]:[стр.60].
Также для изучения гидроксильных соединений применяют импульсную Фурье-спектроскопию на ядрах 17O. Значительная разница в сдвигах для первичных (этанол: δ=5,9 м. д.), вторичных (изопропанол: δ=39,8 м. д.) и третичных спиртов (трет-бутанол: δ=62,3 м д.) относительно воды H217O позволяет установить или подтвердить структуру исследуемого соединения[104].
Применение спиртов
Экономическое значение и направления использования спиртов
Области использования спиртов многочисленны и разнообразны, особенно учитывая широчайший спектр соединений, относящихся к этому классу. Вместе с тем, с промышленной точки зрения, только небольшой ряд спиртов вносит заметный вклад в глобальную мировую экономику.
В TOP 50 за 2002 год соединений[К 10], выпускаемых химической промышленностью США, из спиртов входят только метанол (14-е место) и этиленгликоль (29-е место)[90]:[стр. 17—18]. В следующие 50 важнейших химических соединений, по данным за 1999 год, включены изопропиловый спирт, н-бутиловый спирт, синтетический этанол, пропиленгликоль, диэтиленгликоль, 2-этилгексанол, 1,4-бутандиол, сорбитол и глицерин[90]:[стр. 217—219].
В мире наибольшее значение из алканолов имеют метиловый, этиловый, пропиловый, изопропиловый спирт, а также бутиловые, амиловые и высшие жирные спирты. Из циклических и ароматических спиртов: циклогексанол, 2-этилгексанол, фенилэтиловый и бензиловый спирты; из гликолей и полиолов: этиленгликоль, пропиленгликоль, диэтиленгликоль, глицерин, пентаэритрит[66].
Самым распространённым и используемым спиртом в мире является этанол. Его мировой объём потребления составляет около 65 млн тонн[К 11]. Совокупный мировой объём потребления прочих спиртов (кроме этанола) по различным направлениям использования составляет около 70 млн тонн (по состоянию на 2009 год)[К 12].
Наиболее крупнотоннажными направлениями использования спиртов являются (в произвольном порядке):
- промежуточные продукты для основного органического синтеза;
- применение в качестве топлива;
- производство растворителей;
- производство синтетических моющих средств, парфюмерии и косметики;
- использование в пищевой и фармацевтической промышленности.
[T 14]Таблица 17. Ключевые направления использования некоторых распространённых спиртов.
Спирт Преобладающее направление использования Прочие значимые направления использования Источники метиловый спирт 1. Синтез формальдегида. 2. Синтез простых эфиров — оксигенирующих компонентов бензина (2-метокси-2-метилбутан и 2-метокси-2-метилпропан).
3. Синтез уксусной кислоты и уксусного ангидрида.
4. Прямое использование в качестве топлива.[78] этиловый спирт 1. Прямое использование в качестве топлива. 2. В качестве растворителя.
3. Синтез органических соединений.[105] пропиловый спирт 1. В качестве растворителя. 2. Органический синтез. [106] изопропиловый спирт 1. В качестве растворителя. 2. Синтез ацетона и его производных.
3. Синтез изопропиловых эфиров.[107] н-бутиловый спирт 1. Синтез бутиловых эфиров, используемых в качестве растворителей и пластификаторов. 2. В качестве растворителя.
3. Прямое использование в качестве топлива.[108][109] высшие жирные спирты 1. Синтез пластификаторов, смазочных масел, присадок и синтетических моющих средств. — [110][111] циклогексанол 1. Полупродукт в синтезе нейлона. — [112] этиленгликоль 1. Производство полиэфирных волокон, смол и плёнок. 2. Производство антифризов. [113] пропиленгликоль 1. Производство ненасыщенных полиэфирных смол. 2. Производство антифризов для авиации и пищевой промышленности. [114] глицерин 1. В парфюмерно-косметической промышленности как компонент средств личного ухода и ухода за полостью рта. 2. Производство напитков и продуктов питания.
3. В фармацевтической промышленности.[115] Применение спиртов в основном органическом синтезе
[T 15] Таблица 18. Применение спиртов для производства продукции основного органического синтеза.
Спирт (исходный продукт) Конечный продукт Химическая реакция (схематично) Краткое описание процесса Источники метиловый спирт формальдегид 2CH3OH + O2 → 2HCHO + 2H2O Высокотемпературное (300—720 °С) каталитическое окисление метанола (частичное с дегидрированием или прямое) [К 13]. [116]:[стр 95-97] 2-метокси-2-метилпропан[К 14] CH3OH + (CH3)2C=CH2 → (CH3)3COCH3 Реакция протекает в жидкой фазе при 50—85 °С и давлении 0,7—1,5 МПа в присутствии катионообменных смол. [116]:[стр. 212] уксусная кислота CH3OH + CO → CH3COOH Жидкофазное карбонилирование при 220—250 °С и давлении 30 МПа в присутствии сложного родиевого катализатора и небольших количеств иодметана. [80]:[стр. 53] N-диметиланилин C6H5NH2 + 2CH3OH → C6H5N(CH3)2 + 2H2O Жидкофазное алкилирование анилина при 200 °С и давлении 3,7 МПа в присутствии каталитических количеств серной кислоты [89]:[стр. 1.3] метиламины CH3OH + NH3 → CH3NH2 + H2O
CH3OH + 2NH3 → (CH3)2NH + 2H2O
CH3OH + 3NH3 → (CH3)3N + 3H2OГазофазный аммонолиз метанола при высокой температуре и давлении [117] хлорметан CH3OH + HCl → CH3Cl + H2O Реакция протекает в газовой фазе при 200—350 °С в присутствии ZnCl2 на твёрдом носителе [118]:[стр. 132] этиловый спирт диэтиловый эфир 2C2H5OH → (C2H5)2O + H2O Дегидратация этанола при 250 °С над Al2O3 [118]:[стр. 188] хлораль C2H5OH + 4Cl2 → CCl3CHO + 5HCl Многостадийное жидкофазное хлорирование этанола [118]:[стр. 133] ацетальдегид 1. 2C2H5OH + O2 → 2CH3CHO + H2O
2. C2H5OH → CH3CHO + H21. Окисление воздухом в газовой фазе при 375—550 °С в присутствии серебряного или медного катализатора
2. Дегидрирование при 260—290 °С над активированным хром-медным катализатором[80]:[стр. 31] [80]:[стр. 33]
этилацетат C2H5OH + CH3COOH → CH3COOC2H5 + H2O Этерификация с уксусной кислотой в присутствии кислотного катализатора [89]:[стр. 2.212] изопропиловый спирт ацетон CH3CH(OH)CH3 → CH3C(O)CH3 + H2 Каталитическое жидкофазное (никель Ренея,150 °С) или газофазное (350—400 °С, 0,2 МПа) дегидрирование [80]:[стр 127-133] бутиловый спирт бутилакрилат C4H9OH + C2H2 + CO → CH2=CH−COOC4H9 Модифицированный высокотемпературный Реппе-процесс, протекающий в присутствии HCl и тетракарбонила никеля в качестве катализатора [90]:[стр. 234] Применение спиртов в качестве топлива
Использование спиртов в качестве топлива — тема значимая, обширная и экономически очень важная — более подробно изложена в указанных выше статьях, поэтому здесь ограничимся только общими вопросами. Говоря о практическом применении спиртов, отметим, что основным направлением является их использование в качестве моторного топлива (замена бензину и дизелю), однако существует и ряд вспомогательных направлений, например, использование метанола и этанола в топливных элементах для различных приборов (например: прямой метанольный топливный элемент).
Для топливных целей в настоящий момент используются в промышленных объёмах три спирта: метанол, этанол и бутанол, что связано, прежде всего, с их коммерческой доступностью и возможностью массового производства из растительного сырья (кроме метанола[К 15]). При этом возможно использование спиртов в виде горючего в чистом виде, в виде различных смесей с бензином или дизельным топливом[119], а также в качестве оксигенирующих добавок (до 10 %) с целью повышения октанового числа и снижения токсичности отработанных газов[К 16][120][121]. Также отдельным направлением является использование метанола для переэтерификации жиров в производстве биодизеля[122].
Преобладающим топливным спиртом является этанол. По оценкам экспертов, на 2009 год 80—90 % всего производимого в мире этилового спирта было использовано в этих целях и составило 73,9 млрд литров (≈ 58 млн тонн)[105][123].
Основные причины, послужившие активному изучению спиртов в качестве альтернативного горючего, это[124]:
- рост цен на нефть и газ, а также исчерпаемость этих ресурсов в ближайшем будущем;
- спирты обладают высокими эксплуатационными характеристиками, а продукты сгорания содержат меньше вредных веществ;
- спирты могут изготавливаться биохимическим методом из отходов пищевой, деревообрабатывающей и целлюлозно-бумажной промышленности, тем самым попутно решая проблему утилизации.
Вместе с тем, массовое использование вышеуказанных спиртов в качестве моторного топлива, помимо чисто экономических причин, имеет ряд недостатков[125]:
- метанол и этанол обладают по сравнению с бензином меньшей энергоэффективностью и, соответственно, обеспечивают больший расход;
- низкие температуры кипения спиртов могут служить причиной образования паровых пробок, что может существенно усложнить работу двигателя;
- гигроскопичность спиртов, а также их растворимость в воде может привести к резкому снижению мощности при попадании влаги в топливную систему;
- спирты обладают существенно более высокими коррозионными характеристиками по сравнению с углеводородами;
- относительно высокая скрытая теплота сгорания метанола и этанола может служить причиной проблемы при смешении этих спиртов с воздухом и дальнейшей транспортировки через впускной коллектор двигателя.
Промышленное применение спиртов
Растворители
Среди растворителей широкое распространение имеют самые разные классы спиртов: одноатомные (например: метанол, изопропанол) и многоатомные (этиленгликоль, глицерин); алифатические (этанол, бутанол) и циклические (циклогексанол, бензиловый спирт). Спирты относятся к полярным растворителям и применяются в самых различных отраслях промышленности[126].
Самым распространённым спиртом среди растворителей является этанол — его мировой объём потребления (по данным на 2009 год) в этом качестве превышает 3,5 млн тонн в год[127]. Другими популярными растворителями являются метанол[78] и изопропанол[84] с объёмами потребления более 1 млн тонн в год.
Использование спиртов в качестве растворителей включает в себя следующие направления[128]:
- Технологический растворитель:
- экстракция и очистка натуральных продуктов, таких как жиры и масла, смолы, воск, природные красители и ароматизаторы, альгинаты, витамины, алкалоиды, водоросли;
- носитель в пищевой промышленности;
- очистка, кристаллизация и осаждение органических химических веществ.
- Растворитель в производстве красок и покрытий:
- растворитель для синтетических полимерных материалов (лаки, смолы, клея и т. п.);
- компонент цементов, грунтовок, красок и чернил.
- Очиститель:
- промышленный очиститель в производстве электронных компонентов, металлических поверхностей, фотоплёнок и фотобумаг; стеклоочиститель и пр.;
- компонент жидкого мыла и моющих средств.
- Растворитель в производстве потребительской продукции:
- в производстве фармацевтической продукции: настоек, экстрактов и пр.;
- в парфюмерии и косметике: компонент жидких средств ухода за телом, волосами, кожей, ногтями, парфюмерных композиций, дезодорантов и пр.
- Аэрозольный растворитель:
- самые различные бытовые аэрозоли: очистители, воски, полироли, краски, размораживатели, репелленты от насекомых, освежители и очистители воздуха, лаки для волос;
- аэрозоли, используемые в медицине и ветеринарии: антисептики, фунгициды и инсектициды, спреи для обезболивания и оказания первой помощи, ветеринарные спреи и пр.
Перечень некоторых отраслей промышленности и спиртов, используемых в этих отраслях в качестве растворителей, приведены в таблице 19.
[T 16] Таблица 19. Применение спиртов в качестве растворителей в отдельных отраслях промышленности[129].Отрасль Примеры используемых спиртов Направления использования авиационно-космическая промышленность метанол, бутан-1-ол, этиленгликоль нанесение покрытий на металлические поверхности автомобильная промышленность метанол, пропан-2-ол, бутан-1-ол, бутан-2-ол, 2-метилпропан-2-ол очистка и подготовка поверхностей лакокрасочная промышленность этанол, изопропанол основа для чернил, жидких красителей и лаков, для введения в композиции полимерных компонентов; очиститель металлургия метанол, бутан-1-ол вспомогательное (использование в узкоспецифических областях) микробиологическая промышленность метанол, этанол, пропан-1-ол, этиленгликоль, глицерин приготовление субстратов, экстракция целевых компонентов нефтеперерабатывающая промышленность метанол, этиленгликоль очиститель парфюмерно-косметическая промышленность этанол, изопропанол, бутан-1,3-диол основа парфюмерных композиций (около 70 %), гомогенизация компонентов пищевая промышленность этанол, изопропанол носитель; экстракция и очистка масел и жиров полиграфия метанол, этанол, изопропанол, бутан-1-ол основа для красок, очиститель производство металлоизделий метанол, бутан-1-ол, бутан-2-ол, 2-этоксиэтанол, 2-метоксиэтанол, этиленгликоль, очистка и подготовка поверхностей производство полимеров и искусственных волокон метанол, аллиловый спирт, бутан-1-ол, бутан-2-ол, 2-метилпропан-2-ол, этиленгликоль жидкая основа для полимерных материалов, очиститель промышленность строительных материалов метанол, пропан-2-ол, бутан-1-ол, бутан-2-ол, 2-метилпропан-2-ол, этиленгликоль компонент цементов, бетонов, строительных смесей текстильная промышленность метанол, этиленгликоль очистка и обработка поверхностей, расшлихтовка фармацевтическая промышленность этанол приготовление лекарственных форм химическая промышленность (неорганический синтез) этиленгликоль вспомогательное (использование в узкоспецифических областях) химическая промышленность (органический синтез) метанол, этанол, пропан-2-ол, бутан-1-ол, бутан-2-ол, 2-метилпропан-2-ол, аллиловый спирт, этиленгликоль реакционная среда; очистка, экстракция и осаждение веществ целлюлозно-бумажная промышленность метанол, бутан-1-ол, этиленгликоль очистка и экстракция компонентов, носитель электронная промышленность этанол, изопропанол, пропан-1-ол очистка и обезжиривание электронных компонентов Поверхностно-активные и моющие вещества
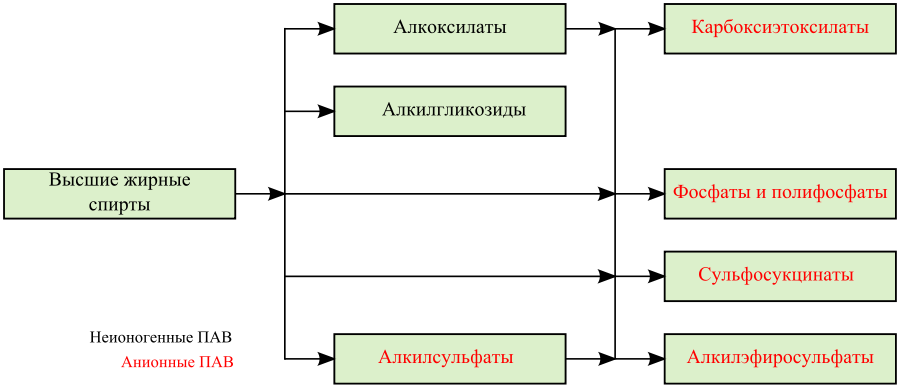
Важнейшим сырьём в производстве современных поверхностно-активных веществ для синтетических моющих средств являются высшие жирные спирты, которые в зависимости от реагента дают неионогенные или анионные ПАВ, что иллюстрирует приведённая ниже схема[130]:[стр. 5].
Мировой объём использования высших жирных спиртов в производстве ПАВ в 2000 году составил 1,68 млн тонн[130]:[стр. 6]. В 2003 году около 2,5 млн тонн ПАВ было произведено на основе высших жирных спиртов[131].
[T 17] Таблица 20. Применение высших жирных спиртов для производства поверхностно-активных веществ.
Класс ПАВ Вид ПАВ Химическая формула Реагент для синтеза Схема синтеза Источники Неионогенные ПАВ Алкоксилаты этоксилаты R−O−(CH2CH2O)nH окись этилена [К 17]ROH + n(CH2CH2)O → RO−(CH2CH2O)nH
Реакция протекает в присутствии щелочи при температуре до 160°С и давлении до 0,55МПа. Обычно используют C9—C15 спирты в сочетании с 6—7 молями окиси этилена.
[85]:[стр. 31, 35][130]:[стр. 137—139] пропоксилаты R−O−(CH2CH(CH3)O)nH окись пропилена бутоксилаты R−O−(CH2CH(C2H5)O)nH окись бутилена Алкилгликозиды R−(O−C6H10O5)nH глюкоза ROH + nC6C12O6 → R−(O−C6H10O5)nH+nH2O
Реакция протекает в присутствии сульфокислот при температуре до 140°С. Другой вариант — предварительное получение бутиловых эфиров с последующей переэтерификацией. Число гликозидных групп колеблется от 1 до 3.[85]:[стр. 38]
[130]:[стр. 149]Анионные ПАВ Карбоксиэтоксилаты R−O−(CH2CH2O)nСH2COOH хлоруксусная кислота RO(CH2CH2O)nH + ClCH2COOH → RO(CH2CH2O)nСH2COOH + HCl
Реакция протекает в присутствии щёлочи, кислота выделяется подкислением водного раствора и отделением водно-солевой фазы.
[85]:[стр. 40]
[130]:[стр. 126—127]Фосфаты и полифосфаты ROP(OH)2O; (RO)2P(OH)O оксид фосфора(V) 3ROH + P2O5 → ROP(OH)2O +(RO)2P(OH)O
Добавление порошкообразного оксида фосфора к безводным спиртам в безводной среде при 50—70 °С и интенсивном перемешивании[К 18].
[85]:[стр. 54]
[130]:[стр. 122—123]Сульфосукцинаты ROC(O)CH2CH(SO3Na)COOH; ROC(O)CH2CH(SO3Na)COOR малеиновый ангидрид, сульфит натрия ROH + (COCH=CHCO)O → ROC(O)CH=CHCOOH
ROC(O)CH=CHCOOH + Na2SO3 → ROC(O)CH2CH(SO3Na)COONa
Этерификация спиртов малиновым ангидридом (T до 100 °С) и дальнейшее присоединение к эфиру сульфита натрия пр нагревании.[85]:[стр. 52—53]
[132]Алкилсульфаты R−O−SO3H[К 19] серная кислота, оксид серы(VI), хлорсульфоновая кислота ROH + SO3 → ROSO3H
Прямое сульфирование спиртов при последующей нейтрализации раствора щелочью.[85]:[стр. 55—56]
[132]Алкилэфиросульфаты R−(CH2CH2O)nOSO3H Также в производстве ПАВ используются и некоторые другие спирты: глицерин (сложные эфиры с жирными кислотами — эмульгаторы), сорбитол (сорбитаны), моноэтаноламин и диэтаноламин (алканоламиды).
Полимерные материалы и их компоненты
Спирты имеют важное применение в качестве исходных компонентов для синтеза методом поликонденсации полимерных материалов, в основном, полиэфиров и полиуретанов:
- полиэтилентерефталат — поликонденсация этиленгликоля с терефталевой кислотой или её диметиловым эфиром;
- полибутилентерефталат — поликонденсация бутиленгликоля с терефталевой кислотой или её диметиловым эфиром;
- поли(дигидроксиметил)циклогексилтерефталат — поликонденсация 1,4-дигидроксиметилциклогексана с терефталевой кислотой или её диметиловым эфиром;
- полиуретаны — поликонденсация изоцианатов с гликолями или полиолами[133].
Спирты также используются для производства пластификаторов для полимеров:
- сложноэфирные пластификаторы — метанол, этанол, бутан-1-ол, 2-этилгексан-1-ол, 2,4-диэтилоктан-1-ол и ряд других, преимущественно первичных спиртов;
- диэфирные пластификаторы — этиленгликоль, диэтиленгликоль, пропан-1,2-диол и ряд других диолов[134].
Гидравлические жидкости и смазочные материалы
Для получения негорючих гидравлических жидкостей применяют водные растворы, содержащие глицерин и этанол. В производстве тормозных жидкостей широко используют этиленгликоль и эфиры на его основе[135].
В производстве ряда синтетических масел, используемых в качестве гидравлических жидкостей, применяются гликоли и некоторые первичные спирты:
- полиалкиленгликоли — продукты конденсации между гликолями и окисями алкенов;
- сложные эфиры дикарбоновых кислот (фталаты, адипинаты), например: бис(2-этилгексил)фталат[136].
Многие современные смазочные материалы имеют в своём составе высшие жирные спирты и их эфиры благодаря низкой токсичности, высокой температуре вспышки и бесследному испарению при нагревании. Эти свойства используются для бытового применения, а также для случаев, когда эффект охлаждения поверхности более важен, чем антифрикционные свойства (например, при сверлении, пилении или другой слесарной обработке металлов)[137].
Пестициды
 Дикопол — препарат для борьбы с клещами — ароматический спирт, аналог ДДТ
Дикопол — препарат для борьбы с клещами — ароматический спирт, аналог ДДТ
Несмотря на то, что незамещённые предельные алифатические спирты обладают фунгицидной или гербицидной активностью, их прямое использование в качестве пестицидов не находит широкого практического применения. Одним из немногих направлений является их использование в качестве регулятора роста растений. Подобными свойствами обладают этанол, этиленгликоль и другие гликоли, некоторые высшие жирные спирты[138]:[стр. 106—110].
Галогензамещённые спирты проявляют значительно большую активность: здесь можно встретить промышленные ратициды, гербицииды и фунгициды. Так, например, препарат глифтор, представляющий смесь 1,3-дифторпропан-2-ола и 1-фтор-3-хлорпропан-2-ола, используется для борьбы с мышевидными грызунами и сусликами[138].
Более высокая биологическая активность наблюдается у непредельных и ароматических спиртов. Аллиловый спирт находит применение в качестве гербицида, многие высшие непредельные спирты являются феромонами насекомых. Активными акарицидами являются некоторые ароматические бифениловые спирты: дикофол, хлорфенетол, проклонол[138][139].
Многие спирты являются полупродуктами для синтеза различных пестицидов[140]. Например, в производстве глифосата используется метанол[140]:[стр. 277], кротоксифоса — α-метилбензиловый спирт[140]:[стр. 294], пиретроидов третьего поколения — 3-феноксибензиловый спирт[138]:[стр. 181—182].
Также спирты широко используются в качестве неводного носителя для создания товарных композиций пестицидов. В их число входят метанол, этанол, изопропанол, пропиленгликоль, гексиленгликоль, диэтаноламин, диацетоновый спирт, тетрагидрофурфуриловый спирт[141].
Биологически активные вещества и лекарственные препараты
Как уже отмечалось в предыдущих разделах, спирты широко используются как полупродукты в органическом синтезе самых разнообразных соединений. Не является исключением и направление, связанное с получением биологически активных веществ. В данном разделе мы приведём некоторые примеры использования спиртов в рассматриваемом качестве.
В производстве витамина С в качестве промежуточного продукта используется сорбит[142]:[стр. 244], витаминов D — холестерин[142]:[стр. 304], витамина E — фитол[142]:[стр. 317].
Многие спирты используются в фармацевтическом производстве[143]:
- бензиловый спирт — карбенициллин;
- бутан-1,4-диол — бусульфан;
- бутиловый спирт — беноксинат, буметанид;
- изоамиловый спирт — амиксетрин, амопроксан;
- изопропиловый спирт — апраклодинин;
- метиловый спирт — апраклодинин, азастен, дезерпидин;
- пентан-1,5-диол — тракриум, цисатракурия безилат;
- тиодигликоль — ауранофин;
- этиленгликоль — алпростадил, цефпрозил;
- этиловый спирт — беноксинат, буфексамак, дицикломин, клофибрат.
Применение спиртов в производстве потребительской продукции
Пищевая промышленность
- Смотри также статью: Алкогольные напитки
В пищевой промышленности широкое применение спиртов общеизвестно: основой всех алкогольных напитков является этанол, который получается при сбраживании пищевого сырья — винограда, картофеля, пшеницы и прочих крахмало- или сахаросодержащих продуктов.
Кроме того, этиловый спирт используется в качестве компонента (растворителя) некоторых пищевых и ароматических эссенций (ароматизаторов), широко используемых в кулинарии, при выпечке кондитерских изделий, производстве шоколада, конфет, напитков, мороженного, варений, желе, джемов, конфитюров и пр.
Однако, этиловым, список спиртов, используемых в индустрии продуктов питания, не ограничивается. Спирты можно встретить среди самых разных пищевых добавок[144]:
- глицерин (E422) — влагоудерживающий агент, растворитель, загуститель, разделитель[К 20], плёнкообразователь[К 21], средство для капсулирования;
- зеаксантин[К 22] — краситель;
- ксилит (E967) — сахарозаменитель;
- лютеин (E161b) — краситель;
- маннит (E421) — сахарозаменитель, наполнитель, носитель, антислеживатель, разделитель;
- ментол — ароматизатор;
- поливиниловый спирт — плёнкообразователь;
- полиэтиленгликоль — пеногаситель, носитель-растворитель;
- пропиленгликоль (E1520) — влагоудерживающий агент, растворитель, стабилизатор, хладагент;
- сорбит (E420) — наполнитель, носитель, сахарозаменитель, влагоудерживающий агент, средство для капсулирования;
- эритрит — подсластитель.
Парфюмерия, косметика и бытовая химия
Спирты довольно широко используются в качестве душистых веществ для составления композиций в парфюмерно-косметической промышленности и производстве отдушек для бытовой химии и прочей потребительской продукции. Перечень некоторых спиртов, производимых в промышленных объёмах, с характеристиками их запахов представлены в таблице 21.
[T 18] Таблица 21. Применение спиртов в качестве душистых веществ для парфюмерии и бытовой химии[145][146].Спирт Характеристика запаха Применение октан-1-ол сильный, жирно-цитрусовый парфюмерные композиции и отдушки, пищевые ароматизаторы нонан-1-ол сильный, жирно-цветочный, ноты розы и апельсина парфюмерные композиции и отдушки деканол-1 жирный, воска с нотами розы, цветов апельсина парфюмерные композиции и отдушки, пищевые ароматизаторы ундекан-1-ол слабый цитрусовый с жирно-восковой нотой парфюмерные композиции и отдушки, пищевые ароматизаторы додекан-1-ол слабый жирный с цветочно-цитрусовыми нотами парфюмерные композиции и отдушки, пищевые ароматизаторы нонан-3-ол кокосовый орех с цветочным, абрикосовым оттенком парфюмерные композиции и отдушки 6-метил-5-гептен-2-ол зелень с цитрусовым оттенком и нотой кориандра парфюмерные композиции и отдушки 2,6-диметилгептан-2-ол свежий, цветочный парфюмерные композиции и отдушки 2,4-диметилгептан-1-ол листва, трава, дерево, оттенки розы парфюмерные композиции и отдушки 2-метилоктан-2-ол мягкий, цветов и зелени с пряным и маслянистым оттенками парфюмерные композиции и отдушки цис-3-гексен-1-ол интенсивный запах листьев и свежей травы парфюмерные композиции и пищевые ароматизаторы; в синтезе эфиров транс-2-гексен-1-ол сильный, зелень и фрукты пищевые ароматизаторы, реже — парфюмерные композиции 9-децен-1-ол воски розы с альдегидным оттенком парфюмерные композиции и отдушки 2,2,5,9-тетраметил-4,8-декадиен-1-ол цветочно-древесный с оттенком зелени парфюмерные композиции гераниол розы парфюмерные композиции и отдушки для мыла, косметические и моющие средства; в синтезе многих других душистых веществ нерол свежий, нежной розы парфюмерные композиции и отдушки для мыла, косметические и моющие средства; в синтезе сложных эфиров линалоол сильный цветочный с древесным оттенком парфюмерные композиции и отдушки для мыла; в синтезе других душистых веществ и витамина E цитронеллол свежий цветочный парфюмерные композиции и пищевые ароматизаторы; в синтезе других душистых веществ мирценол свежий цветочный с оттенком лайма парфюмерные композиции и отдушки для мыла, одеколоны дигидромирценол свежий цветочно-цитрусовый с оттенком лаванды парфюмерные композиции и отдушки фарнезол нежный ландыш парфюмерные композиции, фиксатор запаха; в синтезе других душистых веществ терпинеол оттенки сосны, сирени, лайма парфюмерные композиции и отдушки для мыла и моющих средств, пищевые ароматизаторы; в синтезе других душистых веществ ментол мятный пищевые ароматизаторы, отдушки для зубных паст и парфюмерных изделий санталол богатый, сандалового дерева дорогие парфюмерные композиции 2-циклогексилэтанол цветочно-травянистый, с оттенками розы, сирени, зелени парфюмерные композиции и отдушки бензиловый спирт слабый, приятный, с миндальным оттенком парфюмерные композиции и отдушки; в синтезе других душистых веществ 2-фенилэтанол розы парфюмерные композиции и отдушки, пищевые ароматизаторы, искусственное розовое масло; в синтезе других душистых веществ 2-фенилпропанол цветочный, жимолости, оттенки корицы, гиацинта парфюмерные композиции и отдушки 3-фенилпропанол мягкий, цветочно-бальзамический, оттенок гиацинта парфюмерные композиции и отдушки для мыла, моющие средства и бытовая химия Помимо ароматических, а также важнейших функций растворителя (см. раздел Растворители), в парфюмерно-косметической продукции спирты используются и с другими целями, например[147]:
- антивспениватели: этанол, изопропанол, пропанол, гексанол;
- антикоррозийные вещества: 2-диметиламино-2-метилпропан-1-ол;
- антимикробные препараты: 2,4-дихлорбензиловый спирт, (этилендиокси)диметанол;
- антиоксиданты: тиодигликоль;
- антистатики: высшие жирные спирты (С12—С16);
- гидротропные вещества: гексанол;
- маскирующие средства: бутан-2,3-диол, 2-бензилгептан-1-ол, борнеол, 3,7-диметил-1,6-нонадиен-3-ол;
- консерванты: 2-бром-2-нитропропан-1,3-диол, бензиловый спирт, 1,1,1-трихлор-2-метилбутан-2-ол;
- охлаждающие агенты: ментол, 3-(метокси)пропан-1,2-диол;
- пластификаторы: октан-1,8-диол, 2,2-диметилпропан-1,3-диол;
- противосеборейные средства: ундекан-1-ол;
- связующие: докозан-1-ол, высшие жирные спирты (С20—С22);
- смягчители: высшие жирные спирты (С9—С16); высшие гликоли (С15—С30);
- средства для завивки или распрямления волос: 1,4-меркаптобутан-2,3-диол, 3-меркаптопропан-1,2-диол;
- стабилизаторы эмульсий: 7-дегидрохолестериол, 3-(октадецилокси)-пропан-1,2-диол, высшие жирные спирты (С9—С50);
- стабилизаторы пены: декан-1-ол, миристиловый спирт, цетиловый спирт, стеариловый спирт;
- увлажнители: гексан-1,2,6-триол, бутан-1,2-диол, бутан-2,3-диол, 2-бутилоктан-1-ол, глицерин;
- фиксаторы волос: 2-(2-аминоэтокси)этанол;
- эмульгаторы: высшие жирные спирты (С40—С60).
Медицина
Основным спиртом, применяющимся в медицинских целях, является этанол. Его используют в качестве наружного антисептического и раздражающего средства для приготовления компрессов и обтираний. Ещё более широко применяется этиловый спирт для приготовления различных настоек, разведений, экстрактов и прочих лекарственных форм[148]:[стр. 382]. Применение спиртов в качестве собственно лекарственных средств не столь заметно, однако в перечне 10 наиболее важных рецептурных препаратов США в 2000 году 6-ю строчку занимает альбутерол, который можно отнести к рассматриваемому классу[90]:[стр. 421].
Среди прочих лекарств[149][148]:
- сердечно-сосудистые препараты: кленбутерол, пропранолол, тербуталин, фетанол, эпинефрин, эфедрин;
- средства, действующие на ЦНС: хлоралгидрат;
- противокашлевые препараты: ледин;
- средства для местного стимулирующего действия: ментол, хлорбутанол;
- отхаркивающие препараты: терпингидрат;
- диуретики: маннит;
- желчегонные средства: фенипентол;
- гепатопротекторы: флумецинол;
- гормональные препараты: даназол, дигидротахистерол, преднизолон, эстрадиол, эстриол;
- витамины: ретинол, холекальциферол, эргокальциферол.
Прочие направления использования
В настоящее время трудно найти область практической деятельности человека, где бы ни использовались спирты в той или иной роли. Отметим некоторые вспомогательные направления применения спиртов, отдавая себе отчёт, что данный список не будет исчерпывающим:
- ингибиторы коррозии металлов[150];
- пенообразователи для флотореагентов[151];
- компоненты автокосметики[152];
- исходные продукты для получения взрывчатых веществ, а также их компоненты.
- Глицерин применяется для синтеза нитроглицерина, этиленгликоль — этиленгликольдинитрата, пентаэритрит — пентаэритриттетранитрата[153].
- исходные продукты для получения отравляющих веществ, а также компоненты для их дегазации.
- Низшие спирты применяется для синтеза фосфорорганических боевых отравляющих веществ, например: табуна (этанол) или диизопропилфторфосфата (изопропанол)[154]. Моноэтаноламин и метилцеллозольв используются для дегазации[155].
Перечень используемых в статье таблиц
- ↑ Систематические и тривиальные названия некоторых спиртов.
- ↑ Зависимость температуры кипения некоторых монозамещённых метана от молекулярной массы.
- ↑ Энергия связей в метаноле.
- ↑ Сравнение температур кипения и плотностей некоторых высших алканов и соответствующих алканолов.
- ↑ Значения констант кислотности и энергии диссоциации некоторых гидроксильных соединений.
- ↑ Значения констант основности некоторых спиртов и воды.
- ↑ Некоторые физические константы для алифатических предельных спиртов.
- ↑ Некоторые физические константы для ряда алициклических, ароматических и непредельных спиртов.
- ↑ Основные современные процессы, используемые для промышленного получения спиртов.
- ↑ Основные химические промышленные способы получения экономически наиболее важных спиртов.
- ↑ Получение спиртов биохимическими методами.
- ↑ Перечень основных реагентов и образующихся производных при идентификации спиртов.
- ↑ Типичные полосы поглощения в инфракрасных спектрах спиртов.
- ↑ Ключевые направления использования некоторых распространённых спиртов.
- ↑ Применение спиртов для производства продукции основного органического синтеза.
- ↑ Применение спиртов в качестве растворителей в отдельных отраслях промышленности.
- ↑ Применение высших жирных спиртов для производства поверхностно-активных веществ.
- ↑ Применение спиртов в качестве душистых веществ для парфюмерии и бытовой химии.
Комментарии
- ↑ Среднее значение по данным двух источников.
- ↑ В диметилсульфоксиде.
- ↑ Показатель измерен при 22°C.
- ↑ Показатель измерен при 40°C.
- ↑ 1 2 3 4 По данным за 2008 год.
- ↑ По данным за 2003 год. Речь идёт исключительно об этаноле, получаемом химическим путём. Объём производства биоэтанола почти в 10 раз больше. Подробнее см. в разделе Применение спиртов в качестве топлива.
- ↑ По данным за 2009 год.
- ↑ Установленная производственная мощность по данным на 2003 год.
- ↑ В реакцию со спиртом вступает неустойчивая изоциановая кислота HNCO, образующаяся при термическом разложении циануровой кислоты.
- ↑ Первые три места в списке занимают серная кислота, азот и кислород соответственно. В список не входят соединения, получаемые биохимическими методами, например — этанол, получаемый из растительного сырья.
- ↑ По данным на 2009 год. Рассчитано исходя из данных потребления топливного этанола (биоэтанола) и примерных объёмов производства синтетического этанола.
- ↑ Значение рассчитано исходя из данных по объёмам мирового промышленного производства наиболее распространённых спиртов в промышленности (см. раздел Получение наиболее важных спиртов в промышленности).
- ↑ Существуют два основных технологических метода получения формальдегида из метанола:
- окисление с частичным дегидрированием (катализатор: серебро; температура: 400—720 °С):
CH3OH → HCHO + H2
2H2+ O2 → 2H2O - прямое окисление (катализатор: оксидный железо-молибденовый; температура: 300—400 °С):
2CH3OH + O2 → 2HCHO + 2H2O
- окисление с частичным дегидрированием (катализатор: серебро; температура: 400—720 °С):
- ↑ Аналогично, чуть в более жёстких условиях получают и 2-метокси-2-метилбутан.
- ↑ Так называемый биометанол, как и обычный метанол, производятся из синтез-газа, который в с свою очередь продуцируется из метана. При этом, при получении биометанола используется так называемый биометан, образующийся из биологических отходов в процессе жизнедеятельности специальных бактерий. Для топливных нужд может быть использован метанол любой технологии производства.
- ↑ В качестве оксигенирующих добавок помимо метанола, этанола и бутанола, могут использоваться изопропанол, пропанол, изобутанол и другие алифатические спирты.
- ↑ Приведена схема для окиси этилена, как наиболее распространённому реагенту для синтеза алкоксилатов.
- ↑ Вместо оксида фосфора также используются полифосфорные кислоты, а в качестве исходных продуктов — этоксилаты спиртов.
- ↑ Обычно используют не сами сульфаты, а аммониевые или натриевые соли, например: лаурилсульфат натрия.
- ↑ Разделители — вещества, облегчающие выемку продуктов из форм, противней или иных жарочных или формующих поверхностей, а также, препятствующих плотному контакту или слипанию частей продукта друг с другом.
- ↑ Плёнкообразователи — вещества, наносящиеся на поверхность пищевых продуктов с защитной целью.
- ↑ Разрешение на применение в России отсутствует.
Примечания
- ↑ Alcohols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). doi:10.1351/goldbook.A00204. Архивировано из первоисточника 21 августа 2011. Проверено 2 сентября 2010.
- ↑ Enols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the «Gold Book»). doi:10.1351/goldbook.E02124. Архивировано из первоисточника 21 августа 2011. Проверено 2 сентября 2010.
- ↑ Phenols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the «Gold Book»). doi:10.1351/goldbook.P04539. Архивировано из первоисточника 21 августа 2011. Проверено 2 сентября 2010.
- ↑ Myers R. L. The 100 Most Important Chemical Compounds: A Reference Guide. — Westport: Greenwood Press, 2007. — 327 p. — ISBN 0-313-33758-6
- ↑ 1 2 Фросин В. Н. Спирты. Большая советская энциклопедия. Яндекс.Словари. Проверено 24 августа 2009.
- ↑ IUPAC Nomenclature of Organic Chemistry (англ.). ACD/Labs. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ Леенсон И. А. Откуда твоё имя?. Журнал «Химия и жизнь - XXI век». Всякая всячина. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ Алкоголь. Этимологический словарь Фасмера. Тезуарус. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ Толковый словарь Даля
- ↑ Спирт. Этимологический словарь Фасмера. Тезуарус. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ 1 2 История алкоголя. Gliant.com. Спиртные напитки.(недоступная ссылка — история) Проверено 25 августа 2009.
- ↑ Mousdale D. M. Biofuels: Biotechnology, Chemistry, and Sustainable Development. — Boca Raton: CRC Press, Taylor & Francis Group, 2008. — P. 1—2. — ISBN 978-1-4200-5124-7
- ↑ 1 2 Этиловый спирт // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1999. — Т. 5. — С. 994—997. — ISBN 5-85270-310-9
- ↑ Похлёбкин В.В. Терминология русских спиртных напитков в XIV – XV веках. История водки. vkus.narod.ru. Архивировано из первоисточника 21 августа 2011. Проверено 25 августа 2009.
- ↑ 1 2 3 Соловьев Ю. И. История химии: Развитие химии с древнейших времен до конца XIX в. Пособие для учителей. — 2-е изд., перераб. — М.: «Просвещение», 1983. — С. 32, 174-175, 240.
- ↑ 1 2 3 Фигуровский Н. А. История химии: Учеб. пособие для студентов пед. ин-тов по хим. и биол. спец. — М.: «Просвещение», 1979. — С. 132, 145, 176.
- ↑ Метиловый спирт // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ 1 2 Метиловый спирт // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1992. — Т. 3. — С. 118-119. — ISBN 5-85270-039-8
- ↑ Андреас Ф., Грабе К. Химия и технология попилена = Propylenchemie / Под редакцией Полякова З.Н.. — Л.: «Химия», 1973. — С. 53.
- ↑ Рахманкулов Д. Л., Кимсанов Б. X., Чанышев Р. Р. Физические и химические свойства глицерина. — М.: «Химия», 2003. — С. 8. — ISBN 5-7245-1228-9
- ↑ Васильев А. А., Черкаев Г. В., Никитина М. А. Новый подход к душистым веществам с запахом зелени (pdf). Англо-русскоязычный общественный химический журнал «Бутлеровские сообщения». Архивировано из первоисточника 21 августа 2011. Проверено 11 сентября 2009.
- ↑ b-Фенилэтиловый спирт. Большая советская энциклопедия. Яндекс.Словари. Проверено 25 августа 2009.
- ↑ Борнеокамфорное дерево (Dryobalanops aromatica Coleb.). Получение, состав, свойства и применение эфирных масел. Viness.narod.ru. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ Ментол // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1992. — Т. 3. — С. 59. — ISBN 5-85270-039-8
- ↑ Гераниол // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 1024.
- ↑ Линалоол // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1990. — Т. 2. — С. 1180. — ISBN 5-85270-035-5
- ↑ Цитронеллол // Химическая энциклопедия / Главный редактор H.C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1999. — Т. 5. — С. 774. — ISBN 5-85270-310-9
- ↑ Фарнезол // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1999. — Т. 5. — С. 112. — ISBN 5-85270-310-9
- ↑ Терпинеолы // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1995. — Т. 4. — С. 1093. — ISBN 5-85270-092-4
- ↑ α-Бисаболол. Получение, состав, свойства и применение эфирных масел. Viness.narod.ru. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ Санталол // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1995. — Т. 4. — С. 576. — ISBN 5-85270-092-4
- ↑ α-Фенхиловый спирт. Получение, состав, свойства и применение эфирных масел. Viness.narod.ru. Архивировано из первоисточника 21 августа 2011. Проверено 24 августа 2009.
- ↑ 1 2 3 4 5 Племенков В. В. Химия изопреноидов. Глава 5. Монотерпены // Химия растительного сырья. — 2006. — № 2. — С. 63-87.
- ↑ Серебряков Э. П. Холестерин. Большая советская энциклопедия. Яндекс.Словари. Проверено 25 августа 2009.
- ↑ Эргостерин. Медицинская энциклопедия. Словари и энциклопедии на Академике. Архивировано из первоисточника 21 августа 2011. Проверено 25 августа 2009.
- ↑ Желчные спирты // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1990. — Т. 2. — С. 280. — ISBN 5-85270-035-5
- ↑ Левицкий М. Спирты. Энциклопедия «Кругосвет». Яндекс.Словари. Архивировано из первоисточника 21 августа 2011. Проверено 25 августа 2009.
- ↑ Маннит. Словарь по естественным наукам. Глоссарий.ру. Яндекс.Словари.(недоступная ссылка — история) Проверено 25 августа 2009.
- ↑ Ретинол. Большая советская энциклопедия. Яндекс.Словари. Проверено 27 августа 2009.
- ↑ Инозит. Большая советская энциклопедия. Яндекс.Словари. Проверено 27 августа 2009.
- ↑ Кальциферолы. Большая советская энциклопедия. Яндекс.Словари. Проверено 29 августа 2009.
- ↑ 1 2 Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека: В 2-х томах = Harper's Biochemistry / Перевод с англ. — М.: «Мир», 1993. — Т. 1. — С. 159-160. — ISBN 5-03-001774-7
- ↑ 1 2 Бриттон Г. Биохимия природных пигментов = The Biochemistry of Narural Pigments / Под ред. профессора Запрометова М. Н.. — М.: «Мир», 1986. — С. 52-60.
- ↑ 1 2 3 Лебедева К. В., Миняйло В. А., Пятнова Ю. Б. Феромоны насекомых. — М.: «Наука», 1984. — С. 6-7, 79-82.
- ↑ Arn H., Schwarz C., Limacher H., Mani E. Sex attractant inhibitors of the codling moth Laspeyresia pomonella L (англ.) // Cellular and Molecular Life Sciences. — 1974. — Т. 30. — № 10. — С. 1142-1144.
- ↑ Ковтуненко В. А. Лекарственные средства с действием на центральную нервную систему. — Киев, 1997. — С. 46. — 464 с. — ISBN 966-569-170-8
- ↑ Тюкавкина Н. А., Бауков Ю. И. Биоорганическая химия: Учебник. — 2-е изд., перераб. и доп. — М.: «Медицина», 1991. — С. 158. — ISBN 5-225-00863-1
- ↑ 1 2 Спирты. Новый справочник химика и технолога. Радиоактивные вещества. Вредные вещества. Гигиенические нормативы. ChemAnalitica.com (1 апреля 2009 года). Архивировано из первоисточника 21 августа 2011. Проверено 26 августа 2009.
- ↑ Daniel C., Nachtman J. P. Toxicology of Alcohols, Ketones and Esters--Inhalation // Review of Inhalants: Euphoria to Dysfunction / Editors: Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.. — National Institute of Drug Abuse, 1977. — P. 112—116. — (Research Monograph (15)).
- ↑ 1 2 3 Спирты. Российская энциклопедия по охране труда. Яндекс.Словари. Проверено 26 августа 2009.
- ↑ The Clinical Toxicology Laboratory: Contemporary Practice of Poisoning Evaluation / Edired by Shaw L. M.. — Amer. Assoc. for Clinical Chemistry, 2001. — P. 173—174, 186. — ISBN 1-890883-53-0
- ↑ 1 2 3 Нейланд О. Я. Органическая химия: Учеб. для хим. вузов. — М.: «Высшая школа», 1990. — С. 286-287. — ISBN 5-06-001471-1
- ↑ Термодинамические показатели органических соединений. Новый справочник химика и технолога. Общие сведения. Строение вещества. Физические свойства важнейших веществ. Ароматические соединения. Химия фотографических процессов. Номенклатура органических соединений. Техника лабораторных работ. Основы технологии. Интеллектуальная собственность. ChemAnalitica.com (1 апреля 2009 года). Архивировано из первоисточника 21 августа 2011. Проверено 27 августа 2009.
- ↑ Maréchal Y. The Hydrogen Bond and the Water Molecule: The Physics and Chemistry of Water, Aqueous and Bio-Media. — Elsevier, 2007. — С. 18. — ISBN 0-444-51957-2
- ↑ 1 2 3 Глава I. Энергии разрыва связей // Энергии разрыва химических связей. Потенциалы ионизации и сродство к электрону / Отв. редактор В. Н. Кондратьев. — М.: «Наука», 1974. — С. 83.
- ↑ Бушуев Ю. Г., Дубинкина Т. А. Компьютерное моделирование структур метанола и жидкого метана // Журнал физической химии. — 1996. — Т. 70. — № 9. — С. 1629.
- ↑ Глава III. Потенциалы ионизации // Энергии разрыва химических связей. Потенциалы ионизации и сродство к электрону / Отв. редактор В. Н. Кондратьев. — М.: «Наука», 1974. — С. 247-248, 276.
- ↑ Робертс Дж., Касерио М. Основы органической химии = Basic principles of organic chemistry / Под редакцией академика Несмеянова А. Н.. — 2-е, дополненное. — М.: Мир, 1978. — Т. 1. — 843 с.
- ↑ 1 2 Чичибабин А. Е. Физические свойства предельных углеводородов (алканов). Основные начала органической химии. XuMuK.ru. Архивировано из первоисточника 21 августа 2011. Проверено 27 августа 2009.
- ↑ 1 2 3 Глава XIV. Физико-химические свойства жирных спиртов // Высшие жирные спирты (области применения, методы производства, физико-химические свойства) / Под редакцией С. М. Локтева. — М.: «Химия», 1970. — С. 283-295.
- ↑ 1 2 Курц А. Л., Брусова Г. П., Демьянович В. М. Раздел III. Свойства одноатомных спиртов. Одно- и двухатомные спирты, простые эфиры и их сернистые аналоги. ChemNet. Химический факультет МГУ (1999). Архивировано из первоисточника 21 августа 2011. Проверено 28 августа 2009.
- ↑ 1 2 Ведерников А. Н. Кислотность и основность органических соединений в растворах и газовой фазе // Соросовский образовательный журнал. — 2000. — № 8. — С. 49—52.
- ↑ McMurry J. Organic chemistry. — Seven edition. — Thomson, 2008. — ISBN 0-495-11258-5
- ↑ 1 2 Общая органическая химия. Кислородсодержащие соединения = Comprehensive Organic Chemistry / Под ред. Д. Бартона и В. Д. Оллиса. — М.: «Химия», 1982. — Т. 2. — 856 с.
- ↑ Функции кислотности // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1999. — Т. 5. — С. 422—424. — ISBN 5-85270-310-9
- ↑ 1 2 3 Спирты // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1992. — Т. 3. — С. 800—804. — ISBN 5-85270-039-8
- ↑ Hudlický M. Oxidation in Organic Chemistry. — ACS monograph 186. — Washington: American Chemical Society, 1990. — 434 p. — ISBN 0-8412-1780-7
- ↑ Хейнс А. Методы окисления органических соединений: Алканы, алкены, алкины и арены = Methods for the oxidation of organic compounds: Alkanes, Alkenes, Alkynes and Arenes / Перевод с англ., под редакцией И.П.Белецкой. — М.: Мир, 1988. — С. 82—108. — 400 с. — ISBN 5-03-000149-2
- ↑ 1 2 3 4 Титце Л., Айхер Т. Препаративная органическая химия: Реакции и синтезы в практикуме органической химии и научно-исследовательской лаборатории / Пер. с нем.. — М.: «Мир», 1999. — С. 73—75. — 704 с. — ISBN 5-03-002940-0
- ↑ Corey E. J., Nicolaou K. C., Shibasaki M., Machida Y., Shiner C. S. Superoxide ion as a synthetically useful oxygen nucleophile (англ.) // Tetrahedron Letters. — 1975. — Т. 16. — № 37. — С. 3183—3186.
- ↑ 1 2 Метанол: обзор технологий. Базовая химия и нефтехимия. Newchemistry.ru Новые химические технологии. Архивировано из первоисточника 21 августа 2011. Проверено 25 мая 2010.
- ↑ Бубнов Ю. Н. Аллилбораны. Принципы реагирования и применение в органическом синтезе // Вестник Московского университета : Серия 2. Химия. — 2005. — Т. 46. — № 3. — С. 140—144.
- ↑ Baylis-Hillman Reaction (англ.). Name Reactions. Organic Chemistry Portal. Архивировано из первоисточника 21 августа 2011. Проверено 23 сентября 2009.
- ↑ Гриньяра реакция // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 1202—1205.
- ↑ Вацуро К. В., Мищенко Г. Л. 683. Циглер (Ziegler) // Именные реакции в органической химии. — М.: «Химия», 1976. — С. 464—465.
- ↑ Норман Ж. Ф. Медьорганические соединения и органокупраты в синтезе // Успехи химии. — 1973. — Т. 42. — № 4. — С. 645—676.
- ↑ Петров А. А., Бальян Х. В., Трощенко А. Т. Органическая химия / под редакцией Стадничука М. Д.. — Санкт-Петербург: «Иван Фёдоров», 2002. — С. 138—143, 145, 150—151. — 624 с. — ISBN 5-81940-067-4
- ↑ 1 2 3 Methanol (англ.). WP Report. SRI Consulting (January 2009). Архивировано из первоисточника 21 августа 2011. Проверено 29 сентября 2009.
- ↑ Berg Ch. World Fuel Ethanol - Analysis and Outlook (англ.). The Online Distillery Network for Distillers & Fuel Ethanol Plants Worldwide (April, 2004). Архивировано из первоисточника 21 августа 2011.
- ↑ 1 2 3 4 5 6 Chauvel A., Lefebvre G. Petrochemical processes 2. Major Oxygenated, Chlorinated and Nitrated Derivatives. — 2nd ed. — Paris: Editions Technip, 1989. — Т. 2. — 396 p. — ISBN 2-7108-0563-4
- ↑ Пропиловый спирт // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1995. — Т. 4. — С. 204. — ISBN 5-85270-092-4
- ↑ Product Safety Assessment DOW™ n-Propanol (англ.) (pdf). The Dow Chemical Company. Архивировано из первоисточника 21 августа 2011.
- ↑ Isopropanol (IPA) CAS No: 67-63-0 (англ.). Chemical intelligence. ICIS.com. Архивировано из первоисточника 21 августа 2011.
- ↑ 1 2 Isopropyl Alcohol (IPA) (англ.). WP Report. SRI Consulting (January 2010). Архивировано из первоисточника 21 августа 2011.
- ↑ 1 2 3 4 5 6 7 Ланге К. Р. Поверхностно-активные вещества: синтез, свойства, анализ, применение = Surfactants. A Practical Handbook / Пер. с англ. — СПб.: «Профессия», 2004. — 240 с. — ISBN 5-93913-068-2
- ↑ Brackmann B., Hager C.-D. The Statistical World of Raw Materials, Fatty Alcohols and Surfactants (англ.). CESIO 6th World Surfactants Congress, Berlin, June 20–23, 2004. Laboratory of Formulation, Interfaces, Rheology and Processes FIRP (Venezuela). Архивировано из первоисточника 21 августа 2011. Проверено 20 сентября 2010.
- ↑ Ethylene Glycol (англ.). WP Report. SRI Consulting (January 2010). Архивировано из первоисточника 21 августа 2011.
- ↑ Pagliaro M., Rossi M. Future of Glycerol. — 2nd Edition. — Cambridge: Royal Society of Chemistry, 2010. — P. 11. — (RSC Green Chemistry No. 8). — ISBN 978-1-84973-046-4
- ↑ 1 2 3 Speight J. G. Chemical and Process Design Handbook. — McGraw-Hill, 2002. — ISBN 0-07-137433-7
- ↑ 1 2 3 4 5 Chenier Ph. J. Survey of Industrial Chemistry. — Third Edition. — New York: Kluwer Academic / Plenum Publishers, 2002. — 536 p. — ISBN 0-306-47246-5
- ↑ Fermentation from biomass and waste (англ.). Ethanol. Greener Industry. Архивировано из первоисточника 21 августа 2011. Проверено 12 сентября 2010.
- ↑ Ebert J. Biobutanol: The Next Big Biofuel? (англ.) // Biomass Magazine. — 2008. — № 5.
- ↑ Environmental Biotechnology / Edited by Wang L. K., Tay J.-H., Ivanov V., Hung Y.-T.. — Springer, 2010. — Т. 10. — P. 373. — (Handbook of Environmental Engineering). — ISBN 978-1-58829-166-0
- ↑ 1 2 Терней А. Л. Современная органическая химия / Под ред. Н. Н. Суворова. — 2-е, переработанное. — М.: «Мир», 1981. — Т. 1. — С. 418—421.
- ↑ Галоформная реакция // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 970—971.
- ↑ Williams D. L. H. Nitrosation Reactions and The Chemistry of Nitric Oxide. — First edition. — Elsevier, 2004. — С. 86. — ISBN 0-444-51721-9
- ↑ 1 2 Шрайнер Р., Фьюзон E., Кёртин Д., Моррилл Т. Идентификация органических соединений / Пер. с англ.. — М.: «Мир», 1983. — С. 167—185.
- ↑ Jungreis E. Spot Test Analysis // Encyclopedia of Analytical Chemistry: Applications, Theory, and Instrumentation, 15 Volume Set / Editor-in-Chief: Robert A. Meyers. — John Wiley and Sons, 2000. — Т. 15. — С. 7. — 14344 с. — ISBN 978-0-471-97670-7
- ↑ Zvi Rappoport, Ph. D. Handbook of Tables for Organic Compound Identification. — Third Edition. — Boca Raton: CRC Press, 1967, 2000 (reprinted). — P. 77—90. — ISBN 0-8493-0303-6
- ↑ 1 2 Сиггиа С., Ханна Дж. Г. Количественный органический анализ по функциональным группам / Пер. с англ.. — М.: «Химия», 1983. — С. 16—19.
- ↑ Вульфсон Н. С., Заикин В. Г., Микая А. И. Масс-спектрометрия органических соединений. — М.: «Химия», 1986. — С. 162—163.
- ↑ 1 2 3 4 5 Преч Э., Бюльманн Ф., Аффольтер К. Определение строения органических соединений. Таблицы спектральных данных / Пер. с англ. — М.: «Мир», 2006. — 438 с. — (Методы в химии). — ISBN 5-03-003586-9
- ↑ 1 2 Браун Д., Флойд А., Сейнзбери М. Спектроскопия органических веществ / Пер. с англ.. — М.: «Мир», 1992. — 300 с. — ISBN 5-03-002111-6
- ↑ Ионин Б. И., Ершов Б. А., Кольцов А. И. ЯМР-спектроскопия в органической химии / Под ред. Б. А. Ершова. — 2-е изд., переработанное. — Л.: «Химия», 1983. — С. 177.
- ↑ 1 2 Linak E., Inoguchi Y., Janshekar H. Ethanol (англ.). CEH Report. SRI Consulting (April 2009). Архивировано из первоисточника 21 августа 2011. Проверено 18 августа 2010.
- ↑ 1-Propanol (англ.). Environmental Health Criteria (EHC) Monographs. International Programme on Chemical Safety (IPCS) INCHEM. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Isopropanol (IPA) Uses and Market Data (англ.). Chemical Intelligence. ICIS.com. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Technical Data Sheet. N-Butanol (англ.). BASF Corporation. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Butanol is an alcohol that replaces gasoline (англ.). ButylFuel, LLC. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Глава I. Мировое производство и потребление высших жирных спиртов // Высшие жирные спирты (области применения, методы производства, физико-химические свойства) / Под редакцией С. М. Локтева. — М.: «Химия», 1970. — С. 28-32.
- ↑ Weissermel K., Arpe H-J. Industrial organic chemistry. — 4th ed. — Weinheim: Wiley-VCH, 2003. — P. 205—206. — ISBN 978-3-527-30578-0
- ↑ Malveda M., Mori H. Cyclohexanol and Cyclohexanone (англ.). CEH Report. SRI Consulting (January 2009). Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Ethylene Glycol (EG) CAS No: 107-21-1 (англ.). Chemical Intelligence. ICIS.com. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Propylene Glycol (PG) CAS No: 57-55-6 (англ.). Chemical Intelligence. ICIS.com. Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ Bizzari S., Blagoev M., Mori H. Glycerin (англ.). CEH Report. SRI Consulting (December 2008). Архивировано из первоисточника 21 августа 2011. Проверено 19 августа 2010.
- ↑ 1 2 Chauvel A., Lefebvre G. Petrochemical processes 1. Synthesis-gas Derivatives and Major Hydrocarbons. — 2nd ed. — Paris: Editions Technip, 1989. — Т. 1. — 405 p. — ISBN 2-7108-0562-5
- ↑ Метиламины // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1992. — Т. 3. — С. 106—107. — ISBN 5-85270-039-8
- ↑ 1 2 3 Лебедев Н. Н. Химия и технология основного органического и нефтехимического синтеза: Учебник для вузов. — 4-е изд., перераб. и доп. — М.: Химия, 1988. — 592 с. — ISBN 5-7245-0008-6
- ↑ Использование этилового спирта в качестве компонента автомобильного бензина. Анализ нормативной документации. Законы и практика. Аналитический портал химической промышленности Newchemistry.ru. Архивировано из первоисточника 21 августа 2011. Проверено 12 сентября 2010.
- ↑ Карпов С. А., Кунашев Л. Х., Царев А. В., Капустин В. М. Применение алифатических спиртов в качестве экологически чистых добавок в автомобильные бензины // Нефтегазовое дело. — 2006. — № 2.
- ↑ Использование спиртов как добавок к нефтяным топливам. Альтернативные топлива, энергетика. Аналитический портал химической промышленности Newchemistry.ru. Архивировано из первоисточника 21 августа 2011. Проверено 12 сентября 2010.
- ↑ Биодизель. Российская Национальная Биотопливная Ассоциация. Проверено 12 сентября 2010.
- ↑ Global ethanol production to reach 85.9 billion litres in 2010: Global Renewable Fuels Alliance releases 2010 biofuels production forecast. Press Release. Global Renewable Fuels Alliance (March 21, 2010). Архивировано из первоисточника 2 февраля 2012. Проверено 25 мая 2010.
- ↑ Карпов С. А. Актуальные аспекты применения топливного этанола в России и США // Нефтегазовое дело. — 2006. — № 2.
- ↑ Smith J. L., Workman J. P. Alcohol for Motor Fuels (англ.). Colorado State University Extension (December, 2004). Архивировано из первоисточника 21 августа 2011. Проверено 12 сентября 2010.
- ↑ Дринберг С. А., Ицко Э. Ф. Растворителя для лакокрасочных материалов: Справочное пособие. — 2-е изд., перераб. и доп. — Л.: «Химия», 1986. — С. 51.
- ↑ Ethanol Uses and Market Data (англ.). Chemical Intelligence. ICIS.com. Архивировано из первоисточника 21 августа 2011. Проверено 14 сентября 2010.
- ↑ 2-Propanol (англ.). Environmental Health Criteria (EHC) Monographs. International Programme on Chemical Safety (IPCS) INCHEM. Архивировано из первоисточника 21 августа 2011. Проверено 18 августа 2010.
- ↑ Handbook of Solvents / Edited by Wypych G. — Toronto: Chem Tec Publishing, 2001. — P. 847—1052. — ISBN 1-895198-24-0
- ↑ 1 2 3 4 5 6 Chemistry and Technology of Surfactants / Edited by Richard J. Farn. — Blackwell Publishing Ltd, 2006. — 315 p. — ISBN 978-14051-2696-0
- ↑ Dierker M., Schäfer H. J. Surfactants from oleic, erucic and petroselinic acid: Synthesis and properties (англ.) // European Journal of Lipid Science and Technology. — 2010. — Т. 112. — № 1. — С. 122.
- ↑ 1 2 Плетнев М. Ю. Косметико-гигиенические моющие средства // . — «Химия». — М., 1990. — С. 17—20. — ISBN 5-7245-0275-5
- ↑ Chanda M., Roy S. K. Industrial Polymers, Specialty Polymers, and Their Applications. — Boca Raton: CRC Press, Taylor & Francis Group, 2009. — P. 1-55—1-58, 1-97—1-98. — ISBN 978-1-4200-8058-2
- ↑ Барштейн Р. С., Кирилович В. И., Носовский Ю. Е. Пластификаторы для полимеров. — М.: «Химия», 1982. — С. 19—20.
- ↑ Гидравлические жидкости // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 1068.
- ↑ Hodges P. K. B. Hydraulic Fluids. — New York—Toronto: John Wiley & Sons, 1996. — P. 33—36. — ISBN 0-470-23617-5
- ↑ Lubricants and Lubrication / Edited by Theo Mang and Wilfried Dresel. — 2nd edition. — Weinheim: Wiley-VCH GmbH, 2007. — P. 516—517. — ISBN 978-3-527-31497-3
- ↑ 1 2 3 4 Мельников Н. Н. Пестициды. Химия, технология и применение. — М.: «Химия», 1987. — 710 с.
- ↑ Proclonol (англ.). Compendium of Pesticide Common Names. Alan Wood’s Web site. Архивировано из первоисточника 21 августа 2011. Проверено 26 сентября 2010.
- ↑ 1 2 3 Unger T. A. Pesticide Synthesis Handbook. — New Jersey: Noyes Publications, 1996. — 1080 p. — ISBN 0-8155-1401-8
- ↑ Guidance Manual for Selecting Protective Clothing for Agricultural Pesticide Operations / Contract No. 68-C9-0037. — Work Assignment 0-20. — Cincinatti: U.S. EPA, 1994. — P. 45.
- ↑ 1 2 3 Шнайдман Н. О. Производство витаминов. — Издательство второе, перераб. — М.: «Пищевая промышленность», 1973. — 440 с.
- ↑ Pharmaceutical Manufacturing Encyclopedia / Ed. by Marshall Sittig. — Third Edition. — Norwich: William Andrew Publising, 2007. — 3838 p. — ISBN 978-0-8155-1526-5
- ↑ Сарафанова Л. А. Пищевые добавки: Энциклопедия. — 2-е изд., испр. и доп. — СПб.: ГИОРД, 2004. — 808 с. — ISBN 5-901065-79-4
- ↑ Войткевич С. А. 865 душистых веществ для парфюмерии и бытовой химии. — М.: «Пищевая промышленность», 1994. — 594 с.
- ↑ Хейфиц Л. А., Дашутин В. М. Душистые вещества и другие продукты для парфюмерии. — М.: «Химия», 1994. — 256 с. — ISBN 5-7245-0967-9
- ↑ List of Functions (англ.). Cosmetics CosIng. European Commission. Health and Consumers. Архивировано из первоисточника 21 августа 2011. Проверено 8 сентября 2010.
- ↑ 1 2 Машковский М. Д. Лекарственные средства: В 2-х томах. — 14-е изд., перераб., исправ. и доп. — М.: ООО «Издательство Новая Волна»: Издатель С. Б. Дивов, 2002. — Т. 2. — 608 с. — ISBN 5-7864-0129-4
- ↑ Машковский М. Д. Лекарственные средства: В 2-х томах. — 14-е изд., перераб., исправ. и доп. — М.: ООО «Издательство Новая Волна»: Издатель С. Б. Дивов, 2002. — Т. 1. — 540 с. — ISBN 5-7864-0128-6
- ↑ Органические ингибиторы. Коррозия и защита от коррозии. TehnoInfa.Ru. Архивировано из первоисточника 21 августа 2011. Проверено 15 сентября 2010.
- ↑ Флотация // Химическая энциклопедия / Главный редактор H. C. Зефиров. — М.: Научное Издательство «Большая Российская Энциклопедия», 1999. — Т. 5. — С. 207—208. — ISBN 5-85270-310-9
- ↑ Новые разработки компании Croda в производстве продуктов по уходу за автомобилем. Компания «Кэмикл Сервис». Архивировано из первоисточника 21 августа 2011. Проверено 15 сентября 2010.
- ↑ Орлова Е. Ю. Химия и технология бризантных взрывчатых веществ: Учебник для вузов. — 3-е изд., перераб. — Л.: «Химия», 1981. — С. 263, 278, 281.
- ↑ Франке З. Химия отравляющих веществ / Пер. с нем.. — М.: Химия, 1973. — Т. 1. — С. 271, 288.
- ↑ Франке З., Франц П., Варнке В. Химия отравляющих веществ / Пер. с нем., под редакцией акад. И. Л. Кнунянца и д-ра хим. наук Р. Н. Стерлина. — М.: Химия, 1973. — Т. 2. — С. 317.
Литература
Англоязычная
- Alcoholic Fuels / Edited by Shelley Minteer. — Boca Raton: CRC Press / Taylor & Francis, 2006. — 273 p. — ISBN 978-0-8493-3944-8
- Alcohols / Volume Editor: Prof. Jonathan Clayden. — Science of Synthesis: Houben-Weyl Methods of Molecular Transformations. — Georg Thieme Verlag, 2008. — Т. 36. — 1294 p. — (Category 5: Compounds with One Carbon-Heteroatom Bonds). — ISBN 978-1-588-90527-7
- Catalytic Conversions of Synthesis Gas and Alcohols to Chemicals / Editor: Richard G. Herman. — Plenum Press, 1984. — 475 p. — (American Chemical Society, Middle Atlantic Regional Meeting). — ISBN 0-30-641614-X
- Mellan I. Polyhydric Alcohols. — Spartan Books. — 1962. — 208 p.
- Monick J. A. Alcohols: Their Chemistry, Properties, and Manufacture. — Reinhold, 1968. — 594 p. — ISBN 0-442-15601-4
- Monohydric Alcohols: Manufacture, Applications, and Chemistry: based on a symposium / Editor: Edward J. Wickson. — American Chemical Society, 1981. — 222 p. — (ACS symposium series (volume 159)). — ISBN 0-841-20637-6
- Otera J., Nishikido J. Esterification: Methods, Reactions, and Applications. — Second edition. — Weinheim: Wiley-VCH, 2010. — 374 p. — ISBN 978-3-527-32289-3
- Tojo G., Fernández M. Oxidation of Alcohols to Aldehydes and Ketones. — First Edition. — New York: Springer, 2006. — 375 p. — ISBN 0-387-23607-4
- Weissermel K., Arpe H-J. Alcohols // Industrial organic chemistry. — 4th ed. — Weinheim: Wiley-VCH, 2003. — P. 193—266. — ISBN 978-3-527-30578-0
Русскоязычная
- Спирты // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
- Высшие жирные спирты (области применения, методы производства, физико-химические свойства) / Под редакцией С. М. Локтева. — М.: «Химия», 1970. — 329 с.
- Курц А. Л., Брусова Г. П., Демьянович В. М. Одно- и двухатомные спирты, простые эфиры и их сернистые аналоги. Учебные материалы. Органическая химия. ChemNet. Химический факультет МГУ (1999). Архивировано из первоисточника 21 августа 2011. Проверено 10 июля 2010.
- Маркизова Н. Ф., Гребенюк А. Н., Башарин В. А., Бонитенко Е. Ю. Спирты. — СПб.: «Фолиант», 2004. — 112 с. — (Токсикология для врачей). — ISBN 5-93929-089-2
- Спирты. Энциклопедия по охране и безопасности труда. Том IV. Раздел XVIII. Справочники. Обзор химических соединений. Институт промышленной безопасности, охраны труда и социального партнерства. Архивировано из первоисточника 21 августа 2011. Проверено 27 декабря 2010.
Ссылки
- Алкоголи // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
- Спирты. Фенолы. Органическая химия. Видеоопыты. Единая коллекция цифровых образовательных ресурсов. Архивировано из первоисточника 21 августа 2011. Проверено 6 июля 2010.
Спирты (0°) Метанол Первичные спирты (1°) Этанол · Пропанол · Бутиловый спирт/Изобутанол · Амиловый спирт · Гексанол · Гептанол
Жирные спирты: Октанол (C8) · Нонанол (C9) · Деканол (C10) · Ундеканол (C11) · Додеканол (C12) · Тетрадеканол (C14) · Цетиловый спирт (C16)Вторичные спирты (2°) Изопропиловый спирт · 2-Бутанол · 2-Гексанол Третичные спирты (3°) 2-Метил-2-бутанол Классификация спиртов Алифатические одноатомные спирты Метанол · Этанол · Пропанол-1 · Пропанол-2 · Бутанол-1 · Бутанол-2 · 2-метилпропанол-1 · 2-метилпропанол-2 · Пентанол · Гексанол · Гептанол · Октанол · Нонанол · Деканол · Высшие жирные спирты Ненасыщенные одноатомные спирты Аллиловый спирт · Пропаргиловый спирт · Эленол · Гераниол · Линалоол · Цитронеллол Алициклические насыщенные
одноатомные спиртыЦиклогексанол · Ментол · Борнеол · Туйол Алициклические ненасыщенные
одноатомные спиртыТерпинеол · Вербенол · Терпинен-4-ол · Холестерол Ароматические одноатомные спирты Бензиловый спирт · 2-фенилэтанол Двухатомные и трёхатомные спирты Этиленгликоль · Пропиленгликоль · Глицерин Многоатомные спирты Пентаэритрит · Ксилит · Инозит · Сорбит · Маннит Категории:- Спирты
- Кислородсодержащие органические соединения
- Функциональные группы
Wikimedia Foundation. 2010.


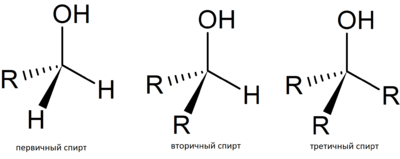


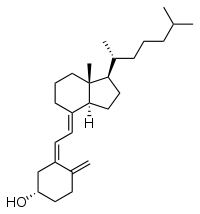






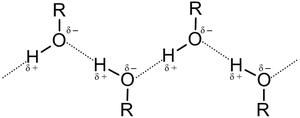




![\mathsf{(R)_3CH+[O]}\rightarrow\mathsf{(R)_3COH}](e93ae02dd27927dd3c9086bebe2f507a.png)

![\mathsf{R\!\!-\!\!CH_2\!\!-\!\!CH\!\!=\!\!CH\!\!-\!\!R'+[O]}\rightarrow\mathsf{R\!\!-\!\!CH\!\!=\!\!CH\!\!-\!\!CH(OOH)\!\!-\!\!R'}\ \xrightarrow[\mathrm{-Na_2SO_4}]{\mathrm{+Na_2SO_3}}\ \ \mathsf{R\!\!-\!\!CH\!\!=\!\!CH\!\!-\!\!CH(OH)\!\!-\!\!R'}](0431ba4631ce8e7eb31dadab2d16c31e.png)
![\mathsf{R\!\!-\!\!CHO+2[H]}\rightarrow\mathsf{R\!\!-\!\!CH_2OH}](b1d570e7861428fe9410a7cb9dd2160a.png)
![\mathsf{R\!\!-\!\!COOR'+4[H]}\rightarrow\mathsf{R\!\!-\!\!CH_2OH+R'OH}](64a3549732d5f36a31809536605a8efe.png)

![\mathsf{RCH\!\!=\!\!CH_2+H_2O}\ \xrightarrow[\mathrm{NaBH_4}]{\mathrm{Hg(CH_3COO)_2}}\ \ \mathsf{RCH_2\!\!-\!\!CH_2OH}\](4a000ba6b7f5c1a82abf898527b6e1c8.png)
![\mathsf{RCH\!\!=\!\!CH_2}\ \xrightarrow[\mathrm{H_2O_2,\ OH^-}]{\mathrm{B_2H_6}}\ \ \mathsf{RCH_2\!\!-\!\!CH_2OH}\](e7ee8ffa4bcad351ef132543b19fe5f4.png)



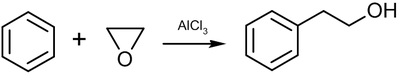
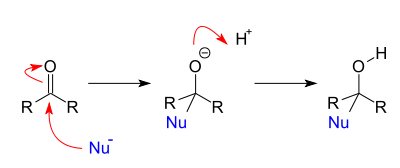

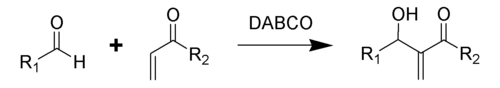



![\mathsf{RCH\!\!=\!\!CH_2}\ \xrightarrow[\mathrm{-RH}]{\mathrm{H_2,\ AlR_3}}\ \mathsf{RCH_2CH_2\!\!-\!\!AlR_2}\ \xrightarrow{\mathrm{O_2}}\ \mathsf{RCH_2CH_2\!\!-\!\!O\!\!-\!\!Al(OR)_2}\ \xrightarrow{\mathrm{H_2O}}\ \mathsf{RCH_2CH_2OH}](8d4614a13188d8675355667b9aa26ad6.png)

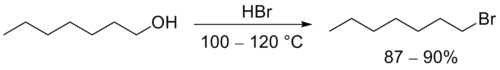
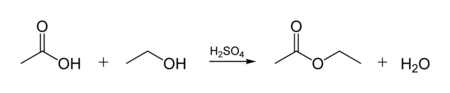


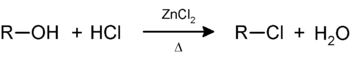



![\mathsf{[Ce(NO_3)_6]^{2-}+ROH}\rightarrow\mathsf{[Ce(OR)(NO_3)_5]^{2-}+HNO_3}](4c9733cf228f73d151aaef352ca3e0e7.png)