- Тетрафторид углерода
-
Тетрафторид углерода 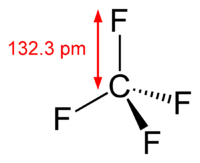

Общие Систематическое наименование фторид углерода(IV), тетрафторид углерода Сокращения R14 Традиционные названия тетрафторметан, перфторметан, метфоран, углерод четырехфтористый, углерода тетрафторид, фреон 14, хладон 14 Химическая формула CF4 Физические свойства Состояние (ст. усл.) бесцветный газ без запаха Молярная масса 88.0043 г/моль Плотность 3.72 г/см³ Термические свойства Температура плавления −183.6 °C Температура кипения −127.8 °C Температура вспышки негорюч °C Температура самовоспламенения 1100 °C Критическая точка температура: −45,65 °C
давление: 3,745 МПа
плотность: 0,625 г/см³
Энтальпия образования (ст. усл.) −933 кДж/моль Химические свойства Растворимость в воде Очень мало растворим в воде
(20 °C) 0.005 %
Растворимость в остальных веществах смешивается с этанолом, эфиром, бензолом Оптические свойства Показатель преломления 1.113 Структура Дипольный момент 0.461 Д Классификация Рег. номер CAS 75-73-0 SMILES C(F)(F)(F)F Регистрационный номер EC 200-896-5 RTECS FG4920000 Безопасность Токсичность Тетрафторметан — бинарное химическое соединение. Химическая формула — CF4. Синонимы: четырёхфтористый углерод, тетрафторид углерода, фреон 14, хладон 14.
Тетрафторметан является самым простым из фторуглеродов. Oбладает высокой химической стойкостью. Из-за большого количества связей углерод-фтор и высокой электроотрицательности фтора атом углерода в этом соединении имеет значительный положительный заряд, что укрепляет и укорачивает связь углерод-фтор. Тетрафторметан является парниковым газом.
Содержание
Свойства
Физические
При комнатной температуре представляет собой химически инертный, бесцветный газ без запаха.
Свойства соединения
Тетрафторметан является одним из самых стабильных соединений в органической химии. Из фторпроизводных метана, представленных фторметаном, дифторметаном, трифторметаном и тетрафторметаном, связь фтора и углерода в тетрафторметане является самой прочной.
Получение
Чистый тетрафторметан был впервые синтезирован в 1926 году[1]. Тетрафторметан может быть получен в лабораторных условиях при реакции карбида кремния с фтором:
Она также может быть получен фторированием двуокиси углерода, окиси углерода или фосгена с помощью тетрафторида серы. Коммерчески он производится реакцией фтора с дихлордифторметаном или хлортрифторметаном; также — в ходе электролиза фторидов металла MF, MF2 с помощью угольного электрода.
Тетрафторметан, как и другие фторуглероды, весьма устойчив благодаря связи фтор—углерод. Энергия связи в этом соединении равна 515 кДж/моль. В результате этого он инертен по отношению к кислотам и гидроксидам. Тем не менее, он реагирует со взрывом с щелочными металлами. При контакте тетрафторметана с пламенем получаются токсичные газы (например карбонилфторид или окись углерода); в присутствии воды получается фтороводород.
Синтез
Также можно получить данное вещество из углекислого газа, угарного газа или фосгена фторированием тетрафторидом серы:
При температуре в 350—375 °C углерод в форме графита реагирует с трифторидом азота:
Самым простым способом получения является реакция при температуре выше 900 °C углерода с фтором:
Использование
- Тетрафторметан иногда в качестве низкотемпературного хладагента (фреон 14, хладон 14).
- В микроэлектронике, отдельно, или в сочетании с кислородом как плазменный протравливатель на кремнии, диоксиде кремния или нитрида кремния.
- Компонент дыхательных смесей при глубоководных погружениях.
- В системах автоматического пожаротушения.
- Стабилизатор разложения озона.
- Разбавитель при проведении химических реакций.
- Реагента для получения фторорганических продуктов.
Воздействие на окружающую среду
Тетрафторметан является сильным парниковым газом, который способствует парниковому эффекту. Это очень стабильное соединение, время его распада составляет примерно 50 000 лет, в то время как самая высокая отметка ПГП составляет 6500 лет (главным парниковым газом является CO2).
Тетрафторметан схож по строению с хлорфторуглеродом (ХФУ), но в отличие от него тетрафторметан не разрушает озоновый слой. Это происходит потому, что с озоном взаимодействуют атомы хлора в ХФУ, которые образуются под действием ультрафиолетового излучения.
Опасность использования
При контакте кожи с жидкостью возможно обморожение. Вдыхание тетрафторметана может привести, в зависимости от концентрации, к головной боли, помутнению сознания, тошноте, головокружению и повредить сердечно-сосудистую систему. Длительное воздействие может вызвать серьёзные повреждения сердца.
Благодаря своей плотности тетрафторметан может вытеснить воздух, что может привести к удушению в недостаточно проветриваемых помещениях.
См. также
Примечания
- ↑ Greenwood, Norman N.; Earnshaw, Alan. (1997), Chemistry of the Elements (2nd ed.), Oxford: Butterworth-Heinemann, ISBN 0080379419
Соединения фтораГексафторалюминат натрия (Na3AlF6) • Гексафтороантимонат водорода (HSbF6) • Гексафторид платины (PtF6) • Гексафторид селена (SeF6) • Гексафторид теллура (TeF6) • Гексафторогерманат калия (K2[GeF6]) • Гексафторогерманат рубидия (Rb2[GeF6]) • Гексафторогерманат цезия (Cs2[GeF6]) • Гексафторосиликат(IV) калия (K2[SiF6]) • Гексафторосиликат натрия (Na2SiF6) • Гексафторплатинат ксенона (XePtF6) • Гексафторсиликат аммония ((NH4)2SiF6) • Гептафторид рения (ReF7) • Гептафторониобат(V) калия (K2[NbF7]) • Гидрофторид аммония ([NH4][HF2]) • Гидрофторид калия (HF2K) • Декафторид дисеры (S2F10) • Диоксидифторид (F2O2) • Диоксидифторид молибдена(VI) (MoF2O2) • Дифтордиазин (N2F2) • Дифторид радона (F2Rn) • Кремнефтористоводородная кислота (H2SiF6) • Монофторид алюминия (AlF) • Монофторид углерода (CF) • Оксид-фторид урана (UO2F2) • Окситетрафторид вольфрама(VI) (WOF4) • Окситетрафторид молибдена(VI) (MoOF4) • Оксифторид иттрия (YOF) • Оксифторид лантана(III) (LaOF) • Оксотетрафторид ксенона (XeOF4) • Оксотрифторид ванадия(V) (F3OV) • Пентафторид висмута (BiF5) • Пентафторид мышьяка (AsF5) • Пентафторид сурьмы (SbF5) • Пентафторид урана (UF5) • Пентафторид фосфора (PF5) • Субфторид серебра (Ag2F) • Тетрафторалюминат калия (KAlF4) • Тетрафтороборат лития (LiBF4) • Тетрафтороборат меди(II) (Cu(BF4)2) • Тетрафтороборат натрия (NaBF4) • Тетрафтороборат нитрозила (BF4NO) • Тетрафтороборат нитрония (BNO2F4) • Тетрафтороборат серебра (AgBF4) • Тетрафторборная кислота (HBF4) • Тетрафторид дибора (B2F4) • Тетрафторид кремния (SiF4) • Тетрафторид селена (SeF4) • Тетрафторид теллура (TeF4) • Тетрафторгидразин (N2F4) • Трифторид алюминия (AlF3) • Трифторид бора (BF3) • Трифторид мышьяка (AsF3) • Трифторид висмута (BiF3) • Трифторид сурьмы (SbF3) • Трифторид тиазила (NSF3) • Трифторид фосфора (PF3) • Фторфосфат натрия (Na2PFO3) • Фторамин (NH2F) • Фторид азота(III) (NF3) • Фторид аммония (NH4F) • Фторид бария (BaF2) • Фторид бериллия (BeF2) • Фторид брома(I) (BrF) • Фторид брома(III) (BrF3) • Фторид брома(V) (BrF5) • Фторид ванадия(III) (VF3) • Фторид ванадия(IV) (VF4) • Фторид ванадия(V) (VF5) • Фторид вольфрама(VI) (WF6) • Фторид галлия(III) (GaF3) • Фторид гафния(IV) (HfF4) • Фторид дейтерия (DF) • Фторид диртути(2+) (Hg2F2) • Фторид железа(II) (FeF2) • Фторид железа(III) (FeF3) • Фторид золота(III) (AuF3) • Фторид золота(V) (AuF5) • Фторид индия(III) (InF3) • Фторид иода(I) (IF) • Фторид иода(III) (IF3) • Фторид иода(V) (IF5) • Фторид иода(VII) (IF7) • Фторид иридия(IV) (IrF4) • Фторид иридия(V) (IrF5) • Фторид иридия(VI) (IrF6) • Фторид иттербия(III) (YbF3) • Фторид иттрия (YF3) • Фторид иттрия-лития (LiYF4) • Фторид кадмия (CdF2) • Фторид калия (KF) • Фторид кальция (CaF2) • Фторид кислорода(II) (OF2) • Фторид кобальта(II) (CoF2) • Фторид кобальта(III) (CoF3) • Фторид криптона(II) (KrF2) • Фторид ксенона(II) (XeF2) • Фторид ксенона(IV) (XeF4) • Фторид ксенона(VI) (XeF6) • Фторид лития (LiF) • Фторид магния (MgF2) • Фторид марганца(II) (MnF2) • Фторид марганца(III) (MnF3) • Фторид меди(I) (CuF) • Фторид меди(II) (CuF2) • Фторид молибдена(VI) (MoF6) • Фторид натрия (NaF) • Фторид никеля(II) (NiF2) • Фторид ниобия(V) (NbF5) • Фторид нитрозила) (NOF) • Фторид оксида азота(IV) (NO2F) • Фторид оксида серы(IV) (SO2F2) • Фторид олова(II) (SnF2) • Фторид олова(IV) (SnF4) • Фторид плутония(III) (PuF3) • Фторид плутония(IV) (PuF4) • Фторид плутония(VI) (PuF6) • Фторид радия (RaF2) • Фторид рения(IV) (ReF4) • Фторид рения(VI) (ReF6) • Фторид рения(VII) (ReF7) • Фторид ртути(II) (HgF2) • Фторид рубидия (RbF) • Фторид самария(III) (SmF3) • Фторид свинца(II) (PbF2) • Фторид серебра(I) (AgF) • Фторид серебра(II) (AgF2) • Фторид серы(IV) (SF4) • Фторид серы(VI) (SF6) • Фторид скандия(III) (ScF3) • Фторид стронция (SrF2) • Фторид таллия(I) (TlF) • Фторид тантала(V) (TaF5) • Фторид теллура(IV) (TeF4) • Фторид технеция(VI) (TcF6) • Фторид тиазила (NSF) • Фторид тианила (SOF2) • Фторид титана(III) (TiF3) • Фторид титана(IV) (TiF4) • Фторид тория(IV) (ThF4) • Фторид урана(III) (UF3) • Фторид урана(IV) (UF4) • Фторид урана(V) (UF5) • Фторид урана(VI) (UF6) • Фторид хлора(I) (ClF) • Фторид хлора(III) (ClF3) • Фторид хлора(V) (ClF5) • Фторид хрома(III) (CrF3) • Фторид хрома(IV) (CrF4) • Фторид хрома(V) (CrF5) • Фторид цезия (CsF) • Фторид цинка (ZnF2) • Фторид циркония(IV) (ZrF4) • Фторид-хлорид оксида серы(IV) (ClFO2S) • Фторноватистая кислота (HOF) • Фтороводород (HF) • Фторосульфоновая кислота (FSO3H) • Фторид хлорила (ClO2F) • Фторид перхлорила (ClO3F) • Фторид оксиперхлорила (ClO3OF)
Категории:- Фториды
- Фторорганические соединения
- Галогензамещённые метаны
-
Wikimedia Foundation. 2010.





