- Диметилформамид
-
N,N-Диметилформамид 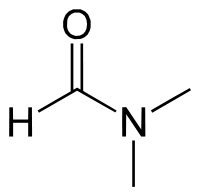
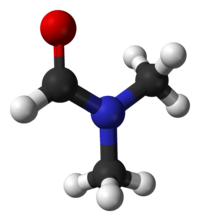
Общие Систематическое наименование N,N-Диметилформамид Сокращения ДМФА Традиционные названия (CH3)2NC(O)H Эмпирическая формула C3H7NO Молярная масса 73.09 г/моль Физические свойства Плотность вещества 0,9445 г/см³ Состояние (ст. усл.) вязкая прозрачная жидость Динамическая вязкость (ст. усл.) 0,795 Па·с
(при 20 °C)Термические свойства Температура плавления -61 °C Температура кипения 153 °C Температура вспышки 59 °C Молярная теплоёмкость (ст. усл.) 148,37 Дж/(моль·К) Энтальпия (ст. усл.) 192 кДж/моль Удельная теплота парообразования 42,3 Дж/кг Химические свойства Растворимость в воде ∞ г/100 мл Растворимость в в спирте ∞ г/100 мл Структура Дипольный момент 3,82 Дебай Классификация номер CAS 68-12-2 Токсикология ЛД50 4,2 (мыши) мг/кг
N,N-Диметилформамид (Диметилформамид, ДМФА) - органическое соединение с формулой (CH3)2NC(O)H. Бесцветная довольно вязкая жидкость со слабым специфическим "рыбным" запахом из-за наличия продукта разложения - диметиламина, в чистом виде практически без запаха.Содержание
Структура и свойства
Благодаря наличию двух резонансных форм в диметилформамиде порядок связи С=O уменьшен, а С-N увеличен. Так в инфракрасном спектре наблюдается понижение частоты карбонильной группы (1675 см-1) по сравнению с такой для свободной. Также благодаря частично двойному характеру связи азот-углерод, при комнатной температуре заторможено вращение вокруг неё в шкале времени ПМР. При этом наблюдается два сигнала(синглеты) метильной группы интенсивностью 3 протона δ 2.97 и 2.88, вместо одного синглета 6 протонов.
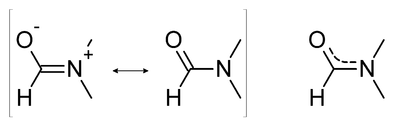 Две резонансные формы ДМФА
Две резонансные формы ДМФАДМФА смешивается с большинством органических раствориетелей за исключением углеводородов. Часто используемый растворитель для проведения химических реакций и очистки веществ перекристаллизацией, благодаря высокой растворяющей способности как для органических соединений так и частично для неорганических солей. ДМФА является полярным апротонным растворителем с высокой точкой кипения. Он способствует прохождению реакций с полярным механизмом, таких как SN2 реакций. Неустойчив к действию сильных кислот и оснований, что приводит к гидролизу, особенно при высоких температурах. Диэлектрическая проницаемость = 36,71
Получение
- по реакции между диметиламином и угарным газом в метаноле (100-150 °С, 2,5-20 МПа ) в присутствии CH3ONa или карбонилов металлов
- реакцией метилформиата с диметиламином (80-120 °С и 0,1-0,4 МПа)
- реакцией муравьиной кислоты с диметиламином
-
-
- HCOOH + HN(CH3)2 →(40 °C) HCOOH*HN(CH3)2 →(120 °C) (CH3)2NC(O)H + H2O
-
Очистка
Диметилформамид-сырец, содержащий незначительные количества влаги, диметиламина, формиата диметиламмония и монометилформамида, очищают вакуумной ректификацией.
Применение
ДМФА применяется
- как растворитель при производстве полиакрилонитрильного волокна (нитрона), и других полимеров
- для растворения красителей при крашении кожи, бумаги, древесины, вискозы и др.
- для абсорбции HCl, SO2 и других кислотных газов
- наряду с ацетонитрилом, является часто употребляемым растворителем в спектроскопии ЭПР
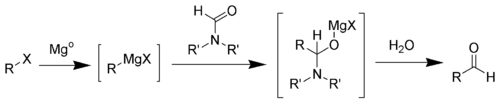
- для получения альдегидов по Вильсмаеру
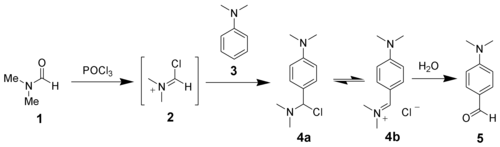
и Bouveault[1]
- для проведения спектроскопических исследований в ближней инфракрасной области
Безопасность
Реакция с использованием гидрида натрия в ДМФА отчасти опасна. Сообщалось об экзотермическом разложении выше 26 °С. В лабораторных условиях данная проблема решается использованием бань со льдом. В опытных производствах сообщалось о нескольких инцидентах при использовании данных реагентов.
Токсичность
Предполагается, что ДМФА является канцерогеном, также ему приписывают появление врождённых патологий. Женщины не допускаются для проведения процессов связанных с использованием ДМФА. Для проведения многих реакций он может быть заменён диметилсульфоксидом. Раздражает слизистые оболочки глаз. ПДК 10 мг/м3
Литература
1. Якушкин М. И., Котов В. И., в кн.: Справочник нефтехимика, под ред. С. К. Огородникова, т. 2, Л., 1978, с. 295-97
Ссылки
Wikimedia Foundation. 2010.
