- Надуксусная кислота
-
Надуксусная кислота 
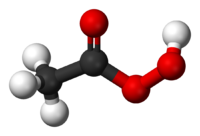
Общие Сокращения НУК Химическая формула СН3С(О)-О—ОН Эмпирическая формула С2Н4О3 Физические свойства Состояние (ст. усл.) бесцветная жидкость Молярная масса 76,05 г/моль Плотность 1,1037 г/см³ Термические свойства Температура плавления 0,1 °C Температура кипения 110 °C Энтальпия образования (ст. усл.) 340 кДж/моль Химические свойства pKa 8,2 Растворимость в воде смешивается Оптические свойства Показатель преломления 1,3964 Структура Дипольный момент 7,9 Д Классификация Рег. номер CAS 79-21-0 SMILES CC(=O)OO RTECS SD8750000 Надуксусная кислота (пероксиуксусная кислота, перуксусная кислота, НУК) — химическое соединение, органическая надкислота с формулой СН3СО3Н. Представляет собой бесцветную жидкость с резким запахом.
Содержание
Физические свойства
Бесцветная жидкость. Температура кипения 35-36 °C/29 мм рт. ст.. d204 1,1037; nD20 1,3964; DH0обр — 340 кДж/моль (25 °C), DH0исп 44,2 кДж/моль. Уравнение температурной зависимости пара lgp (мм рт. ст.) = 8,911 — 3211/T; m 7,9.10-30 Кл.м. Хорошо растворима в органических растворителях.
Получение
Надуксусная кислота СН3С(О)ООН образуется при воздействии концентрированного пероксида водорода на ледяную уксусную кислоту, константа равновесия при этом составляет 0,37.
Надуксусную кислоту получают постепенным добавлением уксусной кислоты и пероксида водорода в воду, содержащую серную кислоту в качестве катализатора. Полученную смесь выдерживают до десяти дней для увеличения выхода.[1]
Для получения НУК можно использовать также ацетилхлорид или уксусный ангидрид.
Перуксусная кислота продаётся в виде смеси с уксусной кислотой и пероксидом водорода для поддержания стабильности состава. Стабилизаторами также служат пирофосфат, триполифосфаты и тетраметапирофосфат натрия.
Другие методы получения НУК включают в себя окисление ацетальдегида, реакцией тетраацетилэтилендиамина[1] с щелочным водным раствором пероксида водорода.
Надуксусная кислота также образуется в природе в результате фотохимических реакций.
Концентрацию кислоты определяют чаще всего йодометрическим методом.
Химические свойства
Надуксусная кислота относится к группе сильных окислителей и довольно легко разрушается. Она, например, менее стабильная, чем перекись водорода. В разбавленных растворах надуксусная кислота разлагается за счет гидролитического расщепления на уксусную кислоту и перекись водорода:
Скорость этой реакции в большой степени зависит от температуры. Если при 40С период полураспада составляет несколько месяцев, то при 40 0С он сокращается до одной недели. Скорость разложения зависит также и от величины рН. При собственном рН 2,7 0,2%-ный раствор надуксусной кислоты стабилен в течение многих недель, тогда как при рН 5,7 период полураспада составляет менее одного дня. В присутствии тяжёлых металлов происходит другая реакция разложения:
Степень разложения по этому механизму зависит от вида и концентрации ионов тяжелого металла. Периоды полураспада могут длиться от нескольких часов до нескольких дней. Однако, при помощи комплексообразующих веществ можно в значительной степени предотвратить каталитическое действие ионов таких металлов.
Применение
Синтез других соединений
Основное применение надуксусной кислоты в промышленности - синтез эпоксидов. В этом процессе происходит перенос атома кислорода на двойную связь, например, этилен или пропилен образуют эпоксиды или спирты. Он может быть также использован при получении глицерина из пропилена. И используется в производстве нейлона[2].
Дезинфицирующие средства
Надуксусная кислота - сильное и удобное дезинфицирующее средство из-за высокого окислительного потенциала. Она эффективна против широкой гаммы микроорганизмов и не дезактивизируется ферментами каталазой и пероксидазой, дезактивирующими пероксид водорода. Она также легко разрушается в пище в безопасные остатки(уксусная кислота и пероксид водорода). Она может быть использована в широком интервале температур (0-40 °C), и широком значении рН (3.0-7.5), для мытья в жесткой воде.
Механизм действия
Пероксиуксная кислота убивает микроорганизмы, окисляя и впоследствии разрушая мембрану клетки, через гидроксил (HO•). Если диффузия гидроксила медленнее чем период его полураспада, то он реагирует с любой способной окисляться частицей. Он может разрушить практически любую макромолекулу связанной с микроорганизмом: углеводы, нуклеиновые кислоты (мутация), липиды и аминокислоты (фенилаланин переводит в м- и о-тирозин ). Это немедленно ведёт к распаду клетки и её гибели.
Применение
В США агентство по защите окружающей среды зарегистрировала перуксусную кислоту в качестве противомикробного средства в 1985 г. для применения в жилых помещениях на твёрдых поверхностей. Места применения включают агрокультурные площади, местах общего питания, медицинское оборудование и домашние ванные.
Надуксусная кислота также зарегистрирована для использования на маслобойнях и заводах по производству сыра, на технологическом оборудовании по производству продуктов питания. Ещё как пастеризатор на пивоваренных и винных заводах.[3]
Она также используется для дезинфекции медицинского снабжения, для предотвращения образования биоплёнок в мясном производстве, и как очиститель воды и дезинфицирующее средство.
Отбеливающее средство
Надуксусная кислота может использоваться как отбеливающее средство, особенно для пульпы при производстве бумаги. Она используется в слабокислой среде и при относительно низкой температуре. Она достаточно активна и как селективный отбеливающий агент, и очень часто используется как альтернатива диоксиду хлора или хлору в полностью бесхлорном отбеливании. Но это однако более дорого, и возникает вопрос хранения из-за её неустойчивости и химической активности. Это ограничивает её применение.
Безопасность
Концентрированные растворы надуксусной кислоты пожароопасны.
Кроме того, надуксусная кислота считается взрывоопасной. Однако показали, что эта взрывоопасность объясняется главным образом присутствием диацетилпероксида, который образуется при определенных способах получения надкислот. Когда её получают из смеси ледяной кислоты, пероксида водорода и соответствующих катализаторов, то образования диацетилпероксида не происходит, а опасность в обращении с концентрированной надуксусной кислотой уменьшается.
Примечания
- ↑ 1 2 United States Department of Agriculture. Agriculture Marketing Service Peracetic acid. (PDF document). URL accessed on 11 November 2006.
- ↑ KEMI - Information on Substances. Peracetic Acid. URL accessed on 11 November 2006.
- ↑ U.S. Environmental Protection Agency. Hydrogen Peroxide and Peroxyacetic Acid. URL accessed on 11 November 2006.
Литература
- Кнунянц И. Л. и др. т.3 Мед-Пол // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1992. — 639 с. — 50 000 экз. — ISBN 5-85270-039-8
См. также
- Надкислота

Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Категории:- Надкислоты
- Органические пероксиды
-
Wikimedia Foundation. 2010.



