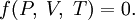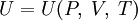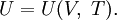- Уравнения состояния
-
Уравнение состояния 
Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван-дер-Ваальса Уравнение Дитеричи Разделы термодинамики Начала термодинамики Уравнение состояния Термодинамические величины Термодинамические потенциалы Термодинамические циклы Фазовые переходы править Уравне́ние состоя́ния — уравнение, связывающее между собой термодинамические (макроскопические) параметры системы, такие, как температура, давление, объём, химический потенциал и др. Уравнение состояния можно написать всегда, когда можно применять термодинамическое описание явлений. При этом реальные уравнения состояний реальных веществ могут быть крайне сложными.
Уравнение состояния системы не содержится в постулатах термодинамики и не может быть выведено из неё. Оно должно быть взято со стороны (из опыта или из модели, созданной в рамках статистической физики). Термодинамика же не рассматривает вопросы внутреннего устройства вещества.
Заметим, что соотношения, задаваемые уравнением состояния, справедливы только для состояний термодинамического равновесия.
Содержание
Виды уравнений состояния
Термическое уравнение состояния
Термическое уравнение состояния связывает макроскопические параметры системы. Для системы с постоянным числом частиц его общий вид можно записать так:
То есть, задать термическое уравнение состояния значит конкретизировать вид функции f.
Калорическое уравнение состояния
Калорическое уравнение состояния показывает, как внутренняя энергия выражается через давление, объем и температуру. Для системы с постоянным числом частиц оно выглядит так:
или, учитывая, что давление можно выразить из термического уравнения:
Каноническое уравнение состояния
Основная статья: Термодинамические потенциалы.
Каноническое уравнение представляет собой выражение для одного из термодинамических потенциалов (внутренней энергии, энтальпии, свободной энергии или потенциала Гиббса) через независимые переменные, относительно которых записывается его полный дифференциал.
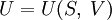 (для внутренней энергии),
(для внутренней энергии),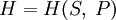 (для энтальпии),
(для энтальпии),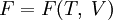 (для свободной энергии),
(для свободной энергии),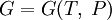 (для потенциала Гиббса).
(для потенциала Гиббса).
Каноническое уравнение, независимо от того, в каком из этих четырех видов оно представлено, содержит полную информацию о термических и калорических свойствах термодинамической системы.
См. также
- Термодинамическое равновесие
- Закон соответственных состояний
- Уравнение состояния идеального газа
- Уравнение Ван-дер-Ваальса
- Уравнение Дитеричи
Литература
- Базаров И. П. Термодинамика. — М.: Высшая школа, 1991. — 376 с.
- Базаров И. П. Заблуждения и ошибки в термодинамике. — Изд. 2-ое, испр. — М.: Едиториал УРСС, 2003. — 120 с.
- Квасников И. А. Термодинамика и статистическая физика. Т.1: Теория равновесных систем: Термодинамика. Том 1. — Изд. 2-ое, испр. и доп. — М.: УРСС, 2002. — 240 с.
- Сивухин Д. В. Общий курс физики. — М.: Наука, 1975. — Т. II. Термодинамика и молекулярная физика. — 519 с.
Термодинамические состояния вещества Физика: Твёрдое тело • Жидкость • Газ • Плазма Твёрдое тело Жидкость Жидкости • Ртуть • Электролиты • Расплавы Газ Газы • Пар Плазма Кварк-глюонная плазма Переходные точки Термодинамические фазы
квантовой жидкостиДисперсные системы Истинный раствор • Коллоид • Грубодисперсная система • Свободнодисперсная коллоидная система (дым, золь)
См. также Сверхкритическая жидкость • Вырожденное вещество • Конденсат Ферми — Дирака • Конденсат Бозе — Эйнштейна • Странная материя • Уравнение состояния • Кривая охлаждения • Квантовая жидкость • Термодинамическая фаза • Фазовый переход • Теория катастроф • Твёрдый гелий
Wikimedia Foundation. 2010.