- Оксигемоглобин
-
 Молекула гемоглобина: 4 субъединицы глобина окрашены в разные цвета
Молекула гемоглобина: 4 субъединицы глобина окрашены в разные цвета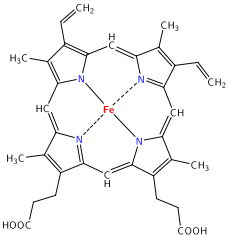 Гем группа
Гем группаГемоглоби́н (от др.-греч. αἷμα — кровь и лат. globus — шар) — сложный железосодержащий белок эритроцитов животных и человека, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани.
Главная функция гемоглобина состоит в транспорте дыхательных газов. В капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало, здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких. Монооксид углерода (CO) связывается с гемоглобином крови прочнее, чем кислород, образуя карбоксигемоглобин (HbCO). Некоторые процессы приводят к окислению иона железа в геме до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от мета… и гемоглобин, иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода. Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в легких.
Нормальным содержанием гемоглобина в крови человека считается: у мужчин 130—170 г/л, у женщин 120—150 г/л; у детей — 120—140 г/л.
Содержание
Строение
Гемоглобин является сложным белком класса хромопротеинов, то есть в качестве простетической группы здесь выступает особая пигментная группа, содержащая химический элемент железо — гем. Гемоглобин является тетрамером, то есть состоит из четырёх субъединиц. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами A-H (От N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Эта простетическая группа нековалентно связана с гидрофобной впадиной молекул гемоглобина и миоглобина. Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две других координационных позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93 положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64 положении цепи (участок E). Всего в гемоглобине четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в легких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь.На эту же связь присоединяется и моноксид углерода, вступая с кислородом в конкурентную борьбу за связь с гемоглобином,образуя карбоксигемоглобин.Связь моноксида углерода с гемоглобином более прочная, чем с кислородом.Поэтому часть гемоглобина,образующая комплекс с моноксидом углерода не участвует в транспорте кислорода.В норме у человека образуется 1,2% карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология
Гемоглобин является одним из основных белков, которыми питаются плазмодии малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение аномалиям относится серповидно-клеточная анемия. Однако, к несчастью, эти аномалии, как и аномалии строения гемоглобина не имеющие явно приспособительного значения, сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высоко токсичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезенкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин, специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других желчных пигментов, или выпускается в рециркуляцию в комплексе с трансферрином для повторного использования костным мозгом в процессе эритропоэза.
Смотри также
- Гемоглобин С (мутантная форма)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (эмбриональный гемоглобин)
Литература
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.), Addison Wesley Longman, ISBN 0-8053-3066-6.
- Levitt, M & C Chothia (June 17, 1976), "Structural patterns in globular proteins", Nature. doi 10.1038/261552a0.
Ссылки
Кровь Состав крови Плазма крови · Эритроциты · Тромбоциты · Лейкоциты: Гранулоциты (Нейтрофилы, Эозинофилы, Базофилы) и Агранулоциты (Лимфоциты, Моноциты) Остальное Кроветворение · Сыворотка крови · Группы крови · Заболевания крови · Костный мозг
Wikimedia Foundation. 2010.
