- Перхлорат натрия
-
Перхлорат натрия 
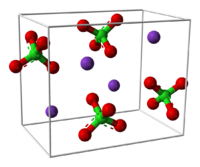
Общие Систематическое наименование Перхлорат натрия Сокращения ПХН Химическая формула NaClO4 Физические свойства Отн. молек. масса 122.45 а. е. м. Термические свойства Перхлорат натрия — химическое соединение NaClO4, натриевая соль хлорной кислоты. Сильный окислитель. Часто используется аббревиатура ПХН. При кристаллизации из водных растворов при температурах выше 51 градуса Цельсия выпадает безводная соль, ниже 51 градуса Цельсия моногидрат NaClO4*H2O, ниже -13 градусов — дигидрат. Как безводная соль, так и кристаллогидраты очень гигроскопичны, поэтому перхлорат натрия, в основном, используется, как сырьё для получения других перхлоратов обменными реакциями.
Содержание
Общие сведения
Бесцветное кристаллическое вещество. Молекулярная масса 122,45 а. е. м.. Очень хорошо растворим в воде - более 209,6 г на 100 г воды при 25 градусах Цельсия [1].
Химические свойства
Перхлорат натрия как окислитель может взаимодействовать с широким кругом горючих веществ, например, с глюкозой:
3 NaClO4 + C6H12O6 → 6 H2O + 6 CO2 + 3 NaCl
Получение
Перхлорат натрия может быть получен несколькими различными способами, в том числе:
1. Термическим диспропорционированием хлората натрия: 4 NaClO3 = 3 NaClO4 + NaCl (при 400-500 градусах Цельсия)
2. Электролитическим окислением хлората натрия на платиновом аноде.
3. Реакцией между хлорной кислотой и гидроксидом или карбонатом натрия.
В промышленности сейчас используется почти исключительно второй метод.
Применение
Ранее перхлорат натрия использовался, как гербицид. Даже небольшая его примесь в чилийской селитре вызывала гибель пшеницы и некоторых других культурных растений. Сейчас перхлорат натрия самостоятельного применения практически не находит, но его отличная растворимость в воде позволяет из него получать перхлораты любых металлов, аммония:
NaClO4 + NH4Cl = NH4ClO4 + NaCl
Кроме того, воздействуя на перхлорат натрия серной кислотой, можно получить свободную хлорную кислоту.
NaClO4 + H2SO4=HClO4 + NaHSO4
Токсичность
Сведения о токсичности перхлората натрия для животных противоречивы. В то же время, очевидно, что в силу большей стабильности тетраэдрического аниона перхлораты менее токсичны, чем хлораты, хлориты и гипохлориты. Однако, при попадении внутрь организма перхлорат натрия сильно нарушает натрий-калиевый баланс, так как перхлорат калия почти не растворим в воде (и в биологических жидкостях) при обычных температурах.
Примечания
 Категории:
Категории:- Соединения натрия
- Перхлораты
Wikimedia Foundation. 2010.
