- Бланфикс
-
Сульфат бария 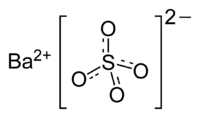
Общие Систематическое наименование Сульфат бария Химическая формула BaSO4 Отн. молек. масса 233.43 а. е. м. Физические свойства Плотность вещества 4.5 г/см³ Состояние (ст. усл.) твердый Термические свойства Температура плавления 1580 °C Химические свойства Растворимость в воде 0.000115 г/100 мл Классификация номер CAS 7727-43-7 Сульфа́т ба́рия (сернокислый барий) — сернокислая соль бария, BaSO4, белый порошок (или прозрачный кристалл), практически нерастворимое в воде (растворимость 0,0015 г/л при 18 °C) и других растворителях кристаллическое вещество. В природе встречается в виде минерала барита, который является основной бариевой рудой. Плотность 4,5 г/см³. Молекулярный вес 233,43 г/моль. Температура плавления 1580 °C. Коэффициент преломления − 1,63.
Содержание
Получение
- Взаимодействием солей, оксида, пероксида или гидроксида бария с серной кислотой или растворимыми сульфатами:
- BaCl2 + H2SO4 → BaSO4↓ + 2HCl
- Ba(NO3)2 + Na2SO4 → BaSO4↓ + 2NaNO3
- BaO2 + H2SO4 → BaSO4↓ + H2O2
- В промышленности большие объёмы сульфата бария получают из природного минерала тяжелого шпата, при этом исходное сырьё измельчается и отмучивается.
Химические свойства
- Сульфат бария не растворим в щелочах и большинстве кислот, однако растворим в хлорной воде, бромистоводородной и йодистоводородной кислотах, растворах гидрокарбонатов щелочных металлов[1]. Вступает во взаимодействие с концентрированной серной кислотой, которая переводит нерастворимый сульфат в хорошо растворимый гидросульфат бария:
- BaSO4 + H2SO4 → Ba(HSO4)2
- При прокаливании с углем или коксом сульфат восстанавливается до сульфида:
- BaSO4 + 2C → BaS + 2CO2
- При температуре свыше 1600°С разлагается:
- 2BaSO4 → 2BaO + 2SO2 + O2
Токсичность
Сульфат бария не является токсичным для организма веществом, в отличие от всех растворимых солей бария, и именно поэтому возможно его применение в качестве рентгеноконтрастного вещества. Однако, для некоторых бактерий, которые способны усваивать сульфаты, это вещество является смертельно опасным.
Применение
Аналитическая химия
В аналитической химии сульфат бария применяют как хорошую гравиметрическую форму для определения сульфат-ионов и ионов бария в гравиметрическом анализе.
Рентгеноконтрастное вещество
Часто используется при рентгеновских исследованиях желудочно-кишечного тракта как радиоконтрастное вещество, так как тяжёлые атомы бария хорошо поглощают рентгеновское излучение. Хотя все растворимые соли бария ядовиты, сульфат бария практически нерастворим в воде (и в растворе соляной кислоты, которая содержится в желудочном соке), поэтому он нетоксичен. Для рентгенографического исследования органов пищеварения пациент принимает внутрь суспензию сульфата бария ("бариевую кашу") BaSO4 (содержание Ba = 58,7%).
Пигмент-наполнитель
Сульфат бария является одной из составляющих часть смесей, используемых как белый краситель в рисовании.
- В смеси с оксидом цинка (ZnO) называется литопон.
- В смеси с сульфатом натрия (Na2SO4) - бланфикс (фр. Blanc fixe).
Употребляется как клеевая краска, так как не растворим в органических растворителях. Эти белила дешевле свинцовых, в отличие от них не токсичны и не темнеют от сернистого водорода.
Пиротехника
Сульфат бария используется как цветовой компонент для пиротехнических средств, так как ионы бария способствуют окрашиванию пламени в зеленый цвет. В настоящее время для этих целей в основном используют нитрат бария, за счет того, что он является сильным окислителем и способствует энергичному горению пиротехнической смеси.
Другие применения
Сульфат бария используется для различных промышленных целей:
- В качестве наполнителя для фото- и писчей бумаги, для линолеума и для некоторых лако-красочных материалов. См., например, баритаж.
- Как белый наполнитель для пластмасс, а также как компонент буровых растворов для увеличения их плотности.
- В электрохимической промышленности при изготовлении свинцовых аккумуляторов как расширитель активной массы отрицательного электрода.
- При производстве пасты для травления стекла.
- При производстве некоторых огнеупорных материалов.
Ссылки
Литература
- Учебник общей химии Некрасов Б.В. 1981 год, в 2 томах.
Примечания
- ↑ Н.С. Фрумина, Н.Н. Горюнова, С.Н. Еременко. Аналитическая химия бария. — Москва: Наука, 1977.
- Взаимодействием солей, оксида, пероксида или гидроксида бария с серной кислотой или растворимыми сульфатами:
Wikimedia Foundation. 2010.
