- Ферроцен
-
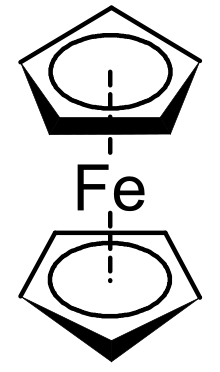
Ферроцен — одно из наиболее известных металлоорганических соединений, представитель класса сэндвичевых соединений (металлоценов). Номенклатурное название: бис-η5-циклопентадиенилжелезо(II) (η5-С5Н5)2Fe.
Оранжевые кристаллы; температура плавления 173 °C, температура кипения 249 °C; плотность 1,49 г/см³ (25 °C); устойчив до 470 °C; возгоняется при атмосферном давлении; растворим в органических растворителях, нерастворим в воде; устойчив к действию воздуха, горячей конц. соляной кислоте и растворам щелочей.
Содержание
Открытие
В 1951 году Т. Кили и П. Посон, провели реакцию C5H5MgBr c хлоридом железа FeCl2 с целью синтезировать новый углеводород — дициклопентадиенил. Неожиданно они получили совершенно новое, исключительно устойчивое жёлто-оранжевое кристаллическое соединение, содержащее железо. Потребовалось около года, чтобы понять, как оно построено. Было обнаружено, что атом железа расположен посередине между двумя симметричными пятичленными кольцами C5H5. Пятичленные кольца в молекуле свободно вращаются вокруг оси, соединяющей центры колец. Такой тип структуры получил название «сэндвичевый» (пятичленные кольца — куски хлеба, а атом железа — начинка). Из-за сходства реакционной способности с бензолом, новое соединение было названо «ферроцен» (звуковая аналогия очевидна в английском языке: benzene — ferrocene). Структура ферроцена была установлена в 1952 году Р. Вудвордом и Дж. Уилкинсоном на основании его реакционной способности, и независимо от них — Э. Фишером на основании рентгеноструктурных данных.
Свойства
Многими исследователями было показано, что по общему характеру реакционной способности ферроцен напоминает бензол; это привело к тому, что очень скоро после открытия ферроцен был назван небензоидной ароматической системой. Для него характерны три типа химических превращений: замещение водорода в С5Н5-кольцах без разрыва связей Fe—С, окисление по атому Fe и разрыв связи Fe—C.
Реакции электрофильного замещения для ферроцена протекают легче, чем для бензола; при этом образуются как моно-, так и гетероаннулярные (содержащие заместители в разных циклах) дизамещённые производные.
Ферроцен легко и обратимо окисляется до катион-радикала ферроцения (кислородом воздуха в кислой среде, перекисью водорода, иодом, хлоридом железа(III) и т. п.). При окислении не происходит заметных изменений в геометрии молекулы ферроцена. Разбавленные растворы солей ферроцения окрашены в синий цвет, концентрированные — в красный.
Связь Fe—С в ферроцене мало реакционноспособна и разрывается только при действии очень сильных восстановителей: водорода в присутствии катализатора (никель Ренея) (300 °C, 2.5 МПа) либо растворов щелочных металлов в жидком аммиаке или аминах. При взаимодействии ферроцена с аренами в присутствии AlCl3/Al одно кольцо замещается на арен и образуется катион [Fе(С5Н5)(арен)]+.
Получение
- Реакция хлорида железа и реактивом Гриньяра:
- Реакция циклопентадиена с пентакарбонилом железа:
- Реакция циклопентадиена с хлоридом железа и диэтиламином:
Применение
Ферроцен используется в нефтяной промышленности в качестве антидетонатора. Применяется как термостабилизатор полиэтилена и диеновых каучуков (например, бутадиеновых); используется в синтезе некоторых медицинских препаратов.
Литература
- Фишер Э., Вернер Г. «π-комплексы металлов», М.: Мир, 1968.
- Посон П. «Химия металлоорганических соединений», М.: Мир, 1970.
- Губин С. П., Шульпин Г. Б. «Химия комплексов со связями металл — углерод», Новосибирск, Наука, 1984.
Ссылки
Соединения железаАрсениды железа • Бромид железа(II) (FeBr2) • Бромид железа(II,III) (Fe3Br8) • Бромид железа(III) (FeBr3) • Гексацианоферрат(II) калия (K4[Fe(CN)6]) • Гексацианоферрат(III) калия (K3[Fe(CN)6]) • Гидроксид железа(II) (Fe(OH)2) • Гидроксид железа(III) (Fe(OH)3) • Динитрозилдикарбонилжелезо (Fe(CO)2(NO)2) • Диоксоферрат(III) натрия (NaFeO2) • Дисульфид(2-) железа(II) (Fe(S2)) • Додекакарбонилтрижелезо (Fe3(CO)12) • Железистосинеродистая кислота (H4[Fe(CN)6]) • Железосинеродистая кислота (H3[Fe(CN)6]) • Иодид железа(II) (FeI2) • Иодид железа(II,III) (Fe3I8) • Карбиды железа • Карбонат железа(II) (FeCO3) • Метагидроксид железа (FeO(OH)) • Нитрат железа(II) (Fe(NO3)2) • Нитрат железа(III) (Fe(NO3)3) • Нитрид дижелеза (Fe2N) • Нитрид тетражелеза (Fe4N) • Нитропруссид калия (K2[Fe(CN)5NO]) • Нитропруссид натрия (Na2[Fe(CN)5NO]) • Нонакарбонилдижелезо (Fe2(CO)9) • Оксалат железа(II) (FeC2O4) • Оксалат железа(III) (Fe2(C2O4)3) • Оксид железа(II) (FeO) • Оксид железа(III) Fe2O3 • Оксид железа(II,III) (Fe3O4) • Оксид железа(III) (Fe2O3) • Оксихлорид железа FeOCl • Олеат железа(III) ((C17H33COO)3Fe) • Пентакарбонилжелезо (Fe(CO)5) • Резинат железа(III) ((C19H29COO)3Fe) • Соль Мора (FeSO4·(NH4)2SO4·6H2O) • Сульфат железа(II) (FeSO4) • Сульфат железа(III) (Fe2(SO4)3) • Сульфат железа(III)-калия (KFe(SO4)2) • Сульфид железа(II) (FeS) • Сульфид железа(II,III) (Fe3S4) • Сульфид железа(III) (Fe2S3) • Тартрат железа(II) (C4H4FeO6) • Тетракарбонилдигидриджелезо (H2Fe(CO)4) • Тетракарбонилжелезо (Fe(CO)4) • Тетранитрозил железа (Fe(NO)4) • Тиоцианат железа(II) (Fe(SCN)2) • Тиоцианат железа(III) (Fe(SCN)3) • Титанат железа(II) (FeTiO3) • Феррат калия (K2FeO4) • Фосфат железа(II) (Fe3(PO4)2) • Фосфат железа(II,III) (Fe4(PO4)3) • Фосфат железа(III) (FePO4) • Фосфиды железа • Фторид железа(II) (FeF2) • Фторид железа(III) (FeF3) • Хлорид железа(II) (FeCl2) • Хлорид железа(II,III) (Fe3Cl8) • Хлорид железа(III) (FeCl3) • Хромат железа(III) (Fe2(CrO4)3) • Хромит железа(II) (Fe(CrO2)2) Цианид железа(II) (Fe(CN)2)
Категории:- Соединения железа
- Комплексные соединения
- Металлоорганические соединения
- Элементоорганические соединения
- Металлоцены
- Антидетонаторы
Wikimedia Foundation. 2010.




![\mathsf{Fe(CO)_5 + C_5H_6 \ \xrightarrow[-CO, -H_2]{200^oC}\ Fe(C_5H_5)(CO)_2 \ \xrightarrow[-Fe_3(CO)_{12}]{T}\ Fe(C_5H_5)_2 }](3de203776f0f207b022ffda75a8c0b21.png)
