- Изоцианаты
-
Изоцианаты — органические соединения, содержащие функциональную группу —N=C=O[1].
Содержание
Свойства
Изоцианаты, будучи гетерокумуленами, являются активными электрофилами. При взаимодействии с первичными и вторичными аминами образуют замещённые мочевины, со спиртами — карбаматы (уретаны), гидролизуются водой до аминов и углекислоты.
Восстановление изоцианатов алюмогидридом лития ведёт к метиламинам:
- RNCO + [H]
 RNHCH3
RNHCH3
1,2-циклоприсоединение изоцианатов к алкенам используется для синтеза напряжённых N-замещённых бета-лактамов, являющихся, в частности, структурным фрагментом антибиотиков пенициллинового ряда. Для получения незамещённых лактамов применяется N-хлорсульфонилизоцианат, способный присоединяться даже к простейшим незамещённым алкенам и лёгкости удаления хлорсульфонильной группы. В реакции с 1,3-диенами N-хлорсульфонилизоцианат способен образовывать и продукты 1,4-циклоприсоединения.
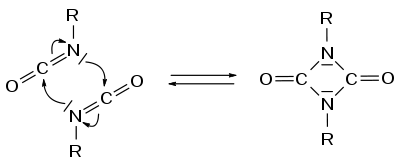
Изоцианаты способны к димеризации с образованием уретдионов (1,2-азетидин-2,4-дионов), реакция катализируется триалкилфосфинами и, с меньшей эффективностью, третичными аминами (например, пиридином). Реакция обратима, при нагреве уретдионы разлагаются с образованием исходных изоцианатов:
Изоцианаты также могут тримеризоваться с образованием три-N-замещенных циануровых кислот. Эта реакция катализируется слабыми основаниями (ацетатом калия, триэтиламином и т. п.).
Взаимодействие иминофосфоранов с изоцианатами по типу реакции Виттига является одним из методов синтеза карбодиимидов:
- R-N=PPh3 + R'-NCO
 R'-N=C=N-R + Ph3P=O
R'-N=C=N-R + Ph3P=O
Синтез
Наиболее распространённый метод синтеза изоцианатов — реакция аминов с фосгеном (фосгенирование аминов), реакция идёт в среде инертного растворителя через промежуточное образование карбамоилхлоридов:
- RNH2 + COCl2
 RNHCOCl + HCl
RNHCOCl + HCl - RNHCOCl
 RNCO + HCl
RNCO + HCl
Этот метод является и основным промышленным методом синтеза изоцианатов.
В случае синтеза промышленно важных диизоцианатов, использующихся в производстве полиуретанов (толуилендиизоцианат, дифенилметандиизоцианат) фосгенирование ведут в две стадии:
- Синтез моноизоцианата фосгенированием диамина при относительно низкой температуре (холодное фосгенирование):
- H2N-R-NH2 + COCl2
 OCN-R-NH2•HCl
OCN-R-NH2•HCl
- H2N-R-NH2 + COCl2
- Синтез диизоцианата фосгенированием гидрохлорида аминоизоцианата при относительно высокой температуре (горячее фосгенирование):
- OCN-R-NH2•HCl + COCl2
 OCN-R-NCO + 2HCl
OCN-R-NCO + 2HCl
- OCN-R-NH2•HCl + COCl2
Другой метод синтеза изоцианатов, использующийся в промышленности — термическое разложение карбаматов:
- R'NHCOOR
 R'NCO + ROH
R'NCO + ROH
Карбаматы, в свою очередь, могут быть получены реакцией соответствующего амина с мочевиной и спиртом:
- R'NH2 + NH2CONH2 + ROH
 R'NHCOOR + 2NH3
R'NHCOOR + 2NH3
Такой «бесфосгенный» метод в промышленности используется для синтеза алифатических изоцианатов, в частности, гексаметилендиизоцианата.
В лабораторной практике вместо газообразного и опасного в обращении фосгена может быть использован оксалилхлорид: он реагирует с аминами и амидами с образованием соответствующих изоцианатов, отщепляя окись углерода:
- RNH2 + (COCl)2
 RNCO + CO + 2 HCl
RNCO + CO + 2 HCl
Таким образом могут быть синтезированы как ацилизоцианаты[2], так и сульфонилизоцианаты.
Изоцианаты, гидролизующиеся in situ до аминов, также образуются в качестве промежуточных продуктов в перегруппировках Гофмана, Курциуса и Лоссена и могут быть выделены при проведении реакции в инертных растворителях:
- RCONH2 + Hal2
 RCONHHal
RCONHHal  RCNO + HHal (Реакция Гофмана)
RCNO + HHal (Реакция Гофмана) - RCOCl + NaN3
 RCN3
RCN3  RCNO + N2 (Реакция Курциуса)
RCNO + N2 (Реакция Курциуса) - RCONHOR' + OH−
 R'CNO + RCOO− (Реакция Лоссена)
R'CNO + RCOO− (Реакция Лоссена)
Изоцианиты также могут быть синтезированы присоединением изоциановой кислоты к алкенам, легче всего реагируют алкены с терминальной двойной связью и электрондонорным заместителем при двойной связи, например, виниловые эфиры:
- RO-CH=CH2 + HNCO
 RO-CH(CH3)-N=C=O
RO-CH(CH3)-N=C=O
Аналогично с изоциановой кислотой реагируют и стирол и его гомологи, изопрен и другие алкены, проведение реакции с неактивированными электрондонорными заместителями алкенами идет в более жестких условиях и под действием катализаторов (эфират трифторида бора, p-толуолсульфокислота)[3].
Изонитрилы окисляются до изоцианатов под действием разнообразных окислителей — диметилсульфоксида[4], оксида ртути(II) и т. д.:
- R—N≡C + [O]
 RN=C=О
RN=C=О
Применение
Основное промышленное применение изоцианатов — использование их в сочетании с многоатомными спиртами для дальнейшего синтеза полиуретанов. Метилизоцианат используется в синтезе пестицидов.
4,4-Метилендифенилдиизоцианат (MDI)Объем мирового рынка изоцианатов в 2000 году составлял 4,4 миллиона тонн, из которых 61,3 % приходилось на метилендифенилдиизоцианат (МДИ), 34,1 % на толуилендиизоцианат (ТДИ), 3,4 % на гескаметилендиизоцианат (ГДИ) и 1,2 % на изофоронилдиизоцианат (ИФДИ).
См. также
Литература
- Общая органическая химия /Под ред. Д. Бартона и У. Д Уиллиса/. Том 3. Азотсодержащие соединения. «Химия», М. 1982.
Примечания
- ↑ John Speziale, Lowell R. Smith. α-Chloroacetyl isocyanate. Organic Syntheses, Coll. Vol. 5, p.204 (1973); Vol. 46, p.16 (1966).
- ↑ Katritzky Alan R. Comprehensive Organic Functional Group Transformations: Synthesis: carbon with two attached heteroatoms with at least one carbon-to-heteroatom multiple link. — Elsevier. — ISBN 9780080423265 (pp. 985—986)
- ↑ Martin, D.; A. Weise (1967-02-01). «Acid‐Catalysed Oxidation of Isocyanides with Dimethyl Sulfoxide». Angewandte Chemie International Edition in English 6 (2): 168-169. DOI:10.1002/anie.196701682. ISSN 1521-3773. Проверено 2011-05-19.
 Категории:
Категории:- Изоцианаты
- Терминология IUPAC
- RNCO + [H]
Wikimedia Foundation. 2010.