- Хинолин
-
Хинолин 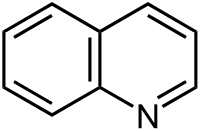
Общие Химическая формула C9H7N Физические свойства Молярная масса 129.16 г/моль Плотность 1.093 г/см³ Термические свойства Температура плавления -15 °C Температура кипения 238 °C Классификация Рег. номер CAS 91-22-5 SMILES c1cccc2cccnc12 Хинолин — органическое соединение гетероциклического ряда. Применяют как растворитель для серы, фосфора и др., для синтеза органических красителей. Производные хинолина, используют в медицине (плазмоцид, хинин).
Содержание
Промышленное получение
Хинолин встречается в составе каменноугольной смолы, из которой и добывается.
Методы синтеза
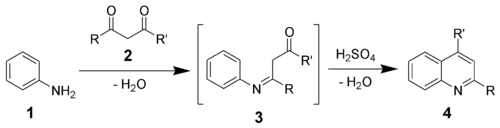
- Производные хинолина с заместителями в положениях 2 и 4 можно получить путем конденсации анилина (1) и β-дикетонов (2) в кислой среде. Этот метод получил название «синтез хинолинов по Комба»
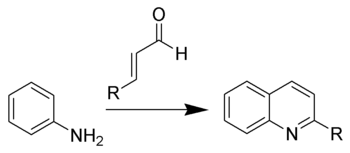
- Из анилина и α,β-ненасыщеных альдегидов (метод Дёбнера-Миллера). Механизм данной реакции очень близок к механизму реакции Скраупа
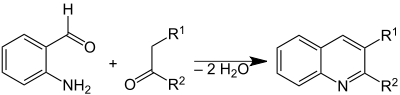
- Из 2-аминобензальдегида и карбонильных соединений, содержащих α-метиленовую группу (синтез Фридлендера). Метод практически не употребляется из-за низкой доступности о-карбонильных производных анилина
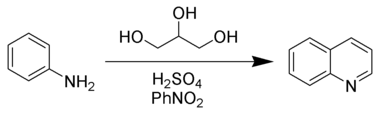
- Конденсацией анилина и глицерина в присутствии серной кислоты (метод Скраупа)
Механизм этой реакции точно не установлен, но предполагают, что процесс идет как 1,4-присоединение анилина к акролеину. Акролеин образуется в результате дегидратации глицерина в присутствии серной кислоты (образование акролена подтверждено: из готового акролеина и анилина также образуется хинолин.

Реакция сильно экзотермична, поэтому процесс обычно проводят в присутствии сульфата железа (II). В качестве окислителя используют также оксид мышьяка (V), в этом случае процесс протекает не так бурно,как с нитробензолом и выход хинолина выше.
- По реакции Поварова из бензальдегида, анилина и алкена.
- Из орто-ацилацетофенона и гидроксида (en:Camps quinoline synthesis).
- Из β-кетоанилида (en:Knorr quinoline synthesis).
- Из анилина и β-кетоэфиров[1] (en:Conrad-Limpach synthesis).
- en:Gould-Jacobs reaction
Токсикология и безопасность
LD50 для млекопитающих составляет несколько сотен мг/кг.
Примечания
- ↑ Reynolds, G. A.; Hauser, C. R. Org. Syn., Coll. Vol. 3, p.593 (1955); Vol. 29, p.70 (1949).
Азотистые гетероциклы Трехчленные Азирин · Азиридин Четырехчленные Азетидин · Азетидинон(β-лактам) Пятичленные Пиррол · Пирролины · Пирролидин · Пиразол · Имидазол · Триазолы · Тетразол · Пентазол · Пирролидон(γ-лактам) · Индол Шестичленные Акридин · Изохинолин · Пиперидин · Пиперидон(δ-лактам) · Пиридин · Пиримидин · Хинолизидин · Хинолин Семичленные Капролактам(ε-лактам) Высшие Порфин · Фталоцианины · Коррин Основные типы алкалоидов Пирролидин Гигрин Тропан Атропин • Гиосциамин • Скополамин • Кокаин • Экгонин Пиперидин Кониин • Лобелин • Пиперин Хинолизидин Цитизин • Пахикарпин Пиридин Никотин • Анабазин Изохинолин Морфин • Кодеин • Тебаин • Папаверин • Ликорин Хинолин Хинин • Хинидин • Эхинопсин Индол Серотонин • Псилоцин • Псилоцибин • ДМТ • 4-HO-MET • 5-MeO-DMT • Буфотенин • Гармин • Гармалин • Физостигмин • Эрготамин • Эргометрин • Иохимбин • Резерпин • Митрагинин • Ибогаин • Стрихнин • Бруцин Пурин Ксантины (Кофеин • Теобромин • Теофиллин) • Сакситоксин Фенилэтиламин Катехоламины (Норадреналин • Адреналин • Дофамин) • Эфедрин • Псевдоэфедрин • Норэфедрин • Катин • Катинон • Мескалин Терпены Аконитин • Дельфинин • Элатин Другие Пилокарпин • Мускарин • Колхицин • Галантамин • Капсаицин 
Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Категории:- Алкалоиды
- Растворители
- Хинолины
- Ароматические основания
Wikimedia Foundation. 2010.