- Индол
-
Индол 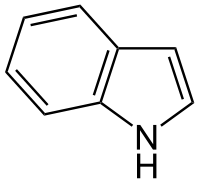
Общие Систематическое наименование 1-H-indole Химическая формула C8H7N Отн. молек. масса 117,15 а. е. м. Физические свойства Состояние (ст. усл.) кристалл Плотность 1,22 г/см³ Термические свойства Температура плавления 52,5 °C Температура кипения 254 °C Классификация Рег. номер CAS 120-72-9 SMILES C1(NC=C2)=C2C=CC=C1 Индол (бенз[b]пиррол) — бесцветные кристаллы с запахом, напоминающим нафталин. Является родоначальником широкого класса природных соединений. Содержится в каменноугольной смоле, в некоторых эфирных маслах (например, в масле жасмина).
Содержание
Физические свойства
Внешний вид: бесцветн. листовидные кристаллы Брутто-формула (система Хилла): C8H7N Молекулярная масса (в а. е. м.): 117,15 Бесцветное кристаллическое вещество с запахом нафталина, растворимое в горячей воде; температура плавления 52 °C.Температура кипения (в °C): 254 Растворимость (в г/100 г или характеристика):
- бензол: растворим
- вода: растворим (100 °C)
- диэтиловый эфир: легко растворим
- лигроин: растворим
- этанол: легко растворим
Химические свойства
Индол — слабое основание (рH —2,4). При протонировании образует катион 3H-индолия (ф-ла I), который при взаимодеиствии с нейтральной молекулой индол дает димер (II). Как слабая кислота (рН 17), индол с Na в жидком NH3 образует N-натрийиндол, с КОН при 130 °C — N-калийиндол. Обладает ароматич. св-вами. Электроф. замещение идет гл. обр. в положение 3. Нитрование обычно осуществляется бензоилнитратом, сульфирование — пиридинсульфотриоксидом, бромирование — диоксандибромидом, хлорирование — SO2Cl2, алкилирование — активными алкилгалогенидами. Ацетилирование в уксусной к-те также идет в положение 3, в присут. CH3COONa — в положение 1; в уксусном ангидриде образуется 1,3-диацетилиндол. Индол легко присоединяется по двойной связи a, b-непредельных кетонов и нитрилов. Аминометилирование (р-ция Манниха) в мягких условиях протекает в положение 1, в жестких — в положение 3. Замещение в бензольное кольцо (преим. в положения 4 и 6) идет лишь в кислых средах при блокированном положении 3. В присут. Н2О2, надкислот или на свету индол окисляется в индоксил, к-рый затем превращ. в тример или индиго. Более жесткое окисление под действием О3, MnO2 приводит к разрыву пиррольного кольца с образованием 2-формамидобензальдегида. При гидрировании индола водородом в мягких условиях восстанавливается пиррольное кольцо, в более жестких — и бензольное.
Индол содержится в эфирных маслах жасмина и цитрусовых, входит в состав кам.-уг. смолы. Кольцо индола — фрагмент молекул важных прир. соединений (напр., триптофана, серотонина, мелатонина, буфотенина). Обычно индол выделяют из нафталиновой фракции кам.-уг. смолы или получают дегидрированием о-этиланилина с послед. циклизацией образующегося продукта. Индол и его производные синтезируют также циклизацией арилгидразонов карбонильных соед. (р-ция Фишера), взаимод. ариламинов с a-галоген- или a-гидроксикарбонильными соед. (р-ция Бишлера) и др. Ядро индола входит в состав индольных алкалоидов. Сам индол-фиксатор запаха в парфюмерии; его производные используют в произ-ве биологически активных соед. (гормонов, галюциногенов) и лек. ср-в (напр., индопана, индометацина).
Ядро индола является R-группой одной из 20 кодируемых аминокислот — триптофана, и поэтому присутствует практически в любом белке.
Применение
Индол служит исходным сырьем для синтеза гетероауксина, триптофана, используется в парфюмерной и фармацевтической промышленности.
Многие алкалоиды содержат ядро индола.
Получение
Для получения И. пользуются: сухой перегонкой бариевой соли оксалортотолуидиновой кислоты CH 3C6H4 NH-CO-COHO (Mauthner u. Suida); пропусканием паров кумидина (ортоамидоизопропилбензола — C 3H7-C6H4-NH2) через накаленную фарфоровую трубку, наполненную окисью свинца (Tileti, 1883), нагреванием при 210° — 230° продукта реакции получаемого кипячением дихлороэфира С 2H8 Cl 2 О с анилином и водой и остающегося после отгонки избытка анилина и воды (Berlinerblau, 1887). Для извлечения И. из сырых продуктов реакции его отгоняют с водяным паром и очищают кристаллизацией. И. кристаллизуется из воды в мелких листочках, из лигроина в крупных с атласным блеском, плавится при 52° и кипит, отчасти разлагаясь, при 245° — 246°; улетучивается и при обыкновенной температуре, распространяя долго не исчезающий фекальный запах, а также легко перегоняется с парами воды. Он легко растворим в спирте, эфире, углеводородах и в горячей воде. Свойства основания в И. развиты весьма слабо. Труднорастворимая хлористоводородная соль его хотя и образуется при действии крепкой соляной кислоты, но водой разлагается. Весьма характерно для И. образование пикрама C 8H7N-C6H2(NO2)3 OH, выделяющегося в виде длинных блестящих игл красного цвета при смешении бензольных растворов И. и пикриновой кислоты. Древесина (сосновая лучинка), смоченная спиртом и соляной кислотой, окрашивается И. в вишнево-красный цвет. Замещением атомов водорода И. образуются его гомологи и др. производные. При этом возможны многочисленные случаи изомерии, которые зависят не только от того, будут ли подвергаться замещению атомы водорода бензольного ядра, или пиррольного, или же водород группы NH, но и от положения замещаемых водородов и, разумеется, от изомерии самих замещающих групп. Синтетические способы получения гомологов разработаны, главным образом, Э. Фишером (1886) и состоят в отнятии частицы аммиака от гидразонов альдегидов и кетонов действием на них минеральных кислот при нагревании или сплавлением их с хлористым цинком. Гомологи И. представляют частью жидкости, частью кристаллические вещества. Неоднократно упоминавшийся выше скатол (β-метилиндол), напр., кристаллизуется в листочках, плавится при 95° и кипит при 265° — 266°. Запах, свойственный И., сохраняется и его гомологами, за исключением тех, у которых замещению подвергся водород группы NH. Вхождение фенильной (С 6H5) и карбоксильной (СООН) групп в состав частицы И. также уничтожает его запах. Гомологи И. водородом в момент выделения восстанавливаются в гидрооснования состава С nH2n-7 N, образуют, подобно И., соединения с пикриновой кислотой и дают, за исключением некот. гомологов, красное окрашивание с древесиной.
Основные типы алкалоидов Пирролидин Гигрин Тропан Атропин • Гиосциамин • Скополамин • Кокаин • Экгонин Пиперидин Кониин • Лобелин • Пиперин Хинолизидин Цитизин • Пахикарпин Пиридин Никотин • Анабазин Изохинолин Морфин • Кодеин • Тебаин • Папаверин • Ликорин Хинолин Хинин • Хинидин • Эхинопсин Индол Серотонин • Псилоцин • Псилоцибин • ДМТ • 4-HO-MET • 5-MeO-DMT • Буфотенин • Гармин • Гармалин • Физостигмин • Эрготамин • Эргометрин • Иохимбин • Резерпин • Митрагинин • Ибогаин • Стрихнин • Бруцин Пурин Ксантины (Кофеин • Теобромин • Теофиллин) • Сакситоксин Фенилэтиламин Катехоламины (Норадреналин • Адреналин • Дофамин) • Эфедрин • Псевдоэфедрин • Норэфедрин • Катин • Катинон • Мескалин Терпены Аконитин • Дельфинин • Элатин Другие Пилокарпин • Мускарин • Колхицин • Галантамин • Капсаицин Категории:- Алкалоиды
- Гетероциклические соединения
- Производные индола
Wikimedia Foundation. 2010.
