- Кремния диоксид
-
Диокси́д кре́мния (оксид кремния (IV), кремнезём, SiO2) — бесцветные кристаллы, tпл 1713—1728 °C, обладают высокой твёрдостью и прочностью.
Содержание
Свойства
- Относится к группе кислотных оксидов.
- При нагревании взаимодействует с основными оксидами и щелочами.
- Растворяется в плавиковой кислоте.
- SiO2 относится к группе стеклообразующих оксидов, то есть склонен к образованию переохлажденного расплава — стекла.
- Один из лучших диэлектриков (электрический ток не проводит).
Полиморфизм
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространенная из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии
При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше 573 °C обратимо переходит в β-кварц. При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях. При высоких температуре и давлении диоксид кремния сначала превращается в коэсит, а затем в стишовит (который впервые был обнаружен на месте эпицентра ядерного взрыва). Согласно некоторым исследованиям стишовит слагает значительную часть мантии, так что вопрос о том какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.
Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с плавиковой кислотой:
SiO2 + 6HF → H2[SiF6] + 2H2O,
и газообразным фтороводородом HF:
SiO2 + 4HF → SiF4↑ + 2H2O.
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xH2O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же).
Например, может быть получен ортосиликат натрия:
SiO2 + 4NaOH → (2Na2O)·SiO2 + 2H2O,
метасиликат кальция:
SiO2 + СаО → СаО·SiO2,
или смешанный силикат кальция и натрия:
Na2CO3 + CaCO3 + 6SiO2 → Na2O·CaO·6SiO2 + 2CO2↑.
Из силиката Na2O·CaO·6SiO2 изготовляют оконное стекло.
Следует отметить, что большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют растворимым стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
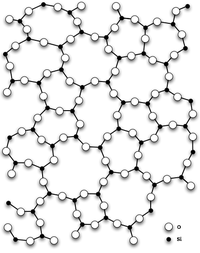
Главным структурным элементом как твердого диоксида кремния, так и всех силикатов выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырех атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры 400—500°C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2.
В лабораторный условиях синтетический диоксид кремния может быть получен действием кислот на силикатные соли. Например:
- Na2SiO3 + 2CH3COOH → 2CH3COONa+H2SiO3,
кремниевая кислота сразу разлагается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87% массы литосферы.
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (SiH4). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремневой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: до 320 м²/г.
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Wikimedia Foundation. 2010.