- Ацетоуксусный эфир
-
Ацетоуксусный эфир 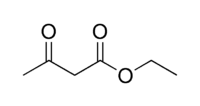
Общие Систематическое наименование Этил-3-оксобутират Традиционные названия Этилацетоуксусный эфир, этиловый эфир ацетоуксусной кислоты Эмпирическая формула C6H10O3 Физические свойства Состояние (ст. усл.) жидкость Молярная масса 130.14 г/моль Плотность 1.0284 г/см³ Термические свойства Температура плавления -45 °C Температура кипения 180.8 °C Химические свойства pKa 10.68 (в воде), 14.2 (в ДМСО) Оптические свойства Показатель преломления 1.4198 Классификация Рег. номер CAS 141-97-9 RTECS AK5250000 Ацетоуксусный эфир(этиловый эфир ацетоуксусной кислоты, этилацетоацетат) - бесцветная подвижная жидкость со своеобразным нерезким запахом. Растворяется в воде (14,3 % при 16,5 °C), смешивается с этанолом и диэтиловым эфиром.
Содержание
Свойства
Для ацетоуксусного эфира, как и для других 1,3-дикарбонильных соединений характерна кето-енольная таутомерия:
Енольный таутомер стабилизирован за счет образования внутримолекулярной водородной связи между протоном и соседним карбонильным кислородом. Положение равновесия и, соответственно, соотношение таутомеров зависит от растворителя и температуры. Так, в чистом ацетоуксусном эфире при комнатной температуре концентрация енольной формы составляет 7,5 %. Равновесие сдвигается в сторону енольной формы при уменьшении полярности растворителя, так, при 18 °C доля енольной формы в водном растворе составляет 0,4 %, в диэтиловом эфире — 27,1 %, в циклогексане — 46,4 %.
Кетонная форма ацетоуксусного эфира может быть выделена из равновесной смеси вымораживанием, енольная - вакуумной перегонкой в кварцевой посуде. Скорость установления кето-енольного равновесия зависит от температуры и материала сосуда, чистые таутомеры хранятся в кварцевой посуде при низких температурах (-80°C - охлаждение сухим льдом).
Содержание енольной формы определяется бромометрически: бром практически мгновенно присоединяется по двойной связи енола, что сопровождается исчезновением желто-оранжевой окраски молекулярного брома.
Реакциями енольной формы также обусловлено O-ацилирование ацетоуксусного эфира хлорангидридами карбоновых кислот в пиридине, при этом образуются сложные эфиры β-гидроксикротоновой кислоты:
- CH3(HO)C=CHCOOC2H5 + ROCl
 CH3(ROO)C=CHCOOC2H5 + HCl
CH3(ROO)C=CHCOOC2H5 + HCl
При взаимодействии с пентахлоридом фосфора гидроксил енольной формы ацетоуксусного эфира замещается на хлор с образованием этилового эфира β-хлоркротоновой кислоты:
- CH3(HO)C=CHCOOC2H5 + PCl5
 CH3ClC=CHCOOC2H5 + POCl3 + HCl
CH3ClC=CHCOOC2H5 + POCl3 + HCl
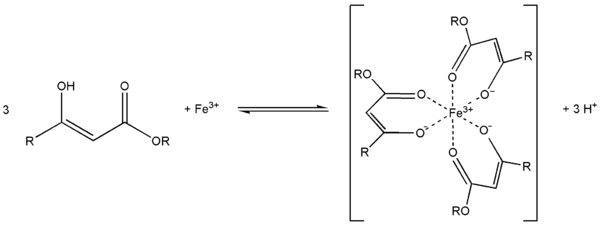
С металлами ацетоуксусный эфир образует хелаты, в которых ацетилацетат-анион выступает в роли бидентантного лиганда, так, с солями трехвалентного железа ацетоуксусный эфир образует окрашеный в пурпурный цвет комплекс:
Под действием сильных оснований и щелочных металлов ацетоуксусный эфир депротонируется с образованием резонансно стабилизированный аниона:
Образование натриевой соли ацетилацетата (натрийацетоуксусного эфира) под действием алкоголята натрия - в том числе и под действием этилата натрия, образующегося in situ при действии металлического натрия на ацетоуксусный эфир - широко используется в синтетической практике вследствие высокой нуклеофильности аниона.
Ацетилацетат натрия в реакциях с мягкими электрофилами выступает в роли C-нуклеофила. Так, он легко алкилируется галогеналкилами с образованием соответствующих алкилацетоуксусных эфиров, из которых, в свою очередь, могут быть получены и затем проалкилированы натриевые производные:
- CH3COCH2COOC2H5 + EtONa
 CH3COCH-COOC2H5 Na+ + EtOH
CH3COCH-COOC2H5 Na+ + EtOH - CH3COCH-COOC2H5 Na+ + RHal
 CH3COCHRCOOC2H5 + NaHal
CH3COCHRCOOC2H5 + NaHal
Под действием кислот или разбавленных растворов щелочей ацетоуксусный эфир омыляется с образованием нестабильной ацетоуксуслой кислоты, которая м мягких условиях декарбоксилируется с образованием ацетона:
- CH3COCH2COOC2H5 + H2O
 CH3COCH2COOH + C2H5OH
CH3COCH2COOH + C2H5OH - CH3COCH2COOH
 CH3COCH3 + CO2 + H2O
CH3COCH3 + CO2 + H2O
Аналогичным образом ведут себя и моно- и дизамещенные ацетоуксусные эфиры, полученные алкилированием натрийацетоуксусного эфира (кетонное расщепление), эта реакция используется для синтеза замещенных метилкетонов.
Иначе протекает взаимодействие ацетоуксусного эфира с концентрированными растворами щелочей: в этом случае протекает отщепление ацетильной группы с образованием двух молекул уксусной кислоты (кислотное расщепление), эта реакция идет и с замещенными ацетоуксусными эфирами и используется для синтеза гомологов уксусной кислоты через алкилпроизводные ацетоуксусного эфира:
- CH3COCHRCOOC2H5 + OH- + H2O
 CH3COO- + RCH2COOH + C2H5OH
CH3COO- + RCH2COOH + C2H5OH
Синтез
Классическим методом синтеза ацетоуксусного эфира является сложноэфирная конденсации этилацетата в присутствии этанола под действием металлического натрия, катализатором конденсации является образующийся in situ этилат натрия. Образующийся натрийацетоуксусный эфир действием разбавленной минеральной кислоты переводят в ацетоуксусный эфир[1]:
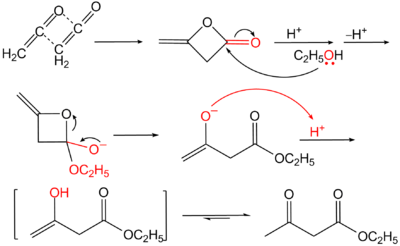
Ацетоуксусный эфир также может быть синтезирован ацилированием этанола дикетеном, этот метод является промышленным методом синтеза:
Применение
Ацетоуксусный эфир широко применяется в органическом синтезе. Будучи 1,3-дифункциональным реагентом, он применяется для синтеза гетероциклических соединений. В промышленности применяется в производстве фармацевтических препаратов (пирамидона, акрихина, витамина B1), а также красителей для цветной фотографии, ряда органических веществ.
Биологическое действие
Обладает кожнораздражающим действием. Всасывается через кожу. ПДК 1 мг/м³
Примечания
- ↑ С.В.Пономарев, А.С.Золотарева, Л.Г.Сагинова, В.И.Теренин "Практикум по органической химии"
Ссылки
- Ацетоуксусный эфир // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.

Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
- Добавить иллюстрации.
Категория:- Сложные эфиры
- CH3(HO)C=CHCOOC2H5 + ROCl
Wikimedia Foundation. 2010.