- Оксид цинка
-
Оксид цинка 
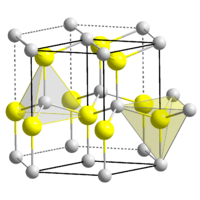
Общие Систематическое наименование Цинка оксид Химическая формула ZnO Физические свойства Состояние (ст. усл.) твердое Молярная масса 81.408 г/моль Плотность 5.61 г/см³ Термические свойства Температура сублимации 1800 °C Молярная теплоёмкость (ст. усл.) 40,28 Дж/(моль·К) Энтальпия образования (ст. усл.) 350.8 кДж/моль Оптические свойства Показатель преломления 2,015 и 2,068 Структура Кристаллическая структура гексагональная сингония, a = 0,32495 нм, c = 0,52069 нм, z = 2 Классификация Рег. номер CAS 1314-13-2 Рег. номер PubChem 14806 Регистрационный номер EC 215-222-5 ChEBI ZH4810000 Безопасность ПДК в воздухе рабочей зоны 0.5 мг/м3
в атмосферном воздухе 0.05 мг/м3Токсичность Токсичен, при вдыхании пыли вызывает литейную лихорадку R-фразы R50/53 S-фразы S60, S61 NFPA 704 См. также: Оксид цинка (лекарственное средство)Окси́д ци́нка (окись цинка) ZnO — бесцветный кристаллический порошок, нерастворимый в воде, желтеющий при нагревании и сублимирующийся при 1800 °C .
Содержание
Свойства
- Теплопроводность: 54 Вт/(м*К)[1]
Оксид цинка является прямозонным полупроводником с шириной запрещённой зоны 3,36 эВ. Естественное легирование кислородом делает его полупроводником n-типа.
При нагревании вещество меняет цвет: белый при комнатной температуре, оксид цинка становится жёлтым. Объясняется это уменьшением ширины запрещённой зоны и сдвигом края в спектре поглощения из УФ-области в синюю.
Оксид цинка амфотерен — реагирует с кислотами с образованием солей, при взаимодействии с растворами щелочей образует комплексные три- тетра- и гексагидроксицинкаты (Na2[Zn(OH)4], Ba2[Zn(OH)6]):
- [Zn(OH)3]- + OH-
 [Zn(OH)4]2-
[Zn(OH)4]2-
Оксид цинка растворяется в водном растворе аммиака, образуя комплексный аммиакат:
- ZnO + 4NH3 + Н20 — [Zn(NH3)4](OH)2
При сплавлении с щелочами и оксидами металлов оксид цинка образует цинкаты:
- ZnO + 2NaOH
 Na2ZnO2 + H2O
Na2ZnO2 + H2O - ZnO + CoO
 CoZnO2
CoZnO2
При сплавлении с оксидами бора и кремния оксид цинка образует стекловидные бораты и силикаты:
- ZnO + B2O3
 Zn(BO2)2
Zn(BO2)2 - ZnO + SiO2
 ZnSiO3
ZnSiO3
Получение
- природный минерал цинкит
- сжиганием паров цинка в кислороде («французский процесс»)
- термическим разложением соединений:
- ацетата ZnS
- гидротермальный синтез[2]
- извлечением из пылей и шламов металлургических комбинатов, особенно тех, что работают на металлоломе в качестве сырья (он содержит значительную долю оцинкованного железа).
- извлечением из тройной системы фазового равновесия «нитрат цинка-нитрат амина-вода» (с нитратом пиридина и хинолина размерность частиц порядка 5-10 нм до 75 %)
Применение
- активатор вулканизации некоторых каучуков
- вулканизирующий агент хлоропреновых каучуков
- катализатор синтеза метанола
- белый пигмент при производстве красок и эмалей (в настоящее время (2007) вытеснен нетоксичной двуокисью титана TiO2)
- наполнитель и пигмент в производстве:
- В медицине в виде присыпок и в составе мазей как антисептик. См. статью: Оксид цинка (лекарственное средство).
- добавка к кормам для животных
- в производстве стекла и красок на основе жидкого стекла
- как один из компонентов преобразователя ржавчины
Известно также, что оксид цинка обладает фотокаталитической активностью, что на практике используется для создания самоочищающихся поверхностей, бактерицидных покрытий для стен и потолков в больницах и пр. Для фотокаталитической очистки воды в промышленных масштабах оксид цинка в настоящее время не используется.
Кроме того, порошок оксида цинка — перспективный материал в качестве рабочей среды для порошковых лазеров. На основе оксида цинка создали светодиод голубого цвета. Тонкие пленки и иные наноструктуры на основе оксида цинка могут применяться как чувствительные газовые и биологические сенсоры.
Свойства оксида цинка обуславливают его широко применение в фармацевтической промышленности. Оксид цинка нашел широкое применение в создании абразивных зубных паст и цементов в терапевтической стоматологии, в кремах для загара и косметических процедурах, в производстве электрокабеля, искусственной кожи и резинотехнических изделий. Кроме того, применение распространено в шинной, лакокрасочной, нефтеперерабатывающей промышленностях. Оксид цинка участвует процессе производства стекла и керамики.
Влияние на человека
Слабо токсичен, ПДК в воздухе рабочих помещений — 6 мг/м³. Пыль может образовываться при обжиге изделий из латуни.
Примечания
- ↑ Термопрохладки
- ↑ S. Baruah and J. Dutta «Review: Hydrothermal growth of ZnO nanostructures» Sci. Technol. Adv. Mater. 10 (2009) 013001 скачать бесплатно
ПДК 2 мг/м3.
Литература
- В.И.Перельман. Краткий справочник химика. — М.-Л.: Химия, 1964.
- статья «Цинка окись» в Большой советской энциклопедии

Категории:- Соединения цинка
- Оксиды
- Ингибиторы коррозии
- Пигменты
- Катализаторы
- Полупроводники
- Амфотерные оксиды
Wikimedia Foundation. 2010.

