- Метилйодид
-
Йодистый метил 
Общие Систематическое наименование иодметан Традиционные названия метилиодид Химическая формула CH3I Эмпирическая формула CH3I Молярная масса 141.94 г/моль Физические свойства Плотность вещества 2.2789 г/см³ Состояние (ст. усл.) жидкость Термические свойства Температура плавления -66.45 °C Температура кипения 42.43 °C Температура вспышки -28 °C Давление пара 50 Химические свойства Растворимость в воде 1.4 г/100 мл Оптические свойства Показатель преломления 1.5304 Структура Дипольный момент 1.59 Дебай Классификация номер EINECS 200-819-5 RTECS PA9450000 Токсикология Токсичность канцероген Иодистый метил (метилиодид, MeI) — тяжёлая летучая жидкость с формулой CH3I. Часто используется в органическом синтезе для метилирования. В природе выделяется в небольшом количестве рисом.
Содержание
Свойства
Тяжёлая подвижная жидкость, желтеющая при стоянии, особенно на свету из-за выделения I2. Для предотвращения этого его хранят в тёмной посуде над медной проволокой, поглощающей йод.
Получение
Получают по экзотермической реакции между метанолом и фосфора трииодидом, который получается in situ из красного фосфора
- 3 CH3OH + PI3 → 3 CH3I + H3PO3
Также реакцией иодида калия с диметилсульфатом в присутствии карбоната кальция:[1]
Для очистки CH3I может быть обработан Na2S2O3 для удаления иода. Или обработан раствором соды и высушен плавленным хлористым кальцием и перегоняют.[2]
Также можно получить реакцией йодистого калия с метилтозилатом
- KI + CH3OSO2C6H4CH3 → CH3I + KOSO2C6H4CH3
Или реакцией метанола с пятийодистым фосфором
- CH3OH + PI5 → [3]
Применение
Йодметан отличный реагент для SN2 реакций замещения. Он стерически открыт для атак нуклеофилам и к тому же йод является хорошей уходящей группой.
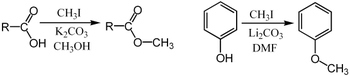
В представленных реакциях основные карбонатыK2CO3 or Li2CO3) удаляют кислые протоны в результате чего образуются карбоксильный и фенольный карбанион, который выступает в роле нуклеофила в SN2 реакции. Иодиды являются более "мягкими" реагентами в нуклеофильных реакциях в силу более слабой связи с внешними электронами и более лёгкой поляризуемостью иодида. В силу этого он предпочитает более "мягкие" нуклеофилы. Так при алкилировании тиоционата происходит алкилирование по сере, а не по азоту с образованием CH3SCN), а не CH3NCS. Это также наблюдается при алкилировании 1,3-дикарбонильных соединений, метилирование енолятов этих соединений практически польностью идёт по углеродномы атому, хотя заряд сосредоточен больше на атомах кислорода. Метил йодид лекго образовует метилмагний йодид. Он широко распространён на практике из-за лёгкости получения и часто используется в учебных лабораториях. В Monsanto[4] процессе йодметан образуется in situ из метанола и йодоводорода . CH3I затем реагирует окисью углерода в присутствии родиевых комплексов с образованием ацетил йодида, прекурсора уксусной кислоты после гидролиза. Большое количество уксусной кислоты получается таким способом.
Безопасность
Ярко выраженный канцероген. ЛД50 при ингаляции для крыс 76 мг/кг. В печени метилиодид быстро превращается в S-метилглутатион. Вдыхание большого количества паров йодметана вызывает поражение лёгких, печени, почек и центральной нервной системы, что приводит к тошноте, головокружению, кашлю и рвоте. Длительный контакт с кожей вызывает ожоги. Большие дозы при ингаляции вызывают отёк лёгких.
Пределы взрываемости воздушных смесей 8.5 - 66%.
Примечания
- ↑ Л. Гаттерман, Г. Виланд. Практические работы по органической химии. М.-Л., ГНТИ ХимЛит., 1948, стр. 139
- ↑ Практические работы по органической химии. Выпуск 2. Юрьев Ю. К. Общие правила работы. Примеры синтезов. Изд-во МГУ, М., 1957, стр. 173
- ↑ Препаративная органическая химия.М., Госхимиздат, 1959, стр. 424
- ↑ http://en.wikipedia.org/wiki/Monsanto_process
См. также
Wikimedia Foundation. 2010.
