- Дейтерий
-
Дейтерий 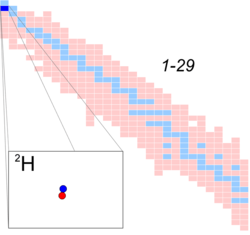
Общие сведения Название, символ Дейтерий, 2H Альтернативные названия тяжёлый водород, D Нейтронов 1 Протонов 1 Свойства нуклида Атомная масса 2,0141017778(4)[1] а. е. м. Избыток массы 13 135,7216(3)[1] кэВ Удельная энергия связи (на нуклон) 1 112,283(0)[1] кэВ Изотопная распространённость 0,0115(70) %[2] Период полураспада стабильный[2] Спин и чётность ядра 1+[2] Дейте́рий (лат. deuterium, от др.-греч. δεύτερος «второй»), тяжёлый водород, обозначается символами D и 2H — стабильный изотоп водорода с атомной массой, равной 2. Ядро (дейтрон) состоит из одного протона и одного нейтрона.
Открыт в 1932 г. американским физико-химиком Г. Юри. Природное содержание — 0,0115 ± 0,0070[2] %.
Содержание
Изотопные модификации соединений водорода
Соединения изотопов водорода практически не различаются по химическим свойствам, но обладают довольно различными физическими свойствами (температура плавления, кипения, вес)[3]. Молекула D2, состоит из двух атомов дейтерия. Вещество имеет следующие физические свойства:
- Температура плавления −254,5 °C
- Температура кипения −249,5 °C
Содержание дейтерия в природном водороде — 0,0011-0,0016 ат.% [4].
По своим химическим свойствам соединения дейтерия имеют определенные особенности. Так, например, углерод-дейтериевые связи оказываются более «прочными», чем углерод-протиевые, из-за чего химические реакции с участием атомов дейтерия идут в несколько раз медленнее. Этим, в частности, обусловлена токсичность тяжёлой воды (вода состава D2O называется тяжёлой водой из-за большой разницы в массе протия и дейтерия).
Получение
Мировое производство дейтерия — десятки тысяч тонн в год. Основные методы получения: многоступенчатый электролиз воды, ректификация воды, ионный обмен, ректификация аммиака. При электролизе 100л воды выделяется 7,5 мл 60%-ного D2O[5].
При длительном кипячении природной воды концентрация тяжёлой воды в ней повышается очень незначительно — в пределах 1 %. Среди населения бытует миф о том, что это якобы может вредно сказаться на здоровье. В действительности же повышение концентрации тяжёлой воды при кипячении ничтожно, гораздо сильнее ощущается повышение концентрации растворённых солей.
Применение
Дейтерий широко используется в атомной энергетике как замедлитель нейтронов в атомных реакторах; в смеси с тритием или в соединении с литием-6 применяют для термоядерной реакции в водородных бомбах, применяется в качестве меченого стабильного индикатора в лабораторных исследованиях и технике. Перспективным также представляется применение дейтерия (в смеси с тритием) для получения высокотемпературной плазмы, необходимой для осуществления управляемого термоядерного синтеза (см. проект ITER).
Примечания
- ↑ 1 2 3 G. Audi, A.H. Wapstra, and C. Thibault (2003). «The AME2003 atomic mass evaluation (II). Tables, graphs, and references.». Nuclear Physics A 729: 337—676. DOI:10.1016/j.nuclphysa.2003.11.003.
- ↑ 1 2 3 4 G. Audi, O. Bersillon, J. Blachot and A. H. Wapstra (2003). «The NUBASE evaluation of nuclear and decay properties». Nuclear Physics A 729: 3–128. DOI:10.1016/j.nuclphysa.2003.11.001.
- ↑ Н. Е. Кузьменко, В. В. Ерёмин, В. А. Попков Начала химии (том 1) 2007.— М.: Изд-во Экзамен, С.298
- ↑ Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- ↑ Н. Е. Кузьменко, В. В. Ерёмин, В. А. Попков Начала химии (том 1) 2007.— М.: Изд-во Экзамен, С.299
Литература
- Н. Е. Кузьменко, В. В. Ерёмин, В. А. Попков Начала химии (том 1) 2007.— М.: Изд-во Экзамен, С.298-299
- Физическая энциклопедия. / Гл. ред. Прохоров А. М. — М.: Советская энциклопедия, 1988. — Т. 1.— 704 с., ил. — 100 000 экз.
 Изотопы водородаКатегория:
Изотопы водородаКатегория:- Изотопы водорода
Wikimedia Foundation. 2010.
