- Хлористая кислота
-
Хлористая кислота 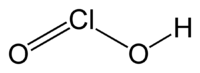
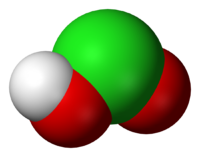
Общие Систематическое наименование Хлористая кислота Химическая формула HClO2 Физические свойства Состояние (ст. усл.) Бесцветный раствор Отн. молек. масса 68.46 а. е. м. Молярная масса 68.46 г/моль Термические свойства Химические свойства pKa 1.96 Классификация Рег. номер CAS 13898-47-0 Хлористая кислота — HClO2, одноосновная кислота средней силы.
Содержание
Свойства
Хлористая кислота НClO2 в свободном виде неустойчива, даже в разбавленном водном растворе она быстро разлагается:
Ангидрид этой кислоты неизвестен.
Получение
Раствор кислоты получают из её солей - хлоритов, образующихся в результате взаимодействия ClO2 со щёлочью:
А также по реакции:
Соли хлористой кислоты называются хлоритами, они, как правило, бесцветны и хорошо растворимы в воде. В отличие от гипохлоритов, хлориты проявляют выраженные окислительные свойства только в кислой среде. Из солей наибольшее применение имеет хлорит натрия NaClO2, применяемый для отбелки тканей и бумажной массы. Хлорит натрия получают по реакции:Безводный NaClO2 взрывается при ударе и нагревании; воспламеняется при контакте с органическими веществами, резиной, бумагой и т. д.
Литература
- Ахметов Н. С. «Общая и неорганическая химия» М.: Высшая школа, 2001
- Карапетьянц М. Х., Дракин С. И. «Общая и неорганическая химия» М.: Химия 1994
Ссылки
 На Викискладе есть медиафайлы по теме Хлористая кислота
На Викискладе есть медиафайлы по теме Хлористая кислота
Основные хлорсодержащие неорганические кислоты Соляная кислота(HCl)
Соляная кислота(HCl) Хлорноватистая кислота(HClO)
Хлорноватистая кислота(HClO)  Хлористая кислота(HClO2)
Хлористая кислота(HClO2)  Хлорноватая кислота(HClO3)
Хлорноватая кислота(HClO3)  Хлорная кислота(HClO4)
Хлорная кислота(HClO4) Категории:
Категории:- Неорганические кислородсодержащие кислоты
- Соединения хлора
-
Wikimedia Foundation. 2010.




