- Критическая точка (термодинамика)
-
Фазовые переходы 
Статья является частью серии «Термодинамика». Понятие фазы Равновесие фаз Квантовый фазовый переход Разделы термодинамики Начала термодинамики Уравнение состояния Термодинамические величины Термодинамические потенциалы Термодинамические циклы Фазовые переходы править См. также «Физический портал» Критическая точка — сочетание значений температуры
 и давления
и давления  (или, что эквивалентно, молярного объёма
(или, что эквивалентно, молярного объёма  ), при которых исчезает различие в свойствах жидкой и газообразной фаз вещества.
), при которых исчезает различие в свойствах жидкой и газообразной фаз вещества.Критическая температура фазового перехода — значение температуры в критической точке. При температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Физическое значение
В критической точке плотность жидкости и её насыщенного пара становятся равны, а поверхностное натяжение жидкости падает до нуля, потому исчезает граница раздела фаз жидкость-пар.
Для смеси веществ критическая температура не является постоянной величиной и может быть представлена пространственной кривой (зависящей от пропорции составляющих компонентов), крайними точками которой являются критические температуры чистых веществ — компонентов рассматриваемой смеси.
Критической точке на диаграмме состояния вещества соответствуют предельные точки на кривых равновесия фаз, в окрестностях точки фазовое равновесие нарушается, происходит потеря термодинамической устойчивости по плотности вещества. По одну сторону от критической точки вещество однородно (обычно при
 ), а по другую — разделяется на жидкость и пар.
), а по другую — разделяется на жидкость и пар.В окрестностях точки наблюдаются критические явления: из-за роста характеристических размеров флуктуаций плотности резко усиливается рассеяние света при прохождении через вещество — при достижении размеров флуктуаций порядков сотен нанометров, т. е. длин волн света, вещество становится непрозрачным — наблюдается его критическая опалесценция. Рост флуктуаций приводит также к усилению поглощения звука и росту его дисперсии, изменению характера броуновского движения, аномалиям вязкости, теплопроводности, замедлению установления теплового равновесия и т. п.
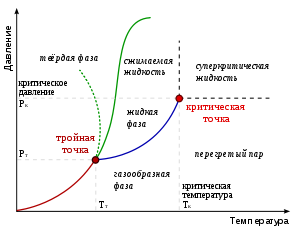 На этой типичной фазовой диаграмме граница между жидкой и газообразной фазой изображена в виде кривой, начинающейся в тройной точке, и заканчивающейся в критической точке.
На этой типичной фазовой диаграмме граница между жидкой и газообразной фазой изображена в виде кривой, начинающейся в тройной точке, и заканчивающейся в критической точке.
История
Практически явление критической точки было обнаружено при нагревании жидкости, частично заполняющей запаянную трубку. По мере нагрева мениск постепенно терял свою кривизну, становясь всё более плоским, а при достижении критической температуры переставал быть различимым.
Параметры критических точек некоторых веществ Вещество 


Единицы Кельвины Атмосферы см³/моль Водород 33,0 12,8 61,8 Кислород 154,8 50,1 74,4 Ртуть 1750 1500 44 Этанол 516,3 63,0 167 Диоксид углерода 304,2 72,9 94,0 Вода 647 218,3 56 Азот 126.25 Аргон 150.86 Бром 588 Гелий 5.19 Йод 819 Криптон 209.45 Ксенон 289.73 Мышьяк 1673 Неон 44.4 Радон 378 Селен 1766 Сера 1314 Фосфор 994 Фтор 144.3 Хлор 416.95 Критические точки существуют не только для чистых веществ, но и, в некоторых случаях, для их смесей и определяют параметры потери устойчивости смеси (с разделом фаз) — раствор (одна фаза). Примером такой смеси может служить смесь фенол-вода.

Термодинамические состояния вещества Твёрдое тело Жидкость Электролит • Перегретая • Переохлаждённая • Расплав (Критическая точка • Температура кипения)
Газ Плазма Электромагнитная • Кварк-глюонная • Глазма
См. также Сверхкритическая жидкость • Вырожденный газ • Конденсат Бозе — Эйнштейна • Странная материя • Кривая охлаждения • Твёрдый гелий (λ-точка) • Квантовая жидкость (Сверхтекучесть • Сверхтекучее твёрдое тело) • Дисперсная система (Раствор • Коллоидные • Грубодисперсная • Свободнодисперсная коллоидная (Дым • Золи)) • Термодинамическая фаза • Фазовый переход • Нормальные и стандартные условия • Статистика Ферми — Дирака • Уравнение состояния • Теория катастроф
Категории:- Термодинамика
- Физическая химия
- Фазовые переходы
- Критические величины
Wikimedia Foundation. 2010.
