- МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ
- МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ
-
взаимодействие электрически нейтральных молекул или атомов; определяет существование жидкостей и мол. кристаллов, отличие реальных газов от идеальных и проявляется в разл. физ. явлениях. М. в. зависит от расстояния r между молекулами и, как правило, описывается потенц. энергией вз-ствия U(r) (потенциалом М. в.), т. к. именно ср. потенц. энергия вз-ствия определяет состояние и мн. св-ва вещества.Впервые М. в. стал учитывать голл. физик Я. Д. ван дер Ваальс (1873) для объяснения св-в реальных газов и жидкостей. Он предположил, что на малых расстояниях r между молекулами действуют силы отталкивания, к-рые с увеличением расстояния сменяются силами притяжения, и на основе этих представлений получил ур-ние состояния реального газа (Ван-дер-Ваальса уравнение).М. в. имеет злектрич. природу и складывается из сил притяжения (ориентационных, индукционных и дисперсионных) и сил отталкивания.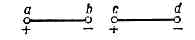 Рис. 1. Электрич. диполи аb и cd при таком расположении притягиваются, т. к. разноимённые заряды b и с взаимодействуют сильнее, чем находящиеся на большем расстоянии друг от друга одноимённые заряды а и с (а также b и d).Ориентационные силы действуют между полярными молекулами, т. р. молекулами, обладающими дипольными и квадрупольными электрич. моментами (см. ДИПОЛЬ). Сила притяжения между двумя полярными молекулами максимальна в том случае, когда их дипольные моменты располагаются по одной линии (рис. 1) и зависит от их взаимной ориентации (поэтому силы М. в. в этом случае и наз. ориентационными). Хаотич. тепловое движение непрерывно меняет ориентацию полярных молекул, но, как показывает расчёт, среднее по всем ориентациям значение силы имеет конечную, не равную нулю, величину. Потенц. энергия ориентац. М. в.Uор(r)=p1p2r-6,где р1 и р2 — дипольные моменты взаимодействующих молекул. Соответственно сила вз-ствия Fор=-дUор/дr=r-7, т. е. Fop убывает расстоянием значительно быстрее, чем кулоновская сила вз-ствия заряженных ч-ц (Fкул = г-2).Индукционные (поляризационные) силы действуют между полярной и неполярной молекулами, а также между полярными молекулами. Полярная молекула создаёт электрич. поле, к-рое поляризует др. молекулу — индуцирует в ней дипольный момент. Потенц. энергия М. в. в этом случае пропорц. дипольному моменту р1 полярной молекулы и поляризуемости a2 второй молекулы: Uинд =p1a2r-6. Индукц. силы Fинд = г-7. Дисперсионное М. в. действует между неполярными молекулами. Его природа была выяснена только после создания квант. механики. В атомах и молекулах эл-ны сложным образом движутся вокруг ядер. В среднем по времени дипольные моменты неполярных молекул оказываются равными нулю, но мгновенное значение дипольного момента может быть отлично от нуля. Мгновенный диполь создаёт электрич. поле, поляризующее соседние молекулы,— возникает вз-ствие мгновенных диполей. Энергия взаимодействия неполярных молекул есть ср. результат вз-ствия таких мгновенных диполей. Потенц. энергия дисперсионного М. в. Uдисп (r) =a1a2r-6, a Fдисп = r-7 (a1 и a2 — поляризуемости взаимодействующих молекул). М. в. данного типа наз. дисперсионным потому, что дисперсия света в в-ве определяется теми же св-вами молекул. Дисперсионные силы действуют между всеми молекулами и атомами, т. к. механизм их появления не зависит от наличия у молекул (атомов) пост. дипольных моментов. Обычно эти силы превосходят по величине как ориентационные, так и индукционные. Только при вз-ствии молекул с большими дипольными моментами, напр. молекул воды, Fор>Fдисп (в 3 раза для Н2O). При вз-ствии же таких полярных молекул, как СО, HI, HBr и др., Fдисп в десятки и сотни раз превосходят все остальные. Существенно, что все три типа М. в. одинаковым образом убывают с расстоянием:U=Uор+Uинд+Uдисп =r-6.Силы отталкивания действуют между молекулами на очень малых расстояниях, когда приходят в соприкосновение заполненные электронные оболочки атомов, входящих в состав молекул. Паули принцип запрещает проникновение заполненных электронных оболочек друг в друга. Возникающие при этом силы отталкивания зависят в большей степени, чем силы притяжения, от индивидуальных особенностей молекул. К хорошему согласию с данными экспериментов приводит допущение, что потенц. энергия сил отталкивания Uот возрастает с уменьшением расстояния по законуUот(r)=r-12, т. е. Fот=r-13.Если принять, что U(r)=0 при r®?, и учесть, что энергия притяжения убывает с уменьшением расстояния пропорц. r-6, а энергия отталкивания растёт =r-12, то кривая U(r) будет иметь вид, изображённый на рис. 2. Минимуму U(r) соответствует расстояние, на к-ром силы вз-ствия молекул равны нулю.
Рис. 1. Электрич. диполи аb и cd при таком расположении притягиваются, т. к. разноимённые заряды b и с взаимодействуют сильнее, чем находящиеся на большем расстоянии друг от друга одноимённые заряды а и с (а также b и d).Ориентационные силы действуют между полярными молекулами, т. р. молекулами, обладающими дипольными и квадрупольными электрич. моментами (см. ДИПОЛЬ). Сила притяжения между двумя полярными молекулами максимальна в том случае, когда их дипольные моменты располагаются по одной линии (рис. 1) и зависит от их взаимной ориентации (поэтому силы М. в. в этом случае и наз. ориентационными). Хаотич. тепловое движение непрерывно меняет ориентацию полярных молекул, но, как показывает расчёт, среднее по всем ориентациям значение силы имеет конечную, не равную нулю, величину. Потенц. энергия ориентац. М. в.Uор(r)=p1p2r-6,где р1 и р2 — дипольные моменты взаимодействующих молекул. Соответственно сила вз-ствия Fор=-дUор/дr=r-7, т. е. Fop убывает расстоянием значительно быстрее, чем кулоновская сила вз-ствия заряженных ч-ц (Fкул = г-2).Индукционные (поляризационные) силы действуют между полярной и неполярной молекулами, а также между полярными молекулами. Полярная молекула создаёт электрич. поле, к-рое поляризует др. молекулу — индуцирует в ней дипольный момент. Потенц. энергия М. в. в этом случае пропорц. дипольному моменту р1 полярной молекулы и поляризуемости a2 второй молекулы: Uинд =p1a2r-6. Индукц. силы Fинд = г-7. Дисперсионное М. в. действует между неполярными молекулами. Его природа была выяснена только после создания квант. механики. В атомах и молекулах эл-ны сложным образом движутся вокруг ядер. В среднем по времени дипольные моменты неполярных молекул оказываются равными нулю, но мгновенное значение дипольного момента может быть отлично от нуля. Мгновенный диполь создаёт электрич. поле, поляризующее соседние молекулы,— возникает вз-ствие мгновенных диполей. Энергия взаимодействия неполярных молекул есть ср. результат вз-ствия таких мгновенных диполей. Потенц. энергия дисперсионного М. в. Uдисп (r) =a1a2r-6, a Fдисп = r-7 (a1 и a2 — поляризуемости взаимодействующих молекул). М. в. данного типа наз. дисперсионным потому, что дисперсия света в в-ве определяется теми же св-вами молекул. Дисперсионные силы действуют между всеми молекулами и атомами, т. к. механизм их появления не зависит от наличия у молекул (атомов) пост. дипольных моментов. Обычно эти силы превосходят по величине как ориентационные, так и индукционные. Только при вз-ствии молекул с большими дипольными моментами, напр. молекул воды, Fор>Fдисп (в 3 раза для Н2O). При вз-ствии же таких полярных молекул, как СО, HI, HBr и др., Fдисп в десятки и сотни раз превосходят все остальные. Существенно, что все три типа М. в. одинаковым образом убывают с расстоянием:U=Uор+Uинд+Uдисп =r-6.Силы отталкивания действуют между молекулами на очень малых расстояниях, когда приходят в соприкосновение заполненные электронные оболочки атомов, входящих в состав молекул. Паули принцип запрещает проникновение заполненных электронных оболочек друг в друга. Возникающие при этом силы отталкивания зависят в большей степени, чем силы притяжения, от индивидуальных особенностей молекул. К хорошему согласию с данными экспериментов приводит допущение, что потенц. энергия сил отталкивания Uот возрастает с уменьшением расстояния по законуUот(r)=r-12, т. е. Fот=r-13.Если принять, что U(r)=0 при r®?, и учесть, что энергия притяжения убывает с уменьшением расстояния пропорц. r-6, а энергия отталкивания растёт =r-12, то кривая U(r) будет иметь вид, изображённый на рис. 2. Минимуму U(r) соответствует расстояние, на к-ром силы вз-ствия молекул равны нулю. Рис. 2. Зависимость потенц. энергии U(r) межмол. взаимодействия от расстояния r между молекулами; r=s — наименьшее возможное расстояние между неподвижными молекулами; e — глубина потенц. ямы (определяющая энергию связи молекул).Рассчитать с достаточной точностью U(r) на основе квант. механики очень сложно, поэтому обычно подбирают для U(r) ф-лу и входящие в неё параметры таким образом, чтобы проделанные с их помощью расчёты хорошо согласовались с экспернм. данными. Наиболее часто пользуются ф-лами Леннард-Джонса:U(r)=-ar-6+br-12и Букингема:U(r)=—ar-6+bехр(-cr),где параметры а, b, с связаны простыми соотношениями с глубиной e и положением s потенц. ямы и определяются из разл. эксперим. данных (коэфф. диффузии, теплопроводности и вязкости и т. д.).Приведённые выше ф-лы игнорируют ориентационные М. в., играющие исключительно важную роль в случае многоатомных молекул. Зависимость U(r) от ориентац. М. в. особенно существенна в кристаллах. Её можно учесть с помощью множителя, в к-рый входят углы, характеризующие взаимную ориентацию молекул, либо с помощью метода атом-атомных потенц. ф-ций (см. МЕЖАТОМНОЕ ВЗАИМОДЕЙСТВИЕ). В последнем случае потенциалы Леннард-Джонса и Букингема используют для описания взаимодействий атомов, принадлежащих разным молекулам.Наряду с эмпирич. модельными подходами для изучения М. в. всё чаще используются методы квантовой химии. Расчёты потенц. поверхностей (зависимости энергии вз-ствия от расстояния между молекулами и их взаимной ориентации) проведены в разл. приближениях для мн. димеров (пар молекул). Эти расчёты позволили не только количественно описать М. <в., но и разобраться в их физ. природе. Так, оказалось, что во мн. случаях М. в. в значит. степени определяется переносом заряда с одной молекулы на другую, что не учитывали классич. представления о М. в.
Рис. 2. Зависимость потенц. энергии U(r) межмол. взаимодействия от расстояния r между молекулами; r=s — наименьшее возможное расстояние между неподвижными молекулами; e — глубина потенц. ямы (определяющая энергию связи молекул).Рассчитать с достаточной точностью U(r) на основе квант. механики очень сложно, поэтому обычно подбирают для U(r) ф-лу и входящие в неё параметры таким образом, чтобы проделанные с их помощью расчёты хорошо согласовались с экспернм. данными. Наиболее часто пользуются ф-лами Леннард-Джонса:U(r)=-ar-6+br-12и Букингема:U(r)=—ar-6+bехр(-cr),где параметры а, b, с связаны простыми соотношениями с глубиной e и положением s потенц. ямы и определяются из разл. эксперим. данных (коэфф. диффузии, теплопроводности и вязкости и т. д.).Приведённые выше ф-лы игнорируют ориентационные М. в., играющие исключительно важную роль в случае многоатомных молекул. Зависимость U(r) от ориентац. М. в. особенно существенна в кристаллах. Её можно учесть с помощью множителя, в к-рый входят углы, характеризующие взаимную ориентацию молекул, либо с помощью метода атом-атомных потенц. ф-ций (см. МЕЖАТОМНОЕ ВЗАИМОДЕЙСТВИЕ). В последнем случае потенциалы Леннард-Джонса и Букингема используют для описания взаимодействий атомов, принадлежащих разным молекулам.Наряду с эмпирич. модельными подходами для изучения М. в. всё чаще используются методы квантовой химии. Расчёты потенц. поверхностей (зависимости энергии вз-ствия от расстояния между молекулами и их взаимной ориентации) проведены в разл. приближениях для мн. димеров (пар молекул). Эти расчёты позволили не только количественно описать М. <в., но и разобраться в их физ. природе. Так, оказалось, что во мн. случаях М. в. в значит. степени определяется переносом заряда с одной молекулы на другую, что не учитывали классич. представления о М. в.
Физический энциклопедический словарь. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1983.
.
