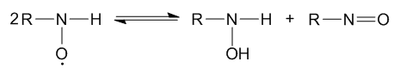- Нитроксильные радикалы
-
Нитроксильные радикалы — органические радикалы, содержащие нитроксильную группу N-O·. Впервые открыты в 1951 г.[1] Первый синтез соединения 2,2,6,6-тетраметил-4-пиперидон-1-оксил (4-оксо-TEMPO) был выполнен О.Л. Лебедевым в 1959 г.[2]
Содержание
Классификация и номенклатура
Нитроксильные радикалы являются представителями различных рядов: пиперидина, пирролина, пирролидина, пиперазина, изоиндолина, карболина, азетидина, имидазолина и др.
Один из способов наименования радикалов исходит из названия исходного вещества, к которому добавляется окончание «оксил» с указанием места расположения этой группы (например, 2,2,6,6-тетраметилпиперидин-1-оксил (TEMPO), 3-карбамоил-2,2,5,5-тетраметилпирролидин-1-оксил (PCM), 3-карбокси-2,2,5,5-тетраметилпирролидин-1-оксил (PCA)). Согласно другому способу, за основу принимается нитроксильная группа — к названию заместителей добавляется окончание «нитроксил», например, (C6H5)2NO· - дифенилнитроксил.
Строение нитроксильной связи
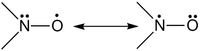
Нитроксильная группа содержит трёхэлектронную связь:
Неспаренный электрон находится на разрыхляющей π*-орбитали, образованной из 2pz-орбиталей атомов азота и кислорода. Гибридизация связей атома азота близка к sp2. В ди-трет.алкилнитроксилах неспаренный электрон практически равномерно локализован на атомах N и O. При замене алкильного радикала на арильный спиновая плотность на атома азота значительно уменьшается, а на атоме кислорода почти не меняется.
Стабильные нитроксильные радикалы
Нитроксильные радикалы, которые характеризуются наличием стерических затруднений вблизи N-O группы (например, обусловленные третичными атомами углерода), отличаются высокой стабильностью и могут быть выделены в свободном состоянии:

Стабильность этих веществ зависит от степени делокализации неспаренного электрона, а также от стерических затруднений в их молекулах. Некоторые нитроксильные радикалы могут храниться годами без разложения.
Стабильные нитроксильные радикалы являются полярными окрашенными веществами, твёрдые или жидкие. Газообразным является только ди-(трифторметил)нитроксил (CF3)2NO·.
Как и все радикалы, нитроксильные радикалы имеют спектр ЭПР. В их спектре наблюдается триплетное расщепление, которое обусловлено сверхтонким взаимодействием неспаренного электрона радикала с ядром атома азота 14N. Константа сверхтонкого расщепления aN меняется от 0,65-1,1 для ацил(трет.бутил)нитроксила до 2,4-2,8 для алкоксиарилнитроксилов. g-Фактор нитроксильных радикалов находится в диапазоне 2,005-2,006.
Синтез нитроксильных радикалов
Окисление гидроксиламинов
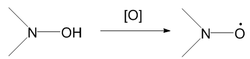
Окисление замещённых гидроксиламинов приводит к образованию нитроксильных радикалов:
Реакция протекает очень легко - даже при стоянии на воздухе.
Окисление аминов
Это наиболее распространённый способ синтеза, по которому был получен широкий ряд нитроксильных радикалов - производных циклических аминов. Наиболее удобными окислителями являются пероксид водорода в присутствии солей вольфрамовой кислоты и надкислоты:
В качестве окислителей можно использовать также гидропероксиды, озон
Восстановление нитрозосоединений
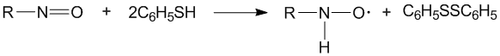
Взаимодействие нитросоединений с такими восстановителями, как гидроксиламины, тиолы может приводить к нитроксильным радикалам:
Свойства
Диспропорционирование
Диспропорционирование нитроксильных радикалов происходит в том случае, если на нитроксильной группе высокая спиновая плотность неспаренного электрона не делокализована на соседних группах. При этом образуются замещённый гидроксиламин и нитрозосоединение:
Окисление
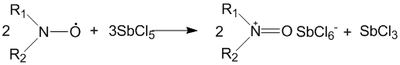
Окисление нитроксильных радикалов протекает только сильными окислителями (Cl2, SbCl5, SnCl4). Продуктом реакции являются оксоаммониевые соли:
Другие реакции
Помимо реакций по N-O группе нитроксильные радикалы вступают в реакции по другим функциональным группам молекулы, не затрагивающие свободной валентности, что позволяет получать модифицированные нитроксильные радикалы.
Применение
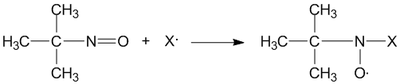
Нитроксильные радикалы могут быть использованы в методе спиновых меток (например, они образуются в реакции 2-метил-2-нитрозопропана со свободным радикалом и имеют время жизни, достаточное для определения aN и g-фактора и идентификации как полученного нитроксильного, так и исходного свободного радикала):
Литература
- Меди — Полимерные// Химическая энциклопедия в 5 томах. — М.: Большая Российская Энциклопедия, 1992. — Т. 3. — 639 с.
- Розанцев Э.Г., Шолле В.Д. Органическая химия свободных радикалов. — М.: Химия, 1979. — 344 с. — 3 200 экз.
- Нитроксильные радикалы: синтез, химия, приложения / Розанцев Э.Г., Жданов Р.И.. — М.: Наука, 1987. — 271 с. — 800 экз.
Ссылки
- ↑ A. N. Holden, W. A. Yager and F. R. Merity, J. Chem. Phys., 19, 1319 (1951)
- ↑ O. L. Lebedev, M. I. Khidekel and G. A. Razuvaev, Doklady Akademii Nauk SSSR, 140, 1327-1329 (1961)
См. также
Категории:- Органическая химия
- Соединения азота
Wikimedia Foundation. 2010.