- Дубильное вещество
-
Дубильные вещества — группа весьма разнообразных и сложных по составу растворимых в воде органических веществ ароматического ряда, содержащих гидроксильные радикалы фенольного характера. Дубильные вещества широко распространены в растительном царстве, обладают характерным вяжущим вкусом. Они способны осаждаться из водного или водно-спиртового раствора раствором клея, а с солями окиси железа давать различных оттенков зелёные или синие окрашивания и осадки (чернильного свойства).
Содержание
Распространение в природе
В растениях (в коре, древесине, корнях, листьях, плодах) они являются или как нормальные продукты их жизнедеятельности (физиологические дубильные вещества, по Wagner'y [Cross and Bevan (1882) смотрят на дубильные вещества как на выделения растительного организма и сравнивают их в этом отношении с мочевиной животных], или же составляют (патологические дубильные вещества) более или менее значительную часть болезненных наростов, образующихся на листьях и других органах некоторых видов дуба и сумаха вследствие укола, производимого насекомыми (см. дубильные материалы).
Свойства
Дубильные вещества в основном аморфны, имеют более или менее ясно выраженный кислотный характер и обладают замечательным свойством (по преимуществу физиологические дубильные вещества) дубить кожу (шкуры), то есть отнимать у них в значительной мере способность к гниению и затвердеванию при высыхании.
Будучи веществами легко окисляющимися, они в присутствии щелочей буреют, поглощая кислород воздуха, и во многих случаях действуют восстановительно, напр., на соли благородных металлов, а некоторые и на Фелингову жидкость.
История изучения
Несмотря на то что дубильные вещества стали известны уже давно (таннин был впервые получен Дейе [Deyeux] и независимо Сегеном в 1797 г. и в руках Берцелиуса в 1815 г. имелся уже в довольно чистом состоянии) и много изучались, к началу XX века они были недостаточно исследованными, и не только химическая натура и строение почти всех их оставалось невыясненными, но даже и эмпирический состав очень многих из них разными исследователями делался различно. Объясняется это легко, с одной стороны, тем, что, будучи в большинстве веществами, не способными кристаллизоваться, они трудно получаются в чистом виде, а с другой — малою их стойкостью и легкою изменяемостью. Глазивец (1867), как и многие другие, считал все Д. вещества за глюкозиды или тела, им подобные; однако позднейшие исследования показали, что таннин хотя, по-видимому, и встречается в соединении с глюкозой в альгаробиллах и мироболанах (Zöllfel, 1891), но сам по себе не есть глюкозид (H. Schiff 1873), также и Д. кислоты дубовой коры (Etti 1880, 83, 89, Löwe 1881), равно как и очень многие др. Д. вещества, ничего общего с глюкозидами не имеют, а получение из некоторых из них сахаристых веществ обусловливалось исключительно нечистотою исследовавшихся препаратов. В настоящее время можно с достаточной уверенностью судить лишь о строении таннина, представляющего ангидрид галловой кислоты (см. и ниже); что же касается других, то в них пока лишь, по-видимому, возможно предполагать, судя по реакциям распадения и некоторым другим, частью ангидридные соединения многоатомных фенолокислот и фенолов, образованные либо по типу простых, либо по типу сложных эфиров, частью ароматические кетонокислоты, являющиеся продуктами конденсации производных галловой кислоты; но часть Д. вещества все же должно и поныне считать за глюкозиды. Ввиду неизвестности строения сама собою понятна невозможность естественной группировки Д. веществ [Собственно Д. вещества выделяются в особую группу органических соединений, обладающих некоторой совокупностью общих признаков, лишь благодаря именно неизвестности их строения. Весьма возможно, что по выяснении последнего они распределятся со временем по различным классам органических соединений, и тогда не представится более надобности и в особом общем названии для них, а нынешнее название "Дубильное вещество", согласно недавнему предложению Рейнитцера, придется, пожалуй, удержать только для тех из них, которые на самом деле способны дубить кожи.]. Деление их по окрашиванию, производимому с солями окиси железа, на железосинящие (Eisenblauende) и железозеленящие (Eisengrünende) ныне оставлено, потому что одно и то же Д. вещество может давать иногда синее, а иногда зелёное окрашивание, смотря по тому, какую взять соль железа, а сверх того, окрашивание может изменяться от прибавки, например, малого количества щелочи. Деление Д. веществ на физиологические (см. выше), дубящие кожу и вместе с тем дающие при сухой перегонке пирокатехин и не дающие галловой кислоты при кипячении с слабой серной кислотой, и патологические, для дубления менее пригодные (хотя и осаждающиеся раствором клея), при сухой перегонке дающие пирогаллол, а при кипячении со слабой серной кислотой — галловую кислоту, также не вполне отвечает фактам, ибо, как в настоящее время известно, и патологические Д. вещества могут, хотя и не столь успешно, служить для дубления, а кроме того, таннин, например, являясь по преимуществу патологическим Д. веществом, встречается, по-видимому, и как нормальный продукт (сумах, альгаробилла, мироболаны). Как кислоты, Д. вещества образуют металлические производные — соли, из которых свинцовые, представляющие нерастворимые в воде аморфные осадки, нередко применяются для извлечения Д. вещества из водных экстрактов Д. материалов, а также при анализе.
Способы получения
Для получения дубильного вещества в чистом состоянии природные дубильные материалы экстрагируют водой или другими растворителями: крепким или слабым спиртом, чистым эфиром или в смеси со спиртом, уксусным эфиром и т. п.; экстракты выпаривают, и получаемые в остатке дубильные вещества очищают с помощью обработки их теми или другими из указанных растворителей. Чаще, приготовив водный или водно-спиртовый экстракт, извлекают из него дубильное вещество взбалтыванием с уксусным или простым эфиром или с их смесью или же осаждают (лучше фракционированно) уксуснокислым свинцом и, отфильтровав, разлагают осадки свинцовых соединений сернистым водородом. По-видимому, последний способ, практиковавшийся весьма часто прежними исследователями, не всегда дает удовлетворительные результаты в смысле чистоты получаемых продуктов (Etti). Пользуются иногда для осаждения дубильных веществ из водных экстрактов уксуснокислым хинином, уксуснокислою медью, рвотным камнем, поваренною солью, соляной кислотой и др. Для очищения прибегают иногда к помощи диализа, дающего с таннином хорошие результаты (Löwe, Biedel).
Описание отдельных Д. веществ
При описании Д. веществ необходимо подробно остановиться лишь на немногих важнейших для практики и лучше исследованных.
Таннин
Таннин, галлодубильная кислота или просто Д. кислота (Galläpfelgerbsäure, Gallusgerbsäure, acide gallotannique), находится в различных сортах чернильных орешков, патологических кнопперсах, сумахе, альгаробилле, мироболанах; имеет состав C14H10O9; представляет вяжущего вкуса аморфный порошок, растворимый в воде, спирте и уксусном эфире, нерастворимый в эфире, бензоле и др.; оптически недеятелен; дает с хлорным железом в водном растворе чёрно-синий осадок, что применяется как качественная реакция на соли окиси железа; легко окисляется, поглощая в присутствии щелочей кислород из воздуха и восстановляя закись меди из солей её окиси и соли серебра; осаждается из водных растворов (в отличие от галловой кислоты) клеем, сырой кожей, алкалоидами, альбуминатами, слабыми соляной и серной кислотами и многими солями (напр., поваренной). По Бёттингеру (1888), соединение таннина с клеем содержит около 34 % таннина. Таннин разлагает углекислые соли, обнаруживая ясно кислотные свойства. Его соли аморфны, в основном нерастворимы и своим составом указывают на присутствие в его частице лишь одного карбоксила (H. Schiff). При нагревании до 210° таннин дает пирогаллол; при кипячении с слабой серной кислотой или едким кали превращается нацело в галловую кислоту [Различные сорта продажного таннина дают при этом также изменчивые количества глюкозы, что и дало повод Штреккеру и др. рассматривать таннин как глюкозид галловой кислоты. Однако вполне чистый таннин, полученный, например, экстрагированием уксусным эфиром, не образует ни следов глюкозы (Löwe). Возможно, что в продажных сортах в виде подмеси находится глюкозид, но не галловой кислоты, а таннина (H. Schiff).], при кипячении с водным аммиаком распадается на галламид и галловокислый аммиак (Etti, 1884), подобно тому как ангидрид молочной кислоты дает амид этой кислоты и её аммиачную соль; при кипячении с уксусным ангидридом образует пятиацетильный эфир C14H5(C2H3O)5O9. Эти реакции определяют строение таннина как дигалловой кислоты, представляющей ангидрид галловой
С6H2(OH) 3 СО—О—С 6H2 (ОН) 2 СОНО.
В подтверждение такого строения таннина Г. Шиффом (1873) получена из галловой кислоты при нагревании её с хлорокисью фосфора, а также при выпаривании её водного раствора с мышьяковой кислотой, дигалловая кислота по уравнению
2C6H2(OH)3COHO — H2O = С 6H2 (OH) 3 СО—О—С 6H2 (OH) 2 СОНО
по своим свойствам, реакциям и производным тождественная с таннином.
Таннин находит обширное применение в медицине, в производстве чернил, красильном деле, для получения галловой кислоты и пирогаллола, но для дубления кож не применяется). Кроме дигалловой кислоты, Шиффом получены искусственно ангидриды и других многоатомных фенолокислот, а также сульфофенолокислот, со свойствами Д. веществ и близкие к таннину. Сюда относятся: динитрогалло- и дифлороглюцинкарбоновые кислоты, полученные (1888) при действии хлорокиси фосфора на соответствующие изомеры галловой кислоты и имеющие состав C14H10O9.
При кипячении протокатеховой кислоты с мышьяковой получена (1882) дипротокатеховая кислота C14H10O7 = 2C7H6O4 — H2O, показывающая все реакции, свойственные таннину, также при кипячении с минеральными кислотами дающая обратно протокатеховую кислоту, с аммиаком её амид и аммиачную соль, но с хлорным железом в отличие от таннина дающая зелёное окрашивание. При действии хлорокиси фосфора протокатеховая кислота образует ещё тетрапротокатеховую кислоту C28H18O13 = 4С7H6O4 — 3Н2O, по окрашиванию с хлорным железом и др. свойствам сходную с предыдущей.
Эллагогендубильная кислота
Стоит в близком отношении к таннину, являясь, как и он, производным галловой кислоты, и часто встречается вместе с ним в растениях. Она составляет главную массу Д. вещества мироболанов, альгаробилл, диви-диви (см. Дубящие материалы) и, вероятно, коры корней граната (Löwe 1875, Zöllfel 1891), а также найдена вместе с дубодубильной кислотой C16H14O9 в древесине черешчатого дуба (Etti 1889). Высушенная при 100°, она представляет состав C14H10O10 и вид буроватой аморфной массы; растворима в воде, спирте и уксусном эфире; образует чёрно-синий осадок с уксуснокислым железом и осадки с клеем, белком, алкалоидами и рвотным камнем; при нагревании с водой до 110° переходит в эллаговую кислоту, теряя при этом 2Н2О, и образует с уксусным ангидридом пятиацетильный эфир. Zöllfel приписывает ей строение, выражаемое формулой С6Н2(ОН) 3 СО—О—О—С 6 Н2 (ОН) 2 СООН = 2C 6H2(OH) З COHO — H2. Эллаговая кислота C14H6O8 +2Н2О добывается из предыдущей или непосредственно из диви-диви; найдена во многих Д. материалах, где, быть может, образуется на счет эллагогендубильной кислоты, получается искусственно из галловой кислоты при разнообразных условиях по уравнению: 2C7H6O5 = C14H6O8 + 2H2O + H2, напр., при нагревании её с мышьяковой к. (Löwe 1868, H. Schiff 1873), при нагревании её этилового эфира с раствором соды (Н. Schiff 1879) и мн. др. Она представляет желтоватый кристаллический порошок; трудно растворима в воде и спирте, нерастворима в эфире; теряет при 100° всю кристаллизационную воду, поглощая её обратно во влажном воздухе, если не была нагрета выше 120°; с хлорным железом дает сперва зелёное и затем чёрно-синее окрашивание, а с азотной и азотистой кислотами в присутствии воды — кроваво-красное (характерно); образует четырёхацетильный (H. Schiff, Zöllfel) и такой же бензольный (Goldschmidt u. Jahoda 1892) эфиры; хотя ей и отвечают разнообразного состава труднорастворимые микрокристаллические или аморфные соли, однако кислотные её свойства выражены слабо, и угольную кислоту из углекислых солей она вытесняет с трудом; при восстановлении амальгамой натрия дает как конечный продукт γ-гексаоксидифенил С12Н4(ОН)6, который образуется из неё также вместе с β-гексаоксидифенилом при плавлении с едким натром; при кипячении с концентрированным раствором едкого кали превращается в гексаоксидифениленкетон C13H8O7, а при перегонке с цинковой пылью во флуорен С13Н10. Строение её не вполне выяснено.
Дубодубильные кислоты
Находятся в молодой коре (Eichenrindegerbs ä ure), древесине (Eichenholzgerbs ä ure) и листьях различных видов дуба. Кислоте (из коры), содержащей в круглых числах 56 % углерода и 4 % водорода и дающей с хлорным железом синее окрашивание, Этти (1880, 1883) дает формулу C17H16O9, а Беттингер (1887) C19H16O10 [Аналитические данные Леве (1881) хорошо согласуются с формулой Этти.]. Из одной дубовой коры Этти получил Д. кислоту состава C18H18O9, из коры Quercus pubescens C20H20O9, из экстракта древесины черешчатого дуба (Qu. pedunculata) C16H14O9, a из этой последней действием соляной кисл. C15H12O9 (1889). К группе дубодубильных кислот Этти причисляет также Д. кислоту из коры красного бука состава C20H22O9 и из шишек хмеля состава C22H26O9. Д. вещество чайных листьев, по Рохледеру, есть также дубодубильная кисл. Дубодубильные кислоты представляют аморфные порошки различных оттенков от буро-красного до светло-красного цвета (C15H12O9 желт.), растворимые в воде (за исключением кислоты C16H14O9, которая почти не растворима), спирте, смеси спирта с эфиром, уксусном эфире и трудно растворимые в чистом эфире; имеют в водном растворе кислую реакцию; растворяются в щелочах; с уксуснокислым свинцом дают желтовато-белые осадки свинцовых соединений; с окисью магния образуют растворимые в воде средние и кислые соли (Etti); с хлорным железом кислоты C17H16O9 (или C19H16O10, по Беттингеру) и C16H14O9 дают синие осадки, прочие зелёные; осаждаются клеем (осадок, по Беттингеру, содержит около 43 % дубодубильной кислоты) и по действию на кожу являются типическими Д. веществами.
Весьма характерна для дубодубильных кислот способность, вполне отсутствующая у таннина, образовать ангидриды при нагревании до 130°—140° и при кипячении со щелочами и разведенными минеральными кислотами. При этом, по Этти, две частицы Д. кислоты теряют одну или более частиц воды (до пяти, смотря по условиям и числу незамещенных водных остатков в частице кислоты). Кислота C17H16O9, например, дает 4 ангидрида C34H30O17 (флобофен), C34H28O16, C34H26O15 (дубовое красное) и C34H24O14 [Но не дает ни следов какого-либо сахаристого вещества ни при кипячении с H2SO4, ни при действии эмульсии (Etti, Löwe).].
Некоторые из этих ангидридов находятся готовыми в дубовой коре (флобофен и дубовое красное, Eichenroth), составляя такое же Д. начало её, как и сами кислоты. Они имеют вид аморфных, в основном красных или буро-красных порошков, трудно или нерастворимы в чистой воде, но растворимы в ней в присутствии дубодубильной кислоты, а также в спирте и щелочах. Ангидриды, представляющие предел дегидратации Д. кислот, в спирте и щелочах не растворяются. Флобофен и дубовое красное к хлорному железу, клею, коже, уксуснокислому свинцу относятся одинаково с самой Д. кислотой и подобно ей восстановляют Фелингову жидкость. Ангидриды эти обратно воды не присоединяют ни при каких условиях (Etti). Кислота C17H16O9 при сухой перегонке дает пирокатехин и вератрол С6Н4(ОСН3)2, при плавлении с едким кали пирокатехин, протокатеховую кислоту и флороглюцин, при кипячении с слабой H2SO4 галловой кислоты не образует (отличие от таннина) и лишь с трудом и в малом количестве при нагревании с нею в запаянной трубке до 130°—140°, с крепкой соляной кислотою при 150°—180° отщепляет метильные группы в виде хлористого метила (Etti). Эти реакции в основном свойственны и др. дубодубильным кислотам. Кислота C16H14O9 с соляною кислотой, отщепляя СН3, переходит отчасти в кислоту C15H13O9 с одним СН3 в составе, который и выделяется в виде йодистого метила при кипячении с йодистым водородом (Etti [Замечательно, что ангидриды дубодубильных кислот, в противоположность самим кислотам, не способны отщеплять CH3 J при действии HJ (Etti).]). Для этой же кислоты C16H14O9 получены гидроксиламинное и фенилгидразинное производные, что указывает на присутствие в её составе карбонильной группы СО. Ацетильные производные дубодубильных кислот изучены недостаточно. Получение их в чистом состоянии затрудняется, по-видимому, легкостью, с которою дубодубильные кислоты переходят в ангидриды в кислой среде. Ацетильному производному кислоты из экстракта дубовой древесины Беттингер дает состав С15Н7(СН3О)5О9, что находится в согласии с данными Этти для строения полученных им кислот C16H14O9 и C15H12O9.
Кинодубильная кислота
Кинодубильная кислота
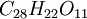 (Kin oroth) составляет главную массу кино (см. Дубильные материалы) и представляет ангидрид киноина
(Kin oroth) составляет главную массу кино (см. Дубильные материалы) и представляет ангидрид киноина 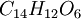 , из кот. может быть получена нагреванием при 120°—130°. Киноин также находится в кино, бесцветен, кристалличен и растворим в воде, спирте и немного в эфире. Он клеем не осаждается, а с хлорным железом дает красное окрашивание и, следовательно, не обладает характерными свойствами Д. веществ. Наоборот, в ангидриде его
, из кот. может быть получена нагреванием при 120°—130°. Киноин также находится в кино, бесцветен, кристалличен и растворим в воде, спирте и немного в эфире. Он клеем не осаждается, а с хлорным железом дает красное окрашивание и, следовательно, не обладает характерными свойствами Д. веществ. Наоборот, в ангидриде его 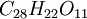 они явственно развиты и обусловливают применение кино как дубла. Кинодубильная кислота представляет красное аморфное смолистое вещество, растворимое в спирте и трудно растворимое в холодной воде, дающее осадок с клеем и грязно-зелёное окрашивание с
они явственно развиты и обусловливают применение кино как дубла. Кинодубильная кислота представляет красное аморфное смолистое вещество, растворимое в спирте и трудно растворимое в холодной воде, дающее осадок с клеем и грязно-зелёное окрашивание с 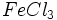 . При нагрвании до 160°—170° или при кипячении с слабыми серной или соляной кислотами она переходит в ангидрид
. При нагрвании до 160°—170° или при кипячении с слабыми серной или соляной кислотами она переходит в ангидрид 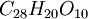 с подобными же свойствами. Как сам киноин, так и кинодубильная кислота с соляной кислотой в запаянной трубке при 120°—130° распадаются на пирокатехин, галловую кислоту и хлористый метил. На основании этой реакции Этти считает киноин за метиловый эфир пирокатехингалловой кислоты (1878).
с подобными же свойствами. Как сам киноин, так и кинодубильная кислота с соляной кислотой в запаянной трубке при 120°—130° распадаются на пирокатехин, галловую кислоту и хлористый метил. На основании этой реакции Этти считает киноин за метиловый эфир пирокатехингалловой кислоты (1878).Катехудубильные кислоты
Находятся вместе с катехинами близкого между собою состава в различных сортах катеху и в гамбире (см. также Дубильные материалы). Они представляют ангидриды катехинов, из которых могут быть получены и искусственно простым нагреванием до 130—170°, кипячением с содой или нагреванием с водой при 110°. Состав катехинов, высушенных при температуре около 100° (они содержат до 5 паев кристаллизационной воды, которую и теряют при этой температуре), выражается формулами
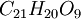 (Liebermann u. Teuchert 1880),
(Liebermann u. Teuchert 1880), 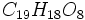 ,
, 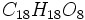 (Etti, Hlasiwetz) и др. Катехины кристаллизуются в форме очень мелких иголочек светло-жёлтого цвета, дают с
(Etti, Hlasiwetz) и др. Катехины кристаллизуются в форме очень мелких иголочек светло-жёлтого цвета, дают с 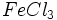 зелёное окрашивание, но клеем не осаждаются, при плавлении с КНО распадаются на флороглюцин и протокатеховую кислоту, а при сухой перегонке образуют пирокатехин. Для катехина
зелёное окрашивание, но клеем не осаждаются, при плавлении с КНО распадаются на флороглюцин и протокатеховую кислоту, а при сухой перегонке образуют пирокатехин. Для катехина 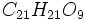 получены двуацетильный и двубензоильный эфиры (Lieb. u. Teuch.). Катехин
получены двуацетильный и двубензоильный эфиры (Lieb. u. Teuch.). Катехин 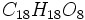 при 140° с разведенной серной кислотой распадается на флороглюцин и пирокатехин. С
при 140° с разведенной серной кислотой распадается на флороглюцин и пирокатехин. С 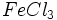 он реагирует подобно пирокатехину, а с древесиной сосны — подобно флороглюцину, представляя как бы молекулярное соединение этих двух фенолов
он реагирует подобно пирокатехину, а с древесиной сосны — подобно флороглюцину, представляя как бы молекулярное соединение этих двух фенолов 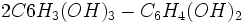 (Etti). Катеху-Д. кислоты, по Этти (1877—81), имеют состав
(Etti). Катеху-Д. кислоты, по Этти (1877—81), имеют состав 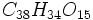 ,
, 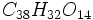 и
и 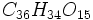 и представляют красновато-бурые аморфные порошки с характерными свойствами Д. веществ. Нагреванием катехинов до более высокой температуры или с минеральными кислотами получены ангидриды, образованные с ещё большею потерею воды (Etti).
и представляют красновато-бурые аморфные порошки с характерными свойствами Д. веществ. Нагреванием катехинов до более высокой температуры или с минеральными кислотами получены ангидриды, образованные с ещё большею потерею воды (Etti).Маклурин
Маклурин, или моринодубильная кислота,
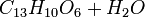 (Hiasiwetz 1863, Benedict 1877) и морин
(Hiasiwetz 1863, Benedict 1877) и морин 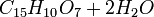 (Löwe 1875, Benedict u. Hazura 1884) находятся в жёлтом дереве (Morus tinctoria или Maclura aurantiaca, применяется в красильном деле), откуда их извлекают кипячением с водой и разделяют, пользуясь меньшею растворимостью морина в воде. Маклурин, светло-жёлтый кристаллический порошок, из свойств, характеризующих Д. вещества, обладает лишь способностью давать с железом (смесью закиси и окиси) чёрно-зелёный осадок и осаждаться клеем, алкалоидами и альбуминатами, но для дубления неприменим. Подобно многим Д. веществам, он распадается на флороглюцин и протокатеховую кислоту по уравнению:
(Löwe 1875, Benedict u. Hazura 1884) находятся в жёлтом дереве (Morus tinctoria или Maclura aurantiaca, применяется в красильном деле), откуда их извлекают кипячением с водой и разделяют, пользуясь меньшею растворимостью морина в воде. Маклурин, светло-жёлтый кристаллический порошок, из свойств, характеризующих Д. вещества, обладает лишь способностью давать с железом (смесью закиси и окиси) чёрно-зелёный осадок и осаждаться клеем, алкалоидами и альбуминатами, но для дубления неприменим. Подобно многим Д. веществам, он распадается на флороглюцин и протокатеховую кислоту по уравнению: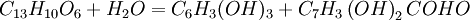 .
.Такое распадение происходит количественно при кипячении его с крепким раствором едкого кали или при 120°C с слабою серною кислотою и указывает на эфирную натуру этого вещества. Морин, составляющий красящее начало жёлтого дерева и кристаллизующийся из водного раствора в форме длинных блестящих игл, за исключением зелёного окрашивания с хлорным железом, типических свойств Д. веществ не представляет. При плавлении с едким кали в качестве главных продуктов распадения он дает резорцин и флороглюцин, при восстановлении амальгамой натрия образует флороглюцин, причём сперва переходит в изоморин (пурпурно-красные призмы), легко превращающийся обратно в морин. Как морин, так и маклурин образуют с металлами частью кристаллические, частью аморфные соли, состав которых нельзя считать установленным
См. также
При написании этой статьи использовался материал из Энциклопедического словаря Брокгауза и Ефрона (1890—1907).
Wikimedia Foundation. 2010.
