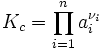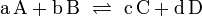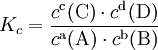- Действующих масс закон
-
Закон действующих масс устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии. Закон действующих масс сформулирован в 1864—1867 гг. К. Гульдбергом и П. Вааге. Согласно этому закону скорость, с которой вещества реагируют друг с другом, зависит от их концентрации. Закон действующих масс используют при различных расчетах химических процессов. Он позволяет решить вопрос, в каком направлении возможно самопроизвольное течение рассматриваемой реакции при заданном соотношении концентраций реагирующих веществ, какой выход нужного продукта может быть получен.
Общая формула
где
- ai — активности веществ, выраженные через концентрации, парциальные давления либо мольные доли;
- νi — стехиометрический коэффициент (для исходных веществ принимается отрицательным, для продуктов — положительным);
- Kc — константа химического равновесия
На практике в расчётах, не требующих особой точности, значения активности обычно заменяются на соответствующие значения концентраций (для реакций в растворах) либо парциальных давлений (для реакций между газами).
Пример: для стандартной реакции
константа химического равновесия определяется по формуле
При постоянной температуре отношение равновесных концентраций (парциальных давлений) конечных продуктов к равновесным концентрациям (парциальным давлениям) исходных реагентов, возведенных соответственно в степени, равные их стехиометрическим коэффициентам, величина постоянная
Wikimedia Foundation. 2010.