- Thermus aquaticus
-
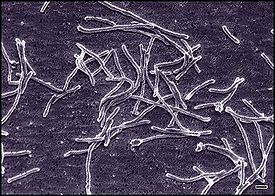
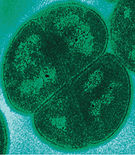
Thermus aquaticus Научная классификация Царство: Бактерии Тип: Deinococcus-Thermus Класс: Deinococci Порядок: Thermales Семейство: Thermaceae Род: Thermus Вид: Thermus aquaticus Латинское название Thermus aquaticus Brock et Freeze, 1969 NCBI 271 Thermus aquaticus — грамотрицательная палочковидная экстремально термофильная бактерия рода Thermus. Обитает в горячих источниках Йеллоустонского национального парка и других подобных регионах, гейзерах при температурах выше 55 °C. Впервые открыта Томасом Броком (англ. Thomas Brock) и Хадсоном Фризом (англ. Hudson Freeze) в районе Больших Фонтанов (англ. Great Fountain) Йеллоустонского национального парка. Термостабильные ферменты (в особенности термостабильная полимераза TaqPol) используются как инструменты в молекулярно-генетических исследованиях.
Содержание
Биологические свойства
Грамотрицательная палочковидная бактерия. Не образует капсул и спор, часть штаммов подвижно и имеют жгутики. На солнечном свету продуцирует разнообразные пигменты [1]. Экстремально-термофильный хемоорганогетеротроф, облигатный аэроб[2], развивается при температуре выше 55 °С(оптимальной является температура 70 °C). Обитает в горячих источниках, гейзерах[2], два штамма были выделены из горячей водопроводной воды[3]
Геном
Геном T. aquaticus штамма HB27 представлен хромосомой размером 1894877 п.н. и мегаплазмидой pTT27 размером 232605 п.н. Имеется большое сходство генома T. aquaticus с геномом мезофильного организма Deinococcus radiodurans[4]. Продолжается секвенирование генома T. aquaticus штамма Y51MC23, размер хромосомы составляет 2340768 п.н., хромосома содержит 2570 гена, из которых 2520 кодируют белки, процент % Г+Ц пар составляет 68 %[5]. T, aquaticus штамм NTU103 имеет плазмиду pTA103 размером 1965 п.н., которая реплицируется по типу «катящегося кольца»[6]. T. aquaticus поражается бактериофагом IN93, чей геном представлен двуцепочечной кольцевой молекулой ДНК размером 19603 п.н.[7].
Термостабильные ферменты
T. aquaticus является экстремально-термофильной бактерией, поэтому ферменты T. aquaticus термостабильны и не инактивируются при повышенных температурах. Некоторые ферменты T. aquaticus (Taq1 рестриктаза и в особенности Taq-полимераза) активно используются в качестве инструментов для молекулярно-генетических исследований[8].
Альдолаза
Первоначально не было понятно, как T. aquaticus может выживать в экстремальных температурных условиях, поэтому необходимо было детально изучить ферменты T. aquaticus и как они избегают денатурации при таких повышенных температурах. Одними из первых изученных ферментов T. aquaticus были альдолаза[9].
РНК-полимераза
Первым полимеразным ферментом, выделенным из T. aquaticus была РНК-полимераза (транскриптаза) в 1974 г.[10] Проведены кристаллографические исследования данного фермента[11] и получена рекомбинантная РНК-полимераза, предназначенная для молекулярно-биологических исследований транскрипции[12].
Taq1-рестриктаза
Рестриктаза Taq1 была одним из первых ферментов T. aquaticus, использовавшихся для молекулярно-генетических исследований[13]. Сайт рестрикции — TCGA.
Taq полимераза
Taq полимераза была впервые выделена в 1976 г.[14]. Преимуществами Taq полимеразы является её способность работать при повышенных температурах (оптимум 72—80 °C) и возможность получать Taq полимеразу в чистом виде. В 1986 г. Кери Маллис (англ. Kary Mullis) решил использовать для изобретённой им в 1983 г. полимеразной цепной реакции (ПЦР) Taq полимеразу ввиду того, что она выдерживала высокую (94—96 °C) температуру, необходимую для денатурации ДНК и не было необходимости вносить новую порцию дорогостоящей ДНК-полимеразы после каждого раунда амплификации. Затем ген Taq полимеразы был клонирован и модифицирован с целью получить высокоэффективный коммерческий продукт[15]. Taq полимераза гомологична ДНК-полимеразе I (pol I) Escherichia coli[16]. Taq полимераза также ограниченно используется в секвенировании ДНК[17], но ввиду большого количества ошибок[18] (из-за отсутствия 3'-5' экзонуклеазной активности) в секвенировании и точных анализах чаще используется Pfu полимераза из археи Pyrococcus furiosus[19] (хотя полимераза AmpliTaqR имеет преимущество перед Pfu полимеразой в виде более высокой процессивности[20]).
Применение
T. aquaticus является источником термостабильных ферментов, используемых в молекулярной биологии (Taq1-рестриктаза, РНК-полимераза, Taq полимераза). Секвенирование генома T. aquaticus может помочь в помощи других необходимых для биотехнологии ферментов (протеаз[21], амиломальтазы[22], НАД оксидаз[23]).
См. также
Примечания
- ↑ Brock T. D.,Mercedes R. E. Fine Structure of Thermus aquaticus, an Extreme Thermophile// Journal of Bacteriology, Oct 1970, Vol 104. р. 509—517.
- ↑ 1 2 Brock T.D. and Freeze H. (1969). «Thermus aquaticus gen. n. and sp. n., a nonsporulating extreme thermophile». Journal of Bacteriology 98 (1): 289-97. PMID 5781580.
- ↑ Pask-Hughes R. and Williams R.A.D. (1975). «Extremely thermophilic gram-negative bacteria from hot tap water». Journal of General Microbiology 88 (2): 321-8. DOI:10.1099/00221287-88-2-321. PMID 1097586.
- ↑ The genome sequence of the extreme thermophile : Thermus thermophilus : Abstract : Nature Biotechnology
- ↑ uid=6010 Genome Result
- ↑ ScienceDirect — Plasmid : Characterization of a rolling-circle replication plasmid from Thermus aquaticus NTU103
- ↑ uid=16835 Genome Result
- ↑ Thermostable DNA Polymerases
- ↑ Freeze H., Brock T.D. Thermostable Aldolase from Thermus aquaticus//J. Bact. 1970, vol. 101(2) pp. 541—550
- ↑ Air G.M., Harris J.I. DNA-Dependent RNA Polymerase From the Thermophilic Bacterium Thermus aquaticus // FEBS Letters 1974, vol. 38(3) pp. 277—281
- ↑ http://www.aps.anl.gov/Science/Reports/1999/darsts2.pdf
- ↑ Recombinant Thermus aquaticus RNA Polymerase, a New Tool for Structure-Based Analysis of Transcription — Minakhin et al. 183 (1): 71 — The Journal of Bacteriology
- ↑ Sato S. A single cleavage of Simian virus 40 (SV40) DNA by a site specific endonuclease from Thermus aquaticus, Taq I // J. Biochem (Tokyo), 1978 83 (2) Р. 633
- ↑ Deoxyribonucleic acid polymerase from the extreme thermophile Thermus aquaticus
- ↑ High-level expression, purification, and enzymatic… [PCR Methods Appl. 1993] — PubMed result
- ↑ Crystal structure of Thermus aquaticus DNA polymerase
- ↑ DNA sequencing with Thermus aquaticus DNA polymerase and direct sequencing of polymerase chain reaction-amplified DNA — PNAS
- ↑ Thermus aquaticus (Taq) error rates adn REP-PCR | British Journal of Biomedical Science | Find Articles at BNET
- ↑ ФЕРМЕНТЫ ДЛЯ МОЛЕКУЛЯРНОЙ БИОЛОГИИ И ГЕНЕТИЧЕСКОЙ ИНЖЕНЕРИИ. Национальный информационный центр по науке и инновациям Sciencerf.ru. В МИРЕ НАУКИ
- ↑ ДНК полимеразы | molbiol.ru
- ↑ http://cancerweb.ncl.ac.uk/cgi-bin/omd?Thermus+aquaticus+Rt41A+proteinase
- ↑ Thermus aquaticus ATCC 33923 Amylomaltase Gene Cloning and Expression and Enzyme Characterization: Production of Cycloamylose - Terada et al. 65 (3): 910 - Applied and Environ...
- ↑ NADH oxidase from the extreme thermophile Thermus aquaticus YT-1 — COCCO — 2005 — European Journal of Biochemistry — Wiley Online Library
Ссылки
- Thermus aquaticus
- Thermus Brock and Freeze 1969
- Terrestrial Life in Extreme Environments
- History of PCR
- Thermus aquaticus Y51MC23
- The Microbiology of Thermus Aquaticus
 Категории:
Категории:- Бактерии по алфавиту
- Экстремофилы
Wikimedia Foundation. 2010.