- Простые эфиры
-
Простые эфиры — органические вещества, имеющие формулу R-O-R1, где R и R1 — углеводородные радикалы. Следует однако учитывать, что такая группа может входить в состав других функциональных групп соединений, не являющихся простыми эфирами (см. Кислородсодержащие органические соединения).
Содержание
Способы получения
- по Вильямсону
в лабораторных условиях эфиры получают по Вильямсону взаимодействием галогенопроизводных, способных вступать в реакцию Sn2 и алкоксид- и феноксид-ионами. Реакция протекает гладко с галогенметаном и первичными галогеналканоми. В случае вторичных галогеналканов реакция может быть осложнена побочной реакцией элиминирования.
Физические свойства
Простые эфиры — подвижные легкокипящие жидкости, малорастворимые в воде, очень легко воспламеняющиеся. Проявляют слабоосновные свойства (присоединяют протон по атому O).
Методы синтеза
- Межмолекулярная дегидратация спиртов:
- Реакция алкоголятов с галогеноуглеводородами:
- Ароматические эфиры можно получить реакцией фенола с органическими сульфатами в присутствии щёлочей:
Реакции
Простые эфиры образуют перекисные соединения под действием света:
Вследствие этого при перегонке простых эфиров в лабораторных условиях запрещается перегонять их досуха, поскольку в этом случае произойдёт сильный взрыв в результате разложения пероксидов.
Важнейшие эфиры
Название Формула Температура плавления Температура кипения Диметиловый эфир CH3OCH3 −138,5 °C −24,9 °C Диэтиловый эфир CH3CH2OCH2CH3 −116,3 °C 34,6 °C Диизопропиловый эфир (CH3)2CHOCH(CH3)2 −86,2 °C 68,5 °C Анизол 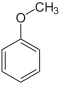
−37 °C 154 °C Оксиран 
−111,3 °C 10,7 °C Тетрагидрофуран 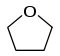
−108 °C 65,4 °C Диоксан 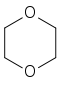
11.7 °C 101.4 °C Полиэтиленгликоль HOCH2(CH2OCH2)nCH2OH − − Литература
- Химия. Справочное руководство. Пер. с нем. Л., Химия 1975, сс. 240—242.
См. также
Категория:- Простые эфиры
Wikimedia Foundation. 2010.





![\mathsf {2CH_3CH_2OCH_2CH_3 + O_2 \xrightarrow[]{h\nu} 2CH_3CH_2OOCH_2CH_3}](bc1dd640fa63182045f2f17d909c0b09.png)