- Фторид брома(III)
-
Фторид брома(III) 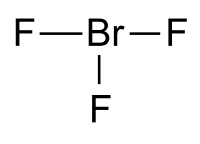
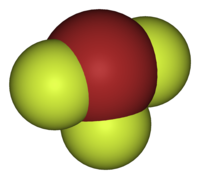
Общие Систематическое наименование Фторид брома (III) Химическая формула BrF3 Физические свойства Отн. молек. масса 137 а. е. м. Молярная масса 136,90 г/моль Плотность (тв.) 3,2 г/см3 ,(жидк) 2,8 г/см³ Термические свойства Температура плавления 8,8 °C Температура кипения 125,8 °C Классификация Рег. номер CAS 7787-71-5 Фторид брома(III) (трифторид брома, трёхфтористый бром) BrF3 — соединение брома с фтором, представляющее собой при комнатной температуре подвижную бесцветную жидкость, иногда окрашенную желтовато-серым или соломенным цветом (за счёт разложения вещества с образованием бурого брома), дымящую на воздухе. Обладает сильным раздражающим запахом.
Содержание
Строение
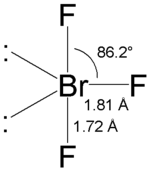
Гибридизация атома брома в молекуле sp³d, а строение молекулы полностью аналогичное строению молекулы трифторида хлора, то есть Т-образное, с одной длинной связью и двумя более короткими.
Для трифторида брома также изучена кристаллическая решётка. Кристаллическая ячейча — орторомбическая. Параметры ячейки: [1]
Параметр Значение a 534 пм b 735 пм c 661 пм Предположительно, в узлах кристаллической решётки находятся ионы [BrF2]+ и [BrF4]−.
Физико-химические свойства
Дипольный момент молекулы составляет 1.19 Дебая.
Термодинамические величины
Свойство Значение Стандартная энтальпия образования (в жидкой фазе) −300,8 кДж/моль Стандартная энтальпия образования (в газовой фазе) −255,6 кДж/моль Энтропия образования (в жидкой фазе) 178,2 Дж/(моль·К) Энтропия образования (в газовой фазе) 292,5 Дж/(моль·К) Теплоёмкость (в жидкой фазе) 124,6 Дж/(моль·К) Теплоёмкость (в газовой фазе) 66,6 Дж/(моль·К) Энтальпия плавления 12,03 кДж/моль Энтальпия кипения 42,68 кДж/моль[2] Растворимость
Растворитель Значение Жидкий бром Не смешивается Вода Реагирует Серная кислота Растворим Фтороводород Неограничено смешиваются
(при температуре выше 292К).Хорошо растворяет фториды некоторых металлов, например NaF, KF, AgF, SnF2, BaF2, править] Химические свойства
- Воспламеняет многие органические соединения (в частности, бумагу и древесину).
- В жидком состоянии подвергается автоионизации по следующей схеме:
- Многие фториды металлов при расторении образуют двойные соединения, которые в большинстве своём устойчивы к нагреванию, и теряют BrF3 лишь при температурах выше 200 °C. Например при растворении в трифториде брома фторида калия выделяется следующее соединение:
Получение
- Трифторид брома можно получить из простых веществ при комнатной температуре (20 °C)
- Также, трифторид брома является продуктом диспропорционирования монофторида брома. При этом также образуется свободный бром:
Применение
BrF3 нашел достаточно большой спектр различных вариантов применения. Вот некоторые из них:
- Трифторид брома — очень хороший фторирующий агент. Он используется во всевозможных органических синтезах. Например, в реакции с сукциннитрилом (NCCH2CH2CN) образуется 1,1,1,4,4,4-гексафторбутан, который сложно получить, если использовать другие фторирующие агенты.[4]
- На основе системы литий/трифторид брома разрабатывается достаточно перспективный источник тока.[5]
- Также трифторид можно использовать для травления кристаллов кремния в газовой фазе, что может успешно применяться для производства различных полупроводниковых приборов.[6]
- Успешно применяется в ядерной промышленности для получения и разделения фторидов урана, а также является перспективным для переработки ядерного топлива:
- Для некоторых синтезов, трифторид брома выступает одновременно в роли растворителя, фторирующего агента и окислителя. Например, реакция с трихлоридами металлов, в которой образуются соли фторпроизводных кислот:
Опасности
Трифторид брома является достаточно опасным веществом. Среди опасностей связанных с применением этого вещества можно выделить следующие:[7]:
- Вероятность взрыва от удара, трения или искры.
- Токсичен для вдыхания и попадание внутрь организма.
- Оставляет серьёзные плохозаживающие ожоги при попадании на кожу.
Примечания
- ↑ X-Ray investigation of the structure of liquid Bremine Trifluoride. V.N. Mitkin, G.S. Yurev, S.V. Zemskov, V.I. Kazakova. Journal of Structural Chemistry Volume 28, Number 1, 1987.
- ↑ Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977
- ↑ Simons JH (1950). «Bromine (III) Fluoride — Bromine Trifluoride». Inorganic Synthesis 3: 184—186
- ↑ Max T. Baker, Jan A. Ruzicka, John H. Tinker. Journal of Fluorine Chemistry Volume 94, Issue 2, Pages 123—126
- ↑ Патент США № 5188913
- ↑ Патент США № 6436229
- ↑ Данные о опасности соединения
См. также
Литература
- Джолли У. И. Синтезы неорганических соединений. М:Мир., 440 с. — 1967 г.
- Некрасов Б. В. Основы общей химии. В 2-ух томах., М:Химия, 1973 г.
Соединения бромаБромат калия (KBrO3) • Бромат кальция (Ca(BrO3)2) • Бромат натрия (NaBrO3) • Бромат серебра (AgBrO3) • Бромат стронция (Sr(BrO3)2) • Броматы • Бромид алюминия (AlBr3) • Бромид бора(III) (BBr3) • Бромид диртути(2+) (Hg2Br2) • Бромид магния (MgBr2) • Бромид меди(I) (CuBr) • Бромид меди(II) (CuBr2) • Бромиды • Бромистая кислота (HBrO2) • Бромистоводородная кислота (HBr) • Бромная кислота (HBrO4) • Бромноватая кислота (HBrO3) • Бромноватистая кислота (HBrO) • Бромопентакарбонилрений(I) (Re(CO)5Br) • Броморганические соединения • Гипобромистая кислота (HOBr) • Диоксид брома (BrO2) • Оксид брома (Br2O) • Пербромат калия (KBrO4) • Фторид брома(I) (BrF) • Фторид брома(III) (BrF3) • Фторид брома(V) (BrF5) • Хлорид брома (BrCl)
Категории:- Соединения брома
- Межгалоидные соединения
- Фториды
Wikimedia Foundation. 2010.