- Гексахлорэтан
-
Гексахлорэтан 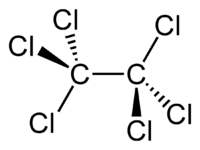
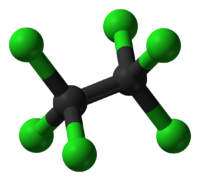
Общие Систематическое наименование гексахлорэтан Химическая формула C2Cl6 Физические свойства Молярная масса 236.74 г/моль Термические свойства Гексахлорэта́н (перхлори́д) C2Cl6 — бесцветные кристаллы со слабым запахом камфоры.
Вещество сублимируется в открытых сосудах. Гексахлорэтан умеренно растворим в спирте и эфире, хорошо — в CS2, растворимость в воде 0,005 % (22,3 °С); образует азеотропную смесь с водой (т. кип. 99 °С, 33,9 % гексахлорэтана).
Гексахлорэтан гидролизуется твёрдой щёлочью при 200 °С и выше, а также спиртовым раствором щёлочи до щавелевой кислоты. В газовой фазе при 500—600 °С (или при 350—450 °С в присутствии активировированного угля) разлагается с образованием ССl4 и тетра-хлорэтилена. Под действием цинка в водной среде превращается в тетрахлорэтилен.
Получают гексахлорэтан хлорированием полихлорэтанов или тетрахлорэтилена. В парофазном процессе гексахлорэтан выделяют десублимацией, в жидкофазном — перекристаллизацией из спирта или бензола.
ПДК 10 мг/м³, в воде водоёмов санитарно-бытового водопользования 0,01 мг/л.
Физические свойства
Некоторые физические константы гексахлорэтана:
- температура кипения: 185,6 °С;
- температура плавления: 187 °С;
- растворимость в воде (22,3 °С): 0,005 %;
Гексахлорэтан сублимируется в открытых сосудах. Вещество не горит и не взрывается.
Применение
Гексахлорэтан используют в производстве хладона-113, таблеток для дегазации при отливке алюминиевых деталей, как заменитель камфоры в производстве нитроцеллюлозных пластмасс, в смеси с некоторыми металлами как дымообразователь, как интенсификатор свечения пиротехнических составов, а также в медицине как противоглистное средство при лечении гельминтозов печени — описторхоза и фасциолёза.
Категория:- Алканы
Wikimedia Foundation. 2010.
