- ПРОТАКТИНИИ
- ПРОТАКТИНИИ
-
(Protactinium), Pa,- радиоактивный хим. элемент III группы периодич. системы элементов Менделеева, ат. номер 91, относится к актиноидам. Все изотопы П. радиоактивны. В природе существует 231 Ра(
 = 3,28·104 лет) - член естеств. радиоактивного ряда 235U (в лабораториях этот изотоп выделен в кол-ве ок. 150 г). В состав естеств. радиоактивного ряда 238U входят ядерные изомеры 234 Ра (b- -радиоактивные,
= 3,28·104 лет) - член естеств. радиоактивного ряда 235U (в лабораториях этот изотоп выделен в кол-ве ок. 150 г). В состав естеств. радиоактивного ряда 238U входят ядерные изомеры 234 Ра (b- -радиоактивные, = 1,18 мин и
= 1,18 мин и 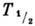 = 6,7 ч). Искусственно получены изотопы 216 Ра - 238 Ра, из них наиб. применение получил b- -радиоактивный 233 Ра (
= 6,7 ч). Искусственно получены изотопы 216 Ра - 238 Ра, из них наиб. применение получил b- -радиоактивный 233 Ра ( = 27 сут), образующийся в реакции 232Th (n, g)333 Th
= 27 сут), образующийся в реакции 232Th (n, g)333 Th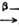 . Электронная конфигурация внеш. электронных оболочек
. Электронная конфигурация внеш. электронных оболочек 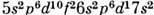 .Энергия ионизации 5,9 эВ. Металлич. радиус атома Ра 0,163 нм, радиус иона Ра 3+ 0,105 нм, Ра 4+0,096 нм, Ра 5+0,090нм. Значение электроотрицательности 1,14.
.Энергия ионизации 5,9 эВ. Металлич. радиус атома Ра 0,163 нм, радиус иона Ра 3+ 0,105 нм, Ра 4+0,096 нм, Ра 5+0,090нм. Значение электроотрицательности 1,14.Металлич. П. существует в виде двух модификаций: ниже 1170
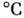 устойчив a-Pa (тетрагональная крис-таллич. структура, постоянные решётки a = 0,3931 нм и с= 0,3236 нм), выше 1170
устойчив a-Pa (тетрагональная крис-таллич. структура, постоянные решётки a = 0,3931 нм и с= 0,3236 нм), выше 1170 - b-Pa (объёмно-центрированная кубич. кристаллич. структура, постоянная решётки a = 0,5019 нм). Плотность a -Ра 15,34 кг/дм 3, b-Pa 12,13 кг/дм 3; t пл ок. 1575
- b-Pa (объёмно-центрированная кубич. кристаллич. структура, постоянная решётки a = 0,5019 нм). Плотность a -Ра 15,34 кг/дм 3, b-Pa 12,13 кг/дм 3; t пл ок. 1575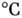 , t кип=4230-4500
, t кип=4230-4500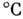 , теплота плавления 12 кДж/моль, теплота испарения 552 кДж/моль, теплоёмкость с р= 27,6 Дж/(моль·К). Уд. электрич. сопротивление 0,19 мкОм*м, термич. коэф. линейного расширения 11,2·10-6 К -1. По твёрдости близок к урану.
, теплота плавления 12 кДж/моль, теплота испарения 552 кДж/моль, теплоёмкость с р= 27,6 Дж/(моль·К). Уд. электрич. сопротивление 0,19 мкОм*м, термич. коэф. линейного расширения 11,2·10-6 К -1. По твёрдости близок к урану.В хим. соединениях проявляет степени окисления +3, +4 и +5 (наиб. устойчива). Хим. свойства Ра во многом отличаются от свойств др. актиноидов. По-тенц. практич. значение Ра связано с предполагаемым использованием 232Th для получения ядерного горючего (при облучении 232Th нейтронами он превращается в 233 Ра, при последующем b- -распаде 233 Ра образуется 233U, к-рый можно использовать как делящийся материал). С. С. Бердоносов,
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.
