- ПРИВЕДЁННОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- ПРИВЕДЁННОЕ УРАВНЕНИЕ СОСТОЯНИЯ
-
- термодинамич. уравнение состояния, записанное относительно безразмерных величин (приведённых переменных), определённых в масштабе критич. значений. П. у. с.
 получается из обычного ур-ния
получается из обычного ур-ния
состояния заменой
заменой 
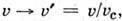
 =
= - критич. значения давления Р, уд. объёма
- критич. значения давления Р, уд. объёма  темп-ры Т, координаты критической точки). Параметры
темп-ры Т, координаты критической точки). Параметры  а следовательно, и
а следовательно, и 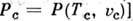 могут быть получены из совместного решения ур-ний
могут быть получены из совместного решения ур-ний 
являющихся необходимым условием термодинамич. устойчивости критич. состояния системы. Использование приведённых переменных
 удобно в случаях, когда феноменологич. ур-ние состояния рассматриваемых систем
удобно в случаях, когда феноменологич. ур-ние состояния рассматриваемых систем  включает только два параметра, конкретизирующих систему данного класса (напр., параметры а и b в Ван-дер-Ваалъса уравнении). В этом случае П. у. с. не содержит указанных параметров и универсально для всех систем, описываемых ур-ниями состояния данного типа ( соответственных состояний закон). Термодинамич. особенности таких систем [уд. теплоёмкости, теплота фазового перехода, уд. объёмы жидкой и газообразной фаз, кривая инверсия (см. Джоуля- Томсона эффект )и др.] также являются универсальными ф-циями
включает только два параметра, конкретизирующих систему данного класса (напр., параметры а и b в Ван-дер-Ваалъса уравнении). В этом случае П. у. с. не содержит указанных параметров и универсально для всех систем, описываемых ур-ниями состояния данного типа ( соответственных состояний закон). Термодинамич. особенности таких систем [уд. теплоёмкости, теплота фазового перехода, уд. объёмы жидкой и газообразной фаз, кривая инверсия (см. Джоуля- Томсона эффект )и др.] также являются универсальными ф-циями  и
и 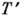 и, будучи определёнными (напр., экспериментально) для одной из таких систем, могут быть пересчитаны на другие.
и, будучи определёнными (напр., экспериментально) для одной из таких систем, могут быть пересчитаны на другие.В микроскопич. теории возможность существования универсальных ур-ний состояния может быть обоснована для систем, статистически невырожденных по отношению к трансляц. движению, когда
 где V- объём системы, содержащей N частиц с массой
где V- объём системы, содержащей N частиц с массой  (см. Статистическая физика), и когда потенциал взаимодействия двух частиц классич. системы
(см. Статистическая физика), и когда потенциал взаимодействия двух частиц классич. системы  где R- расстояние между частицами, d- их эфф. диаметр,
где R- расстояние между частицами, d- их эфф. диаметр,  - параметр интенсивности взаимодействия [ф-ция
- параметр интенсивности взаимодействия [ф-ция 
 для потенциала Ленарда - Джонса n= 12, т =6 (см. Межмолекулярное взаимодействие); для случая твёрдых сфер
для потенциала Ленарда - Джонса n= 12, т =6 (см. Межмолекулярное взаимодействие); для случая твёрдых сфер  ]. Тогда, введя безразмерные величины
]. Тогда, введя безразмерные величины 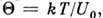
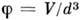 и
и 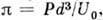 можно показать, что термич. ур-ние состояния
можно показать, что термич. ур-ние состояния  и калорич. ур-ние состояния для теплоёмкости
и калорич. ур-ние состояния для теплоёмкости 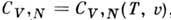 , определяемые производными логарифма статистич. интеграла классич. неидеальной системы, выражаются через
, определяемые производными логарифма статистич. интеграла классич. неидеальной системы, выражаются через 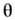 и
и 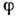 вне зависимости от конкретных значений
вне зависимости от конкретных значений 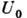 и d:
и d:
Т. о., из подобия потенциалов взаимодействия частиц в разл. физ. системах (т. е. в системах с одинаковой ф-цией
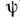 ) следует универсальность П. у. с. Для каждого вида ф-ции
) следует универсальность П. у. с. Для каждого вида ф-ции 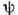 существуют свои П. у. с.
существуют свои П. у. с.Использование приведённых переменных естественно в полуфеменологич. теории критических явлений. В ней предполагается, что существует нек-рый класс физически разл. систем (газ - жидкость, бинарный сплав, магнетики и др.), термодинамич. поведение к-рых в непосредств. близости к критич. точке или к точке фазового перехода является подобным. Поведение разл. термодинамич. величин аппроксимируется степенным законом по параметру
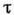 = ( Т-
= ( Т-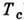 )/Т (степени этого параметра
)/Т (степени этого параметра 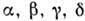 = 1 +
= 1 +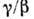 наз. критическими показателями). Ур-ние состояния магнетика М = М (Т, H), где М- намагниченность, H- напряжённость магн. поля, в переменных т =
наз. критическими показателями). Ур-ние состояния магнетика М = М (Т, H), где М- намагниченность, H- напряжённость магн. поля, в переменных т =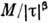 .p
.p 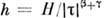 таково, что все изотермы сливаются в одну, имеющую две ветви, т =
таково, что все изотермы сливаются в одну, имеющую две ветви, т =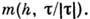 Для ряда магнетиков этот вывод подтверждён экспериментально. Если ур-ние состояния магнетика определяется двумя параметрами А и В, различными для разных систем, напр. зависимостью
Для ряда магнетиков этот вывод подтверждён экспериментально. Если ур-ние состояния магнетика определяется двумя параметрами А и В, различными для разных систем, напр. зависимостью 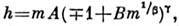
удовлетворяющей заданному с помощью критич. показателей поведению намагниченности
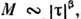 изотермической восприимчивости
изотермической восприимчивости 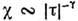 и теплоёмкости
и теплоёмкости 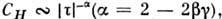 то приведённые значения
то приведённые значения 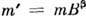 и
и 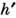 =
=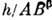 позволяют получить П. у. с.
позволяют получить П. у. с.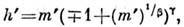
выражающее универсальный закон соответственных состояний магнетика в области критич. точки, к-рый в рамках гипотезы подобия можно перевести на язык систем типа газ - жидкость и т. п.
Лит.: Вукалович М. П., Новиков И. И., Уравнение состояния реальных газов, М.- Л., 1948; Квасников И. А., Термодинамика и статистическая физика. Теория равновесных систем, М., 1991; см., также лит. при ст. Соответственные состояния. И. А. Квасников.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.
