- ГАФНИЙ
- ГАФНИЙ
-
(от позднелат. Hafnia-Копенгаген; лат. Hafnium), Hf,- хим. элемент IV группы периодич. системы элементов, ат. номер 72, ат. масса 178,49. Природный Г. состоит из 6 стаб. изотопов с массовыми числами 174, 176-180, из них 174Hf обладает слабой
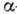 -радиоактивностью (
-радиоактивностью (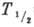 =2*1015 лет), остальные стабильны. В качестве радиоактивного индикатора обычно используют
=2*1015 лет), остальные стабильны. В качестве радиоактивного индикатора обычно используют 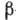 -радиоактивный 181Hf (
-радиоактивный 181Hf (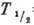 =42,4 сут). Конфигурация внеш. электронных оболочек 5s2p6d26s2. Энергии последовательных ионизации соответственно равны 7,5, 15,0, 23,3 и 33,3 эВ. Металлич. радиус 0,159 нм, радиус иона Hf4+ 0,082 нм. Значение электроотрицательности 1,23.
=42,4 сут). Конфигурация внеш. электронных оболочек 5s2p6d26s2. Энергии последовательных ионизации соответственно равны 7,5, 15,0, 23,3 и 33,3 эВ. Металлич. радиус 0,159 нм, радиус иона Hf4+ 0,082 нм. Значение электроотрицательности 1,23.
В свободном виде - серебристо-серый металл, существует в двух модификациях. Параметры решётки гексагональной
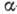 -модификации а=0,31946 нм, с=0,50511 нм, при 1740 0C Г. переходит в кубич.
-модификации а=0,31946 нм, с=0,50511 нм, при 1740 0C Г. переходит в кубич.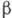 модификацию. Плотность 13,331 кг/дм 3, t пл=2230 0C, t кип=5225 0C. Уд. теплоёмкость 143Дж/(кг*К) (при 298 К), уд. сопротивление 32,4*10-2 мкОм*м (0 0C). Г. обладает высокой эмиссионной способностью, работа выхода электрона для a-модификации 3,20 эВ. Чистый Г. пластичен, поддаётся прокатке, ковке, штамповке.
модификацию. Плотность 13,331 кг/дм 3, t пл=2230 0C, t кип=5225 0C. Уд. теплоёмкость 143Дж/(кг*К) (при 298 К), уд. сопротивление 32,4*10-2 мкОм*м (0 0C). Г. обладает высокой эмиссионной способностью, работа выхода электрона для a-модификации 3,20 эВ. Чистый Г. пластичен, поддаётся прокатке, ковке, штамповке.
По хим. свойствам - полный аналог циркония. В соединениях проявляет степени окисления +4 (наиб. характерна), +3, +2 и +1. Находит применение в ядерной энергетике (регулирующие стержни ядерных реакторов), т. к. имеет высокое сечение захвата тепловых нейтронов (1,15*10-26 м 2). Металлоподобные очень твёрдые соединения Г. с бором, углеродом, азотом, кремнием и т. п. обладают высокими t пл (св. 3000 0C; для твёрдого раствора карбида Г. и тантала t пл>4000°С). С. С. Бердоносов.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.
