- ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ НЕОРГАНИЧЕСКИЕ
содержат группировку из связанных между собой двух атомов О. Употребляют также назв. дикислородные соединения. Общее св-во большинства пероксидных соед. (П. с.)-способность сравнительно легко выделять кислород (при нагр., при действии воды или др. в-в), поэтому иногда говорят, что кислород в них присутствует в активной форме и наз. его активным кислородом.
Различают ионные и ковалентныеП. с. Дикислород-ная группировка может существовать в трех ионных формах, поэтому ионные П. с. подразделяют на три осн. группы: пероксиды с ионом
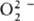 ; супероксиды (гипероксиды) с ионом
; супероксиды (гипероксиды) с ионом 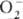 ; диоксигенильные соединения с ионом
; диоксигенильные соединения с ионом 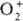 . К ионным П. с. относят также озониды неорганические, гидропе-роксиды и соли пероксония, содержащие соотв. ионы
. К ионным П. с. относят также озониды неорганические, гидропе-роксиды и соли пероксония, содержащие соотв. ионы 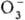 ,
, 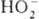 ,
, 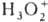 . Среди ионных П. с. только пероксиды диамагнитны и не окрашены (или их окраска не связана с пероксид-ной группой), остальные парамагнитны и, как правило, ярко окрашены.
. Среди ионных П. с. только пероксиды диамагнитны и не окрашены (или их окраска не связана с пероксид-ной группой), остальные парамагнитны и, как правило, ярко окрашены.
Ковалентные П. с. имеют общую ф-лу RЧОЧОЧR', где R и R' - неорг. радикалы или атомы. К этой группе относят водорода пероксид, пероксокислоты, пероксосольваты, хлор-перокситрифторметан CF3OOCl, соед. с цепочкой из трех атомов О, напр. CF3OOOCF3, и др. Ионы
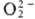 и
и 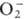 могут образовывать координац. связи с ионами переходных и непереходных элементов, соответствующие соед. входят в группу комплексных П. с., близких по св-вам к ковалентным П. с. Диоксидифторид О 2F2, соед. с цепочкой из трех атомов О (напр., CF3OOOCF3) и нек-рые другие также можно отнести к П. с. К комплексным П. с. следует отнести соед., обратимо отдающие кислород,-комплексы с мол. кислородом, важнейший из к-рых-оксигемоглобин. Энергия, длина и порядок связи ОЧО в молекуде П. с, зависят от заряда на группе O2 (табл. 1).
могут образовывать координац. связи с ионами переходных и непереходных элементов, соответствующие соед. входят в группу комплексных П. с., близких по св-вам к ковалентным П. с. Диоксидифторид О 2F2, соед. с цепочкой из трех атомов О (напр., CF3OOOCF3) и нек-рые другие также можно отнести к П. с. К комплексным П. с. следует отнести соед., обратимо отдающие кислород,-комплексы с мол. кислородом, важнейший из к-рых-оксигемоглобин. Энергия, длина и порядок связи ОЧО в молекуде П. с, зависят от заряда на группе O2 (табл. 1).
Табл. 1. ХАРАКТЕРИСТИКА СВЯЗИ ОЧО
Показатель
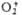
O2
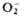
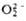
Энергия связи, кДж/моль
642
494
~390
~200
Длина связи. нм
0.112
0,121
0,128
-0,15
Порядок связи
2,5
2
1,5
I
Примеры П. с.-ионные пероксиды и гидропероксиды Na2O2, BaO2, NH4OOH; координац. пероксиды и гидропероксиды [Nb(O2)] 3Ч, [Ti(O2)F5] 3Ч, [BF3OOH] Ч; пероксокислоты и их соли H2CO4, KHSO5; пероксосольваты Na2CO3
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
