- ОКСОНИЕВЫЕ СОЕДИНЕНИЯ
-
(оксониевые соли, соли оксония), содержат положительно заряженный атом кислорода, связанный ковалентно с орг. остатками и(или) водородом и ионной связью с анионом.
Простейшие неорганические О. с.-соли гидроксония [Н 3 О] + Х -, существующие обычно только в р-рах к-т; в кристаллич. состоянии получены лишь соед. с анионами ,
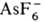 (т. разл. 193°С) и
(т. разл. 193°С) и 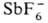 (т. разл. 357 °С).
(т. разл. 357 °С).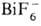
Органические О. с. в зависимости от числа орг. остатков у атома О подразделяют на первичные, вторичные и третичные. Наиб. устойчивы и больше всего изучены третичные О. с. Известны след, типы третичных О. с.: [R3O]+X-, где R-алкил или арил; карбоксониевые (алкоксикарбониевые) соли - производные карбонильных соед. (напр., соед. ф-л I или II) и диалкилацилоксониевые соли (напр., III):
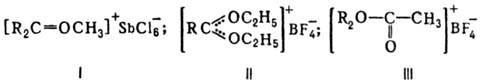
Карбоксониевые соед. м. б. представлены резонансом структур, напр.:
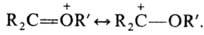 К О. с. относят также пирилия соли с оксониевым атомом кислорода в 6-членном ароматич. цикле и "оксановые" соед., в к-рых оксониевый атом кислорода соединен ковалентно с тремя атомами металла и ионной связью с анионом, напр. [(ClHg)3O]+Cl- или [(Ph3PAu)3O] + BF-4 .
К О. с. относят также пирилия соли с оксониевым атомом кислорода в 6-членном ароматич. цикле и "оксановые" соед., в к-рых оксониевый атом кислорода соединен ковалентно с тремя атомами металла и ионной связью с анионом, напр. [(ClHg)3O]+Cl- или [(Ph3PAu)3O] + BF-4 .
ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ ОКСОНИЕВЫХ СОЕДИНЕНИЙ, °С
Катион
Анион
SbCl-6
BF-4
FeCl-4
(СН 3)3 О +
156-158
141
81
(С 2 Н 5)3O+
131
92
74
(С 6 Н 5)3O+*
-
226
-
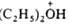
149
-
53
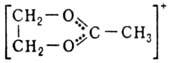
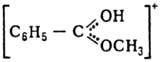
[С 6 Н 5 СН= OCH3]+
166
-
(с разл.)
121-123
164-166
-
[(СН 3O)2 С = ОСН 3]+
130-131
138
-
[С 2 Н 5 СН=ОН]+
181
-
-
112-114
-
-
* Т. пл. [(С 6 Н 5)3O]+ Вг - 182°С, [(С 6 Н 5)3 О]+I- 177-178°C.
Свойства. О. с. -кристаллич. солеобразные в-ва (см. табл.), раств. в полярных р-рителях (ацетон, CH3CN, CH3NO2, C6H5NO2, жидкий SO2), не раств. в диэтиловом эфире и углеводородах. Р-ры О. с. в воде электропроводны, по элект-рич. проводимости [(CH3)3O] + BF-4 близок к KI.
Алифатические и ароматические О. с. различаются геометрией молекул. Катион [(С 2 Н 5)3 О]+ имеет строение тригон. пирамиды с атомом О в вершине, расстояние между к-рым и плоскостью связанных с ним атомов углерода 0,0413 нм. В спектрах ПМР алифатических и ароматических О. с. наблюдается сдвиг сигналов соотв.
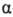 -Н-атома и орто -Н-атома в слабое поле примерно на 1 м. д. по сравнению с соответствующими простыми эфирами.
-Н-атома и орто -Н-атома в слабое поле примерно на 1 м. д. по сравнению с соответствующими простыми эфирами.
Алифатические О. с. устойчивы только при наличии комплексных анионов, обладающих слабыми нуклеоф. св-вами (ВF-4, РF-6 ,
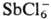 и т. п.), и легко разрушаются водой и спиртами. Особенно лабильны первичные и вторичные О. с., быстро гидролизующиеся уже влагой воздуха; для третичных О. с. устойчивость в сильной степени зависит от природы аниона и уменьшается в ряду:
и т. п.), и легко разрушаются водой и спиртами. Особенно лабильны первичные и вторичные О. с., быстро гидролизующиеся уже влагой воздуха; для третичных О. с. устойчивость в сильной степени зависит от природы аниона и уменьшается в ряду: 
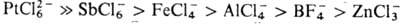 . Ароматич. третичные О. с. очень устойчивы и химически довольно инертны, они не реагируют с водой и разлагаются лишь при сильном нагревании:
. Ароматич. третичные О. с. очень устойчивы и химически довольно инертны, они не реагируют с водой и разлагаются лишь при сильном нагревании:
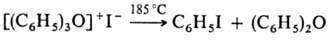
Третичные алифатические О. с.-одни из самых сильных алкилирующих агентов, в очень мягких условиях легко алкилируют не только спирты, фенолы, орг. к-ты, амины, сульфиды, но и соед., не алкилирующиеся обычными реагентами (AlkHal, Alk2SO4), напр, амиды к-т, сложные эфиры, кетоны, сульфоксиды, тиофен (по атому серы):
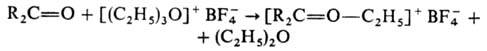
С помощью третичных алифатических О. с. синтезированы чрезвычайно реакционноспособные ацетали амидов к-т и лактамов, нитрилиевые соли (последние м. б. восстановлены до вторичных аминов) и эфиры нитроновых к-т, напр.:
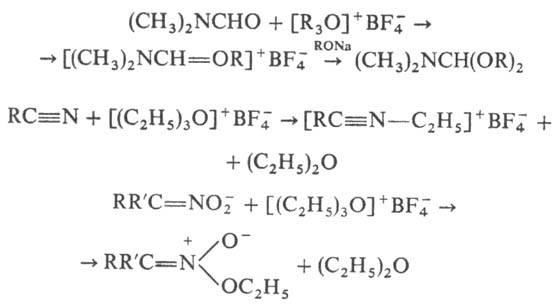
Карбоксониевые соед. могут реагировать с нуклеофилами по атому О или по атому С, напр.:
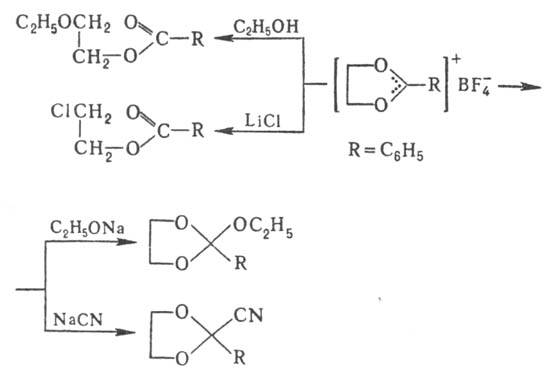
О. с. могут использоваться для замены анионов в ониевых солях, напр.:

Соли трифенилоксония в отличие от своих алифатич. аналогов плохо реагируют с нуклеофилами:
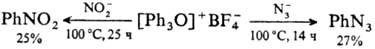
Они также трудно вступают в р-ции электроф. замещения; при этом в отличие от др. ароматич. ониевых соед. (см., напр., Галогенониевые соединения )замещение протекает в пара-положение, напр.:
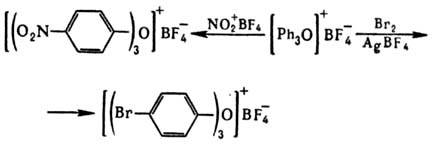
Получение и применение. Общие способы получения третичных О. с. 1) Действием алкилгалогенидов на эфираты BF3 или SbCl5:
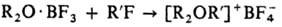
2) Взаимод. простых эфиров с алкилгалогенидами в присут, безводного AgBF4:

3) Алкилированием гидроксониевых солей или первичных и вторичных О. с. диазометаном, напр.:
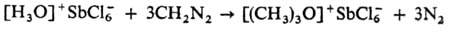
Борофторид триэтилоксония получают след, образом:
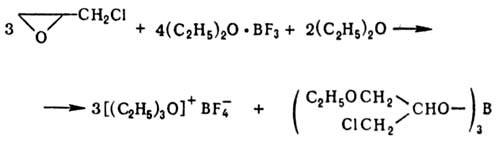
Третичные карбоксониевые соли получают: алкилирова-нием карбонильных соед. третичными О. с. или алкилгалогенидами в присут. безводного AgBF4, а также действием BF3 или SbCl5 на ортоэфиры:
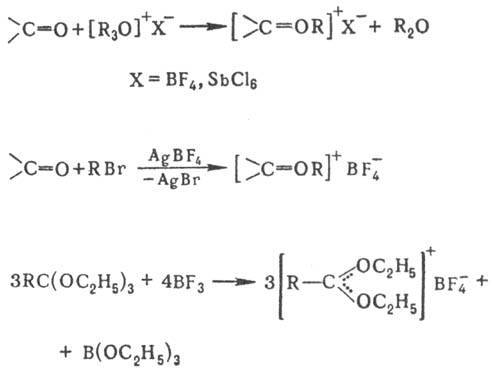
Первичные и вторичные О. с. получают взаимод. спиртов, простых эфиров или кетонов с комплексными к-тами [H4Fe(CN)6 , H3Fe(CN)6, H3Co(CN)6 , H2PtCl6] или с гало-генидами металлов (SbCl5 , FeCl3 , AlCl3 , SnCl4, ZnCl2) и безводным НСl. Р-цию проводят при т-ре от -70 до - 80 °С при полном отсутствии влаги, напр.:
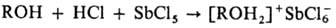
Ароматические О. с. получают термолизом борофторидов арилдиазония в дифениловом эфире или внутримол. циклизацией нек-рых диазосоед., напр.:
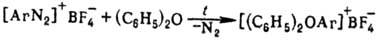
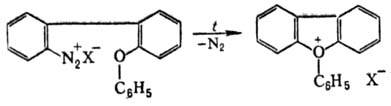
О. с. применяют гл. обр. в качестве катализаторов катион-ной полимеризации и как алкилирующие агенты. Иногда их используют для активации инертных карбонильных групп и в качестве акцептора гидрид-иона.
Лит.: Несмеянов А. Н., Избр. труды, т. 2, М., 1959, с. 458-60, 467-72; т. 3, М., 1959, с. 325-65; Houben-Weyl, Methoden der organischen Chemie, 4 Aufl., Bd 6, Tl 3, Stuttg., 1965, S. 325-65; Perst H., Oxonium ions in organic chemistry, RY., 1971. Т. П. Толстая.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
