- МЕТАЛЛЫ ОРГАНИЧЕСКИЕ
- ,
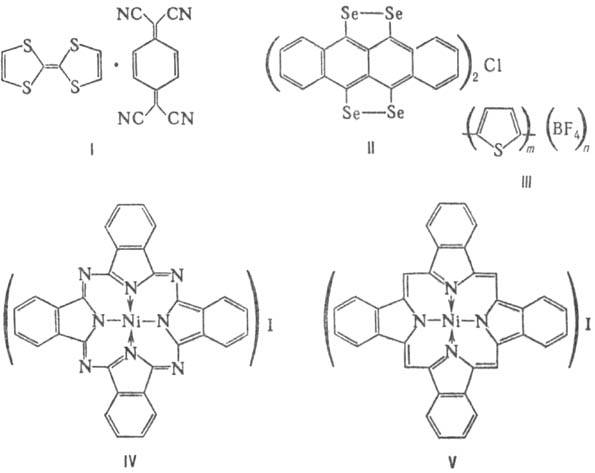
орг. соед., обладающие металлич. проводимостью. В М. о. перенос электрона в твердой фазе осуществляется по орг. компоненте молекулы. М. о. наз. также "с и н т е т и ч. м е т а л л а м и". К М. о. относятся мономерные и высокомол. ион-радикальные соли и комплексы с переносом заряда (см. Молекулярные комплексы), напр. комплекс тетратиофульвалена с 7,7,8,8-тетрациа-нохинодиметаном (ф-ла I) и бис -(тетраселенотетрацен)хло-рид (II), иодированный полиацетилен и политиофентетра-фтороборат (III, m > n), в-ва на основе металлофтало-цианинов и металлобензопорфиринов-соед. соотв. ф-л IV и V и др.
Уд. электрич. проводимость (s) М. о. при обычной т-ре 10-105 Ом -1. см -1 При понижении т-ры величина s может достигать 105 Ом -1. см -1, однако при низких т-рах М. о. претерпевают переход металл-диэлектрик. Существуют М. о., у к-рых металлич. состояние сохраняется при низких т-рах (ниже 40 К), и М. о., способные к переходу в сверх-проводящее состояние. На стабильность металлического состояния существенное влияние оказывают природа ге-тероатома в циклах, давление, ионизирующее излучение и другие факторы.
Характерная особенность кристаллич. структуры М. о.-наличие регулярных "стопок", слоев, цепочек, состоящих из доноров и акцепторов электронов. В мономерных М. о. расстояния между молекулами в стопках существенно меньше ван-дер-ваальсовых и значительно меньше расстояний между самими стопками. Благодаря особенностям кристаллич. структуры М. о.-квазиодномерные проводники, т. е. для них характерна анизотропия электрич. проводимости, к-рая максимальна вдоль длинной оси кристалла и минимальна в перпендикулярном направлении (s||/s| достигает 103).
Методы синтеза М. о. основаны на частичном восстановлении или окислении акцептора или донора электронов с помощью, напр., Na, I2, Br2, AsF5; используют также электрохим., фотохим., электрофотохим. окисление. М. о. получают в виде монокристаллов, порошков, пленок и др. Возможно использование металлов органических в качестве неметаллических проводников, сверхпроводников, электродов в химических источниках тока, для записи и преобразования информации и др.
Лит.: Жуховицкий В. Б., Хидекель М. Л., ДюмаевК. М., "Успехи химии", 1985, т. 54, в. 2, с. 239-52. М. Л. Хидекель.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
