- АЛЛИЛЬНЫЕ СОЕДИНЕНИЯ
содержат группировку R2C=CRCR2, где R-H или орг. остаток. К А. с. относятся аллильные СН 2=СНСН 2 Х, металлильные СН 2=С(СН 3 )СН 2 Х, кротильные СН 3 СН=СНСН 2 Х, пренильные (СН 3)2 С=СНСН 2 Х и др. соед., в к-рых X связан с атомом С соседним с двойной связью. Название "А. с." происходит от лат. allium- чеснок, из к-рого в 1844 был выделен диаллилсульфид.
Аллильная, металлильная, пренильная группы-фрагменты мн. природных соед.: витаминов, терпенов, терпе-ноидов (напр., гераниола, нерола, линалоола), антибиотиков. Во мн. эфирных маслах содержатся аллильные производные бензола, напр. эвгенол, сафрол.
В А. с. Н 2 С=СНСН 2 Х, где Х-функц. группа, энергия связи СЧX на 50-105 кДж/моль меньше, чем в насыщ. аналогах, и это - одна из причин их повышенной хим. активности; вторая связана с тем, что отрыв X в виде иона или своб. радикала приводит к образованию структур, в к-рых предполагается равномерное распределение заряда или неспаренного электрона по обоим концам цепи, напр.:
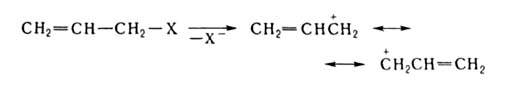
Специфич. св-во А. с.-способность к аллилъной перегруппировке. Для А. с. нек-рых непереходных металлов СН 2=СНСН 2 М (М = 1/2Zn, BR2, V2Cd и др.) характерна перманентная аллильная перегруппировка (см. Аллшбораны).
Аллилвиниловые или аллилариловые эфиры, сульфиды, амины и их гомологи (напр., типа CH2=CHCH2XCH=CHR и СН 2=СНСН 2 ХАг, где X = О, NH, S) при нагр. претерпевают Коупа перегруппировку и Клайзена перегруппировку.
Замещение в А. с. происходит с сохранением двойной связи в ее первоначальном положении или сопровождается аллильной перегруппировкой. См. Аллилъное замещение.
Аллильные производные Mg, Li, В и др. присоединяются к карбонильным соед. количественно с перегруппировкой (часто энантиоселективно), напр.:
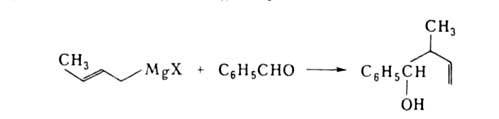
Аллилсиланы и аллилстаннаны (в отличие от алкильных производных) присоединяются к карбонильным соед. в присут. к-т Льюиса.
Для А. с. характерны р-ции непредельных соед.-присоединение, напр.:
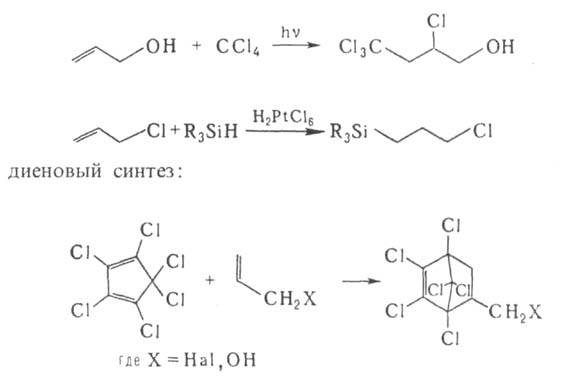
замещение активированного атома Н, находящегося в
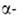 положении к двойной связи:
положении к двойной связи: 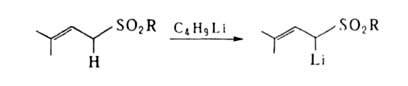
а также восстановление, окисление, полимеризация и др. Аллилгалогениды реагируют с карбонилами Mo, W, Мп, Fe,-Co и др. переходных металлов с образованием
 комплексов (см. Аллильные комплексы переходных металлов).
комплексов (см. Аллильные комплексы переходных металлов). Практически важные способы синтеза А. с. основаны на р-циях замещения и перегруппировках, напр.:
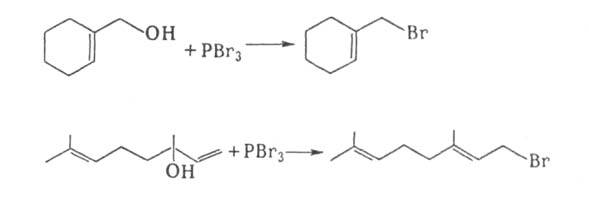
Аллилгалогениды м. б. использованы как алкилирующие агенты для получения
 аллильных производных Mg, A1, В, Sn, Si и др., напр. триметаллилборана или металлилалюминийсесквибромида:
аллильных производных Mg, A1, В, Sn, Si и др., напр. триметаллилборана или металлилалюминийсесквибромида: 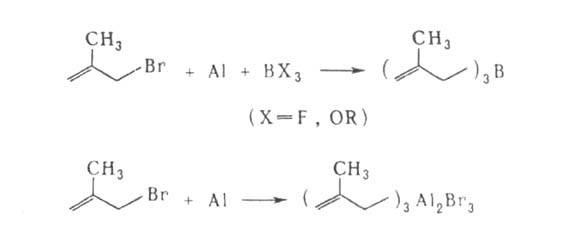
Аллиллитий образуется при взаимод. фениллития и аллилтрифенилолова:
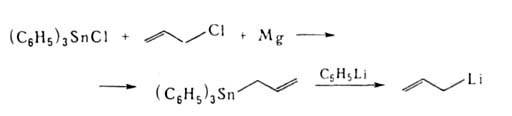
Восстановление, окисление, дегидрирование, расщепление по Гофману и др. р-ции также часто используются для введения двойной связи или функц. группы с образованием А. с., напр.:
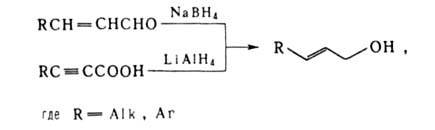
Аллилгалогениды синтезируют радикальным
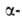 галогенированием алкенов и циклоалкенов бромом, N-хлор- или N-бромсукцинимидом (см. Воля-Циглера реакция). Аллил- и металлилхлориды получают хлорированием соотв. пропилена и изобутилена; аллилиодид - действием 12 и Р на глицерин; кротил- и пренилгалогениды - присоединением НХ (Х = С1, Вr) к 1,3-бутадиену и изопрену, напр.:
галогенированием алкенов и циклоалкенов бромом, N-хлор- или N-бромсукцинимидом (см. Воля-Циглера реакция). Аллил- и металлилхлориды получают хлорированием соотв. пропилена и изобутилена; аллилиодид - действием 12 и Р на глицерин; кротил- и пренилгалогениды - присоединением НХ (Х = С1, Вr) к 1,3-бутадиену и изопрену, напр.: 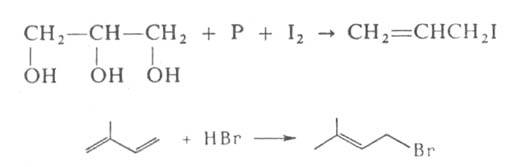
Аллильные спирты можно получать гидролизом аллилгалогенидов или окислением олефинов О 2 воздуха; образующиеся вначале пероксидные соед. превращаются в спирты под действием Na2SO3, NaOH или LiAlH4:
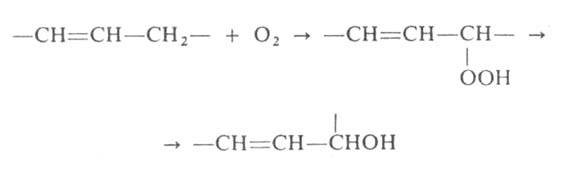
Ацетат 2-циклогексенола синтезируют нагреванием циклогексена с уксусным ангидридом и селенистой к-той при 70
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
