- Е620
-
Глутаминовая кислота 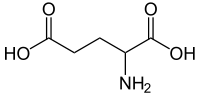
Общие Сокращения Glu,E
GAA,GAGХимическая формула C5H9N1O4 Молярная масса 147.13 г/моль Классификация номер CAS 56-86-0 — алифатическая аминокислота. В живых организмах глутаминовая кислота и её анион глутамат присутствуют в составе белков, ряда низкомолекулярных веществ и в свободном виде. Глутаминовая кислота играет важную роль в азотистом обмене. Глутаминовая кислота также является нейромедиаторной аминокислотой, одним из важных представителей класса «возбуждающих аминокислот». Связывание аниона глутамата со специфическими рецепторами нейронов приводит к возбуждению нейронов.
Содержание
Глутамат как нейромедиатор
Глутаматные рецепторы
Существуют ионотропные и метаботропные (mGLuR 1-8) глутаматные рецепторы.
Ионотропными рецепторами являются NMDA-рецепторы, AMPA-рецепторы и каинатные рецепторы. В нейронах представлены NMDA-рецепторы, в астроцитах — AMPA-рецепторы. Известно перекрестное взаимодействие NMDA-рецепторов и метаботропных mGLu-рецепторов.
Эндогенные лиганды глутаматных рецепторов — глутаминовая кислота, аспарагиновая кислота и N-метил-D-аспартат (NMDA). Блокаторами NMDA-рецепторов являются PCP, кетамин, барбитураты и другие вещества. AMPA-рецепторы также блокируются барбитуратами, в том числе тиопенталом. Каинова кислота является блокиратором каинатных рецепторов.
«Круговорот» глутамата
При наличии глюкозы в митохондриях нервных окончаний происходит дезаминирование глутамина до глутамата при помощи фермента глутаминазы. Также, при аэробном окислении глюкозы глутамат обратимо синтезируется из альфа-кетоглутарата (входит в цикл Кребса) при помощи аминотрансферазы.
Синтезированный нейроном глутамат закачивается в везикулы. Этот процесс является протон-сопряженным транспортом. В везикулу с помощью протон-зависимой АТФазы закачиваются ионы H+. При выходе протонов по градиенту в везикулу поступают молекулы глутамата при помощи везикулярного транспортера глутамата (VGLUTs).
Глутамат выводится в синаптическую щель, откуда поступает в астроциты, там трансаминируется до глутамина. Глутамин выводится снова в синаптическую щель и только тогда захватывается нейроном. По некоторым данным, глутамат напрямую путем обратного захвата не возвращается.[1]
Роль глутамата в кислотно-щелочном балансе
Дезаминирование глутамина до глутамата при помощи фермента глутаминазы, приводит к образованию аммиака, который в свою очередь связывается со свободным протоном и экскретируется в просвет почечного канальца, приводя к снижению ацидоза, превращение глутамата в кетоглутарат, также происходит с образованием аммиака, далее кетоглутарат распадается на воду и углекислый газ, последние при помощи карбоангидразы через угольную кислоту, превращаются в свободный протон и гиброкарбонат, протон экскретируется в просвет почечного канальца, за счет котранспорта с ионом натрия, а бикарбонат попадает в плазму.
Глутаматергическая система
В ЦНС находится порядка 106 глутаматергических нейронов. Тела нейронов лежат в коре головного мозга, обонятельной луковице, гиппокампе, черной субстанции, мозжечке. В спинном мозге — в первичных афферентах дорзальных корешков.
Патологии, связанные с глутаматом
Повышенное содержание глутамата в синапсах между нейронами может перевозбудить и даже убить эти клетки, что приводит к таким заболеваниям, как АЛС. Для избежания таких последствий глиальные клетки астроциты поглощают избыток глутамата. Он транспортируется в эти клетки с помощью транспортного белка GLT1, который присутствует в клеточной мембране астроцитов. Будучи поглощенным клетками астроглии, глутамат больше не приводит к повреждению нейронов.
Применение
Фармакологический препарат глутаминовой кислоты оказывает умеренное психостимулирующее, энергизирующее, возбуждающее и отчасти ноотропное действие.
Глутаминовая кислота (пищевая добавка E620) и её соли (глутамат натрия Е621, глутамат калия Е622, диглутамат кальция Е623, глутамат аммония Е624, глутамат магния Е625) используются как усилитель вкуса во многих пищевых концентратах и консервах.
Примечания
- ↑ Ашмарин И. П., Ещенко Н. Д., Каразеева Е. П. Нейрохимия в таблицах и схемах. М.: «Экзамен», 2007
См. также
Ссылки
Аминокислоты Стандартные аминокислоты Аланин · Аргинин · Аспарагин · Аспарагиновая кислота · Валин · Гистидин · Глицин · Глутамин · Глутаминовая кислота · Изолейцин · Лейцин · Лизин · Метионин · Пролин · Серин · Тирозин · Треонин · Триптофан · Фенилаланин · Цистеин Нестандартные аминокислоты Пирролизин · Селеноцистеин · Цитруллин · 4-гидроксипролин · 5-гидроксилизин · Десмозин · N-метиллизин Близкие по структуре соединения Таурин Незаменимые аминокислоты · Генетический код
Wikimedia Foundation. 2010.
Полезное
