- Трис
-
Трис 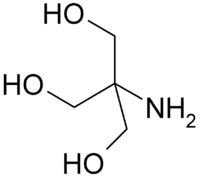
Общие Систематическое наименование 2-амино-2-гидроксиметил-пропан-1,3-диол Сокращения THAM Традиционные названия ТРИС, трис, Trizma™ Химическая формула C4H11NO3 Физические свойства Молярная масса 121,14 г/моль Термические свойства Температура плавления 175—176 °C Температура кипения 219 °C Химические свойства Растворимость в воде ~50 г/100 мл Классификация Рег. номер CAS 77-86-1 Рег. номер PubChem 6503 SMILES OCC(N)(CO)CO Трис (англ. Tris, THAM) — сокращённое название химического соединения трис(гидроксиметил)аминометана (HOCH2)3CNH2. Трис широко используется в биохимии и молекулярной биологии в качестве буферного раствора,[1] например, в буферных системах TAE и TBE, для растворения нуклеиновых кислот. По химической структуре трис является первичным амином и имеет характерные для аминов свойства, например, конденсируется с альдегидами.
Содержание
Буферные свойства
Трис имеет pKa 8,06, и эффективен в качестве буфера при pH от 7,0 до 9,2.
Значение pKa снижается приблизительно на 0,03 при снижении температуры на один градус Цельсия.[2][3]
Широко распространённый вариант буферного раствора, Трис-HCl, является кислой солью. Когда pH раствора соответствует pKa, концентрации противоионов равны (OH- для трис-HCl и H+ для трис-основания).
Показано, что трис ингибирует некоторые ферменты,[4][5] и поэтому должен использоваться с осторожностью при изучении белков.
Синтез
Трис синтезируют в две стадии из нитрометана через интермедиат (HOCH2)3CNO2. Восстановление последнего дает трис(гидроксиметил)аминометан.[6]
Применение
Буферные свойства при рН 7—9 соответствуют физиологическим значениям рН для большинства организмов. Эти свойства и низкая стоимость делают трис одним из лучших буферов для биохимии и молекулярной биологии. Трис используют в качестве первичного стандарта для растворов кислот при химическом анализе.
Трис используют в качестве альтернативы гидрокарбонату натрия при лечении метаболического ацидоза.[7]
См. также
- MOPS
- HEPES
- MES
Примечания
- ↑ Gomori, G., Preparation of Buffers for Use in Enzyme Studies. Methods Enzymology., 1, 138—146 (1955).
- ↑ El-Harakany, A.A.; Abdel Halima, F.M. and Barakat, A.O. (1984). «Dissociation constants and related thermodynamic quantities of the protonated acid form of tris-(hydroxymethyl)-aminomethane in mixtures of 2-methoxyethanol and water at different temperatures». J. Electroanal. Chem. 162 (1-2): 285–305. DOI:10.1016/S0022-0728(84)80171-0.
- ↑ Vega, C.A.; Butler, R.A. et al. (1985). «Thermodynamics of the Dissociation of Protonated Tris(hydroxymethy1)aminomethane in 25 and 50 wt % 2-Propanol from 5 to 45 °C». J. Chem. Eng. Data 30: 376–379. DOI:10.1021/je00042a003.
- ↑ Desmarais, WT; et al. (2002). «The 1.20 Å resolution crystal structure of the aminopeptidase from Aeromonas proteolytica complexed with Tris: A tale of buffer inhibition». Structure 10 (8): 1063–1072. DOI:10.1016/S0969-2126(02)00810-9. PMID 12176384.
- ↑ Ghalanbor, Z; et al. (2008). «Binding of Tris to Bacillus licheniformis alpha-amylase can affect its starch hydrolysis activity.». Protein Peptide Lett. 15 (2): 212–214. DOI:10.2174/092986608783489616. PMID 18289113.
- ↑ (2000) «Nitro Compounds, Aliphatic». DOI:10.1002/14356007.a17_401.
- ↑ Kallet, RH; Jasmer RM, Luce JM et al. (2000). «The treatment of acidosis in acute lung injury with tris-hydroxymethyl aminomethane (THAM)». American Journal of Respiratory and Critical Care Medicine 161 (4): 1149–1153. PMID 10764304.
 Категории:
Категории:- Амины
- Буферные растворы
- Полиолы
Wikimedia Foundation. 2010.
