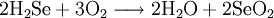- Селенистый водород
-
Селеноводород 

Общие сведения Систематическое наименование Селеноводород Прочие наименования Селенистоводородная кислота
Селеноводородная кислота
Селенистый водород
Гидрид селена
Селенид водорода
Дигидрид селенаМолекулярная формула H2Se Молярная масса 80,9758 г/моль Внешние признаки Бесцветный газ. Номер CAS [7783-07-5] [1] Свойства Плотность и Агрегатное состояние 3,310 г/л, газ. Растворимость в воде 0,70 г/100 мл Температура плавления −65,73 °C (207,42 K) Температура кипения −41,25 °C (231,9 K) Кислотность (pKa) 3,89 (11,0 при 25 °C) Структура Молекулярная форма Планарная. Дипольный момент ? D Факторы риска MSDS Основные факторы риска Крайне токсично, крайне
огнеопасен, едкийNFPA 704  443
443Температура воспламенения ?°C Указания по безопасности R/S RTECS number X1050000 Supplementary data page Structure and
propertiesn, εr, etc. Thermodynamic
dataPhase behaviour
Solid, liquid, gasSpectral data UV, IR, NMR, MS Related compounds Other group 16
hydrogen compoundsH2O
H2S
H2Te
H2PoOther selenides Ag2Se Related compounds OSeCl2 Except where noted otherwise, data are given for
materials in their standard state (at 25 °C, 100 kPa)
Infobox disclaimer and referencesСеленоводоро́д (хим. формула H2Se) — соединение водорода и селена. Представляет собой бесцветный горючий газ с отвратительным запахом при нормальных условиях. Селеноводород — самое токсичное соединение селена с опасным периодом воздействия: 0,3 ppm на 8 часов.
Содержание
Структура
Молекула селеноводорода имеет «изогнутую» структуру H-Se-H с валентным углом 91°. Наблюдается три колебательные полосы в инфракрасном спектре: 2358, 2345, и 1034 см−1.
Свойства
Химические свойства селеноводорода схожи со свойствами сероводорода, хотя H2Se обладает большей кислотностью (pKa = 3,89 при 25 °C), чем H2S (pKa = 11,0 при 25 °C). Учитывая высокую кислотность, селеноводород растворим в воде.
При горении селеноводорода в воздухе или кислороде образуется оксид селена и вода.
Получение
Для получения селеноводорода используется несколько реакций, в том числе:
- H2Se получают из реакции воды и селенида алюминия Al2Se3, сопровождающейся выделением гидроксида алюминия.
- Аналогичный результат получается при кислотном гидролизе селенида железа(II) FeSe:
-
- Al2Se3 + 6 H2O ⇌ 2 Al(OH)3 + 3 H2Se
См. также
Аналоги соединения по VI группе:
- Вода
- Сероводород
- Теллуроводород
- Полоноводород
Wikimedia Foundation. 2010.