- Замещения реакции
-
химические превращения, характеризующиеся тем, что «атакующая», частица вытесняет какой-либо атом или группу атомов из др. реагента:Х + Y - S → X - S + Y.В зависимости от характера Х З. р. подразделяют на нуклеофильные (sn реакции; Х — анион или молекула, несущая неподелённую электронную пару), электрофильные (se реакции; Х — катион или иная частица, обладающая сродством к электронной паре) и радикальные (sr реакции; Х — частица с неспаренным электроном). Различают мономолекулярные и бимолекулярные З. р. По механизму нуклеофильного мономолекулярного замещения (SN1) протекает, например, гидролиз трет-бутилхлорида, при этом на первой стадии происходит медленная диссоциация на ион карбония и хлорид-ион, на второй — быстрая реакция карбониевого иона с водой с образованием трет-бутилового спирта:(CH3)3C—Cl → (CH3)3C+ + Cl-,(CH3)3C+ + H2O → (CH3)3C—OH + H+.Для первичных и вторичных алкилгалогенидов более характерен одностадийный гидролиз, при котором разрыв связи С — галоген и образование связи С—ОН происходит синхронно (нуклеофильное бимолекулярное замещение, SN2):
 Кинетика процесса в первом случае отвечает первому, во втором — второму порядку (см. Кинетика химическая). Электрофильное замещение наиболее характерно для ароматических соединений, например:
Кинетика процесса в первом случае отвечает первому, во втором — второму порядку (см. Кинетика химическая). Электрофильное замещение наиболее характерно для ароматических соединений, например: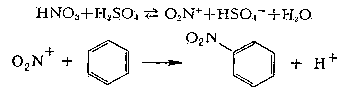 Пример радикального замещения — металепсия (радикально-цепное хлорирование парафинов):Cl2 → Cl∙ + Cl∙; Cl∙ + CH4 → CH3∙ + HCl;CH3∙ + Cl2 → CH3Cl и т.д.Частным видом З. р. являются реакции двойного обмена:X—Y + Z—W → X—W + Y—Zи вытеснения:Zn + CuSO4 → ZnSO4 + Cu.Б. Л. Дяткин.
Пример радикального замещения — металепсия (радикально-цепное хлорирование парафинов):Cl2 → Cl∙ + Cl∙; Cl∙ + CH4 → CH3∙ + HCl;CH3∙ + Cl2 → CH3Cl и т.д.Частным видом З. р. являются реакции двойного обмена:X—Y + Z—W → X—W + Y—Zи вытеснения:Zn + CuSO4 → ZnSO4 + Cu.Б. Л. Дяткин.
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
