- Боран
-
Бороводороды (также Бораны) — химические соединения бора с водородом. Отличаются высокой химической активностью и чрезвычайно большой теплотой сгорания. Представляют интерес как ракетное топливо. В органическом синтезе находит применение реакция присоединения борана и некоторых алкилборанов к двойной связи алкенов с вовлечением полученных соединений в дальнейшие превращения.
Содержание
Получение бороводородов
Бороводороды являются недостаточно устойчивыми термодинамически соединениями бора и водорода, и в этой связи, главными методами их производства являются косвенные методы. На сегодняшний день одним из основных способов получения бороводородов является т.наз «магниевый метод» или «Способ Стока», то есть получение борида магния и последующее разложение последнего соляной кислотой. Полученные бораны(бороводороды) подвергают вакуумной разгонке, очистке и накапливают разделенные отдельные бороводороды в соответствующих условиях для сохранения и дальнейшего использования. Другим важным промышленным способом получения бороводородов является способ предложенный впервые Шлезингером и Бургом. Способ заключается в реакции треххлористого бора с с водородом в Вольтовой дуге высокого напряжения. Полученный в нем гидрохлороборан подвергают диспропорционированию при охлаждении до комнатной температуры, и разделению диборана и треххлористого бора. Выход диборана приближается к 55 % вес. В дальнейшем Шлезингер и Браун предложили новый способ эффективного получения бороводородов путем реакции обмена между боргидридом натрия и трехфтористым бором. Все высшие «бораны» получают исключительно путем термического крекинга диборана.
Свойства бороводородов

Диборан 
Декаборан 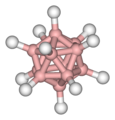
Додекаборан Физические характеристики важнейших бороводородовФормула Температура плавления °С Температура кипения °С Плотность г/см3 Теплота обр,298,15°К, ккал/моль Терм.стабильность. Реакция с воздухом. Реакция с Н2О. В2Н6 −165,5 °C −92,5 °C тв.0,577-183, ж.0,447-112 +9,8(газ) Стаб при 25 °C Самовоспл Мгновенно гидролизуется В4Н10 −120,0 °C +18 °C ж.0,56-36 +7,53(газ) Разл при 25 °C Самовоспл в прис воды Гидролизуется 24 ч В5Н9 −46,81 °C +62 °C ж.0,610 +10,240(жидк) +17,5(газ) Стаб при 25 °C Самовоспл Гидролизуется при нагревании В5Н11 −123 °C +63 °C +22,2(газ) Медл разл при 150 °C Самовоспл Гидролизуется быстро В6Н10 −62,3 °C 110 °C ж.0,69о +19,6(газ) Разл при 25 °C Стабилен Гидролизуется при нагревании В6Н12 −90 °C °С Разл при 25 °C Стабилен Гидролизуется при нагревании В9Н15 +2,6 °C °С Разл при 25 °C Стабилен Гидролизуетс при нагревании В10Н14 +98,78 °C +219 °C тв.0,9425, ж.0,78100 −6,9(тв) −1,7(жидк) +11,3(газ) Стаб при 150 °C Очень стабилен Медленно гидролизуется Бороорганические соединения в качестве ракетного топлива
Основная статья - «Пентаборан»
Наиболее удобен для синтеза и применения Пентаборан—9. Остальные бороводороды интенсивно изучаются и их применение в настоящее время ограничено. Видами топлива, производными от бора, являются пропилпентаборан (US: BEF-2) и этилпентаборан (US: BEF-3).[1] Диборан, декаборан и их производные также исследовались на предмет перспективности использования.
Токсичность и огнеопасность
Бороводороды — ядовитые вещества, имеющими помимо общетоксической составляющей, так же особое, но довольно сильно выраженное нервнопаралитическое воздействие на человека и животных. Как огнеопасные вещества, бороводороды представляют собой в основном вещества с наивысшей категорией огнеопасности и способны к самовоспламенению не только на воздухе но и и при контактах с водой и рядом галогенопроизводных углеводородов. При горении их на воздухе развиваются высокие температуры.
Смотри также
- Бор
- Боргидриды
Примечания
- ↑ МакДональд Г. Теплоустойчивость промышленного пропилпентаборана (BEF-2) в диапазоне температур 147-190°C (en). Национальный совещательный комитет по аэронавтике (США). (13 Ноября 1957 года).
Литература
Wikimedia Foundation. 2010.

