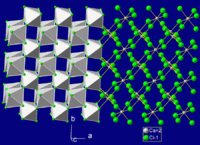
- Хлорид хрома(II)
-
Дихлорид хрома Общие Систематическое наименование хлорид хрома(II) Химическая формула CrCl2 Физические свойства Молярная масса 122.902 г/моль Плотность 2.9 г/см³ Термические свойства Температура плавления 824 °C Температура кипения 1120 °C Химические свойства Растворимость в воде растворим г/100 мл Структура Координационная геометрия октаэдрическая, 6-ти координированная Кристаллическая структура орторомбическая, oP6 Классификация Рег. номер CAS 10049-05-5 RTECS GB5250000 Безопасность ЛД50 (орально, крысы) 1870 мг/кг Токсичность 
Хлори́д хро́ма(II) CrCl2 — белые, чрезвычайно гигроскопичные кристаллы, растворимые в воде. Нерастворим в диэтиловом эфире, малорастворим в спирте.
Содержание
Свойства
Водные растворы имеют голубой цвет. Образует комплексы с аммиаком, гидразином, дипиридилом и другими соединениями.
Получение
Получают восстановлением CrCl3 водородом при 700 °C:
2CrCl3 + H2 → 2CrCl2 + 2HCl,
взаимодействием CrCl3 с алюмогидридом лития:
4CrCl3 + Li[AlH4] → 4CrCl2 + LiCl + AlCl3 + 2H2↑,
взаимодействием атомарного водорода с CrCl3:
2CrCl3 + 2Zn + 2HCl → 2CrCl2 + 2ZnCl2 + H2↑
Zn + 2Н+ = Zn2+ + 2[H], 2[H] = H2
или взаимодействием соляной кислоты с хромом в инертной атмосфере (в присутствии воздуха образуется CrCl3):
Cr + 2HCl → CrCl2 + H2↑.
Химические свойства
CrCl2 — сильный восстановитель. Как и многие другое соединения Cr(II), CrCl2 легко окисляется:
2CrCl2 + 2HCl → 2CrCl3 + H2↑.
Взаимодействием солей Cr(II) со щелочами в инертной атмосфере можно получить жёлтый осадок гидроксида хрома(II) Cr(OH)2:
CrCl2 + 2KOH → Cr(OH)2↓ + 2KCl.
Применение
Применяют в хроматометрии, как катализатор при синтезе многих органических соединений.
Физиологическое действие
CrCl2 — раздражающее вещество.
Соединения хромаБихромат аммония ((NH4)2Cr2O7) • Борид хрома (CrB) • Бромид хрома(II) (CrBr2) • Бромид хрома(III) (CrBr3) • Гексагидроксохромат (III) натрия (Na3[Сr(OH)6]) • Гексакарбонил хрома (Cr(CO)6) • Гидроксид хрома (III) (Cr(OH)3) • Гидроксид хрома(II) (Cr(OH)2) • Двухромовая кислота (H2Cr2O7) • Диоксид-дихлорид хрома (CrO2Cl2) • Дихромат калия (K2Cr2O7) • Дихромат лития (Li2Cr2O7) • Дихромат натрия (Na2Cr2O7) • Дихромат рубидия (Rb2Cr2O7) • Дихромат цезия (Cs2Cr2O7) • Зелень Гинье (Cr2O3•nH2O) • Иодид хрома(II) (CrI2) • Иодид хрома(III) (CrI3) • Карбид хрома(II) (Cr3C2) • Нитрат хрома (Cr(NO3)3) • Нитрид хрома (CrN) • Оксид хрома(II) (CrO) • Оксид хрома(III) (Cr2O3) • Оксид хрома(IV) (CrO2) • Оксид хрома(VI) (CrO3) • Оксифторид хрома(III) (CrOF) • Ортофосфат хрома(III) (CrPO4) • Пероксид хрома(VI) (CrO5) • Сульфат хрома(II) (CrSO4) • Сульфат хрома(III) (Cr2(SO4)3) • Сульфид хрома(II) (CrS) • Сульфид хрома(III) (Cr2S3) • Сульфат хрома(III)-калия (KCr(SO4)2) Фосфат хрома (CrPO4) • Фосфид хрома (CrP) • Фторид хрома(II) (CrF2) • Фторид хрома(III) (CrF3) • Фторид хрома(IV) (CrF4) • Фторид хрома(V) (CrF5) • Фтористый хромил (CrO2F2) • Хлорид гексаамминхрома(III) ([Сr(NH3)6]Cl3) • Хлорид хрома(II) (CrCl2) • Хлорид хрома(III) (CrCl3) • Хлорид хрома(IV) (CrCl4) • Хлористый хромил (CrO2Cl2) • Хромат аммония ((NH4)2CrO4) • Хромат калия (K2CrO4) • Хромат лития (Li2CrO4) • Хромат натрия (Na2CrO4) • Хромат рубидия (Rb2CrO4) • Хромат серебра (Ag2CrO4) • Хромат цезия (Cs2CrO4) • Хромит железа(II) (Fe(CrO2)2) • Хромит калия (KCrO2) • Хромовая кислота (H2CrO4) •
 Категории:
Категории:- Соединения хрома
- Хлориды
- Бинарные соединения
- Галогениды металлов
Wikimedia Foundation. 2010.