- Диоксид селена
-
Диоксид селена 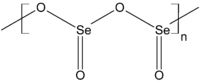


Общие Систематическое наименование Диоксид селена Традиционные названия Окись селена Химическая формула SeO2 Физические свойства Состояние (ст. усл.) бесцветные кристаллы Молярная масса 110,96 г/моль Плотность 3,954 г/см³ Термические свойства Температура плавления под давл. 340; 389 °C Температура кипения субл. 315 °C Молярная теплоёмкость (ст. усл.) 58,3 Дж/(моль·К) Энтальпия образования (ст. усл.) -225 кДж/моль Химические свойства Растворимость в воде 264 г/100 мл Растворимость в этаноле 6,7 г/100 мл Оптические свойства Показатель преломления 1,76 Классификация Рег. номер CAS 7446-08-4 Рег. номер PubChem 24007 SMILES O=[SeH2]=O RTECS VS8575000 Диоксид селена — неорганическое соединение селена и кислорода с формулой SeO2, бесцветные кристаллы, пары́ имеют желтовато-зелёный цвет и запах гнилой редьки, реагирует с водой.
Содержание
Получение
- В природе встречается минерал селенолит (доунеит) — SeO2. Описан в виде игольчатых кристаллов с церусситом и молибдоменитом, встречается в Качеута (Аргентина).
- Окисление селена:
- Действие перегретого пара на селен:
- Окисление селена горячей концентрированной серной кислотой:
- Окисление красного селена иодноватой кислотой:
- Окисление селена горячей концентрированной селеновой кислотой:
- Разложение триоксида селена:
- Разложение селенистой кислоты:
Физические свойства
Диоксид селена образует бесцветные кристаллы тетрагональная сингонии, пространственная группа P 4/mbc, параметры ячейки a = 0,8353 нм, c = 0,5051 нм, Z = 8.
В твёрдом состоянии диоксид селена является полимером. Газовая фаза состоит из нелинейных мономеров (по геометрии похожих на диоксид серы).
При возгонке образует пары́ желтовато-зелёного цвета и с запахом гнилой редьки.
Легко растворяется в воде, вступая в реакцию с ней, растворяется в этаноле, уксусной и серной кислотах. Мало растворим в бензоле, не растворим в ацетоне.
С безводным хлористым водородом образует аддукты вида SeO2•4HCl.
Химические свойства
- Реагирует с водой образуя селенистую кислоту:
- Реагирует с гидроксидами металлов образуя селениты:
- Обратимо разлагается при сильном нагревании:
- Реагирует с галогеноводородами:
- Растворённый в серной кислоте диоксид селена реагирует с хлороводородом с образованием оксихлорида селена (аналог тионилхлорида):
- Реагирует с тионилхлоридом с образованием тетрахлорида селена:
- Окисляется концентрированной перекисью водорода:
- Восстанавливается сероводородом:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
 Категории:
Категории:- Соединения селена
- Оксиды
Wikimedia Foundation. 2010.

![\mathsf{Se + O_2 \ \xrightarrow[NO_2]{250^oC}\ SeO_2 }](ca1b1d1ebf5e0de3a5cca2df0e358b0f.png)









![\mathsf{SeO_2 + HCl \ \xrightarrow{}\ H_2[SeO_2Cl_2] }](7fe7da3aa76c1b1b4030b053dbc06bfd.png)



