- Хлорид висмута(III)
-
Хлорид висмута(III) 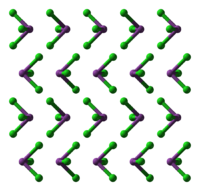
Общие Систематическое наименование Хлорид висмута(III) Традиционные названия Хлорид висмута, трихлорид висмута Химическая формула BiCl3 Эмпирическая формула BiCl3 Физические свойства Состояние (ст. усл.) твёрдое Молярная масса 315,34 г/моль Плотность 4,75[1] г/см³ Термические свойства Температура плавления 234[2] °C Температура кипения 440[2] °C Критическая точка 905 °С, 11,97 МПа[3] Молярная теплоёмкость (ст. усл.) 109[3] Дж/(моль·К) Энтальпия образования (ст. усл.) −378[4] кДж/моль Давление пара (при 343 °С) 1,33·104[3] Классификация Рег. номер CAS 7787-60-2 Безопасность ЛД50 (крысы, орально) 3324 мг/кг Токсичность Хлори́д ви́смута(III) (трихлорид висмута, хлористый висмут) — BiCl3, неорганическое бинарное соединение висмута с хлором, висмутовая соль хлороводородной кислоты. В нормальных условиях представляет собой белое (бесцветное) или бледно-жёлтое кристаллическое, очень гигроскопичное вещество.
Содержание
Молекулярная и кристаллическая структура
Хлорид висмута имеет следующий элементный состав: Bi (66,27 %), Cl (22,73 %). Энергия разрыва связи в соединении (Есв.): 275 кДж/моль, длина связи Bi—Cl: 0,248 нм, валентный угол Cl—Bi—Cl составляет 100°[5][6]. Молекула соединения представляет собой тригональную пирамиду, у которой вершина — атом висмута — имеет неподелённую электронную пару, что делает BiCl3 сильной кислотой Льюиса.
Кристаллическая структура BiCl3 кубическая.
Физические свойства
Хлорид висмута — белое или бледно-жёлтое, в кристаллическом виде — бесцветное вещество, плавящееся (T пл.= 234 °С) и кипящее без разложения (T кип.= 440 °С). Гигроскопичен, образует кристаллогидрат: BiCl3 • H2O[1].
Водой гидролизуется; растворим в метаноле, этаноле, ацетоне[1][3].
Термодинамические константы:
- стандартная энтальпия образования, ΔHo298: −378 кДж/моль[4];
- стандартная энтропия, So298: 172 Дж/(моль·K)[4];
- стандартная энергия Гиббса, ΔGo298: −313 кДж/моль[4].
- стандартная мольная теплоемкость, Cpo298: 109 Дж/(моль·K)[3];
- энтальпия плавления, ΔHпл: 23,47 кДж/моль [7];
- энтальпия кипения, ΔHкип: 72,59 кДж/моль [7].
Получение
- Прямая реакция элементов при 200 °С:
- 2Bi + 3Cl2 = 2BiCl3.
- Взаимодействие оксида висмута(III) с концентрированной соляной кислотой при нагревании:
- Bi2O3 + 6HCl = 2BiCl3 + 3H2O.
Химические свойства
- Гидролизуется водой:
- BiCl3 + H2O → Bi(Cl)O + 2HCl.
- В солянокислом растворе устойчив, склонен образовывать комплексы — хлорвисмутаты (III):
- BiCl3 + Cl− = [BiCl4]−.
- [BiCl4]− + Cl− = [BiCl5]2−.
- [BiCl5]2− + Cl− = [BiCl6]3−.


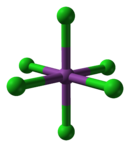
Cs3[BiCl6] Cs3[BiCl6] [BiCl6]3− - Реагирует с водными растворами щелочей с образованием гидроксида:
- BiCl3 + 3NaOH = Bi(OH)3↓ + 3NaCl.
- При сильном нагревании до 1000°С разлагается до хлорида висмута(I):
- BiCl3 → BiCl + Cl2
Применение
Висмут хлористый используется для получения других солей висмута, в качестве катализатора в органическом синтезе и как компонент пигментов и косметических средств[1].
См. также
Безопасность
Примечания
- ↑ 1 2 3 4 Patnaik P. Handbook of Inorganic Chemicals. — McGraw-Hill, 2003. — P. 109—110. — ISBN 0-07-049439-8
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Глава 3. Физические свойства // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 85. — ISBN 5-7107-8085-5
- ↑ 1 2 3 4 5 Серебра хлорид. Справочник по веществам. XuMuK.ru. Архивировано из первоисточника 20 апреля 2012. Проверено 1 марта 2010.
- ↑ 1 2 3 4 Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть IV. Глава 1. Энтальпия образования, энтропия и энергия Гиббса образования веществ // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 452. — ISBN 5-7107-8085-5
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть III. Глава 5. Энергия и длина связи для двухатомных частиц // Константы неорганических веществ: справочник / Под редакцией проф. Р. А. Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 387. — ISBN 5-7107-8085-5
- ↑ Лидин Р. А., Андреева Л. Л., Молочко В. А. Часть III. Глава 7.1. Геометрическая форма, длина связей и валентные углы в частицах с одним центральным атомом sp-элемента // Константы неорганических веществ: справочник / Под редакцией проф. Р. А. Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 396. — ISBN 5-7107-8085-5
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть IV. Глава 2. Энтальпия и энтропия фазовых переходов // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 532. — ISBN 5-7107-8085-5
Литература
Ссылки
Категории:- Соединения висмута
- Хлориды
- Галогениды металлов
Wikimedia Foundation. 2010.