- Правило n l
-
Правило Клечковского (также Правило n+l; за рубежом обычно используется название правило Маделунга) — эмпирическое правило, описывающее энергетическое распределение орбиталей в многоэлектронных атомах.
Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитального квантовых чисел 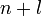 . При одинаковой сумме раньше заполняется орбиталь с меньшим значением
. При одинаковой сумме раньше заполняется орбиталь с меньшим значением 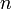 .
.
Правило n+l предложено в 1936 г. немецким физиком Э. Маделунгом; в 1951 г. было вновь сформулировано В. М. Клечковским.Содержание
Распределение электронов по орбиталям в водородоподобных и многоэлектронных атомах
По мере увеличения суммарного числа электронов в атомах (при возрастаний зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра. Поэтому энергетическая последовательность орбиталей в водородоподобном атоме выглядит просто:
1s<2s=2p<3s=3p=3d<4s=4p=4d=4f<5s...Здесь орбитальная энергия электрона повышается только по мере увеличения главного квантового числа и и не меняется при увеличении орбитального квантового числа l; состояния с различными значениями l, но с одним и тем же значением n (например, 3s, Зр, 3d) энергетически эквивалентны, то есть соответствующие атомные орбитали (3s, Зр, 3d) обладают одинаковой энергией и оказываются энергетически вырожденными (не путать обсуждаемое вырождение по энергии атомных орбиталей различного типа в гипотетических водородоподобных атомах с энергетическим вырождением атомных орбиталей одного и того же типа, например Зрx, Зру и Зрz в реальных изолированных атомах).
В многоэлектронных атомах в результате эффекта межэлектронных взаимодействий происходит энергетическое расщепление (расхождение) орбиталей различного типа, но с одним и тем же значением главного квантового числа (3s<3p<3d и т. д.). Если бы это расщепление было небольшим и меньшим расщепления по энергии атомных орбиталей под воздействием изменения главного квантового числа n, то энергетическая последовательность атомных орбиталей выглядела бы так:
1s«2s<2p"3s<3p<3d"4s<4p<4d<4f"5s...В действительности же расщепление по l, начиная с n≥З, оказывается большим, чем расщепление по n. Сложный характер явления межэлектронных взаимодействий предопределяет сильную зависимость орбитальной энергии каждого электрона уже не только от пространственной удаленности его зарядовой плотности от ядра (от главного квантового числа n), но и от формы его движения в поле ядра (от орбитального квантового числа l). Именно межэлектронное взаимодействие приводит к резко усложнённой (по сравнению с вышеописанной) энергетической последовательности заселяющихся электронами атомных орбиталей. Итак, в реальных многоэлектронных атомах картина энергетического распределения орбиталей оказывается очень сложной. Строгая квантовомеханическая теория электронного строения атомов и экспериментальная спектроскопия обнаруживают энергетическую последовательность атомных орбиталей в следующем виде:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f≅5d<6p<7s<5f≅6d<7p<8s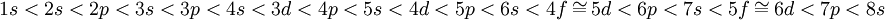
Формулировка правила Клечковского
Эта энергетическая последовательность легко может быть описана при помощи эмпирического правила суммы двух первых квантовых чисел, разработанного в 1951-м году В. М. Клечковским и иногда называемого правилом (n+l). Это правило основано на зависимости орбитальной энергии от квантовых чисел n и l и описывает энергетическую последовательность атомных орбиталей как функцию суммы
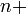 l. Суть его очень проста:
l. Суть его очень проста:орбитальная энергия последовательно повышается по мере увеличения суммы
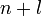 , причём при одном и том же значении этой суммы относительно меньшей энергией обладает атомная орбиталь с меньшим значением главного квантового числа
, причём при одном и том же значении этой суммы относительно меньшей энергией обладает атомная орбиталь с меньшим значением главного квантового числа 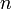 . Например, при
. Например, при 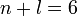 орбитальные энергии подчиняются последовательности
орбитальные энергии подчиняются последовательности 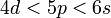 , так как здесь для
, так как здесь для 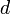 -орбитали главное квантовое число наименьшее
-орбитали главное квантовое число наименьшее 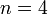 , для
, для  -орбитали
-орбитали  ; наибольшее
; наибольшее  ,
, 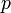 -орбиталь занимает промежуточное положение
-орбиталь занимает промежуточное положение 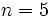 .
.Или же:
При заполнении орбитальных оболочек атома более предпочтительны (более энергетически выгодны), и, значит, заполняются раньше те состояния, для которых сумма главного квантового числа
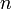 и побочного (орбитального) квантового числа
и побочного (орбитального) квантового числа 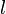 , т.е.
, т.е. 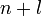 , имеет меньшее значение.
, имеет меньшее значение.Правило (n+l) в целом хорошо иллюстрирует таблица 1, где по мере постепенного возрастания суммы (n+l) приведена энергетическая последовательность атомных орбиталей. В этой таблице не указаны, естественно, нереальные (запрещенные квантовой механикой атома) варианты, для которых не выполняется обязательное требование n>l, в частности не указаны комбинации для (n+l)=6:
n 1 2 3 l 5 4 3 Таблица 1. Энергетическая последовательность орбиталей в изолированных атомах (n+l) n l Атомные орбитали 1 1 0 1s Первый период 2 2 0 2s Второй период 3 2 1 2p 3 0 3s Третий период 4 3 1 3p 4 0 4s Четвёртый период 5 3 2 3d 4 1 4p 5 0 5s Пятый период 6 4 2 4d 5 1 5p 6 0 6s Шестой период 7 4 3 4f 5 2 5d 6 1 6p 7 0 7s Седьмой период 8 5 3 5f 6 2 6d 7 1 7p 8 0 8s Начало восьмого периода Приведённую в таблице очерёдность заполнения электронами атомных орбиталей удобно представить в виде схемы:
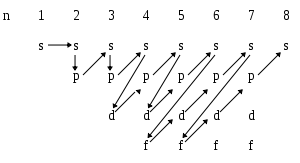
Исключения из правила Клечковского
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречат реальной энергетической последовательности атомных орбиталей только в двух однотипных случаях, а именно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d, а не 4f, и только затем происходит заселение четырнадцатью электронами 4f орбиталей, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и для орбиталей 7s, 6d и 5f. Объяснение этого факта см. в статье Физическое объяснение очерёдностей заселения орбиталей атомов электронами.
При написании статьи использована следующая литература:
- Корольков Д. В. Основы неорганической химии. — М.:»Просвещение", 1982. — 271 с.
Мнемоническое правило
Нас арифметикой банальною
не мучай,
Над нами лишь Клечковский -
господин,
А он сказал, что 3+2
получше
Чем, например, 4+1См. также
Wikimedia Foundation. 2010.
