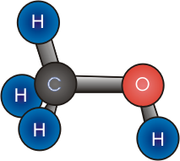
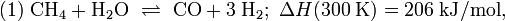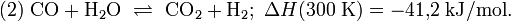- Метиловый спирт
-
Метанол 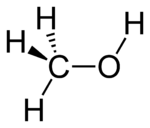
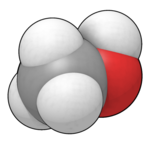
Общие свойства Молекулярная формула CH3OH Молярная масса 32,04 г/моль Внешний вид бесцветная жидкость Номер CAS [67-56-1] Свойства Плотность и
агрегатное состояние791,8 кг/м³, жидкость Растворимость в воде Полностью растворим Температура плавления −97 °C (176,15 K) Температура кипения 64,7 °C (337,85 K) Тройная точка −97,7 °C (175,45 K), ? бар Критическая точка 240 °C (513,15 K), 78.5 бар pKa ~15,5 Вязкость 0,59 Пз при 20 °C Поверхностное натяжение 22,5•10-3 Н/м при 20 °C Строение Форма молекулы Тетраэдр с изгибом Дипольный момент 1,69 D (газ) Опасность Температура
вспышки11 °C Температура
самовоспламенения436 °C (709,15 K) Пределы взрываемости 6,72 — 36,5 % Родственные соединения Родственные спирты Этанол
БутанолДругие соедининия Диметиловый эфир
МетилхлоридМетано́л (метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила) — CH3OH, простейший одноатомный спирт, бесцветная ядовитая жидкость. Метанол — это первый представитель гомологического ряда одноатомных спиртов.
С воздухом образует взрывоопасные смеси (температура вспышки 11 °C). Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.
Содержание
Получение
До 1960-х годов метанол синтезировали только на цинкхромовом катализаторе при температуре 300—400°С и давлении 25—40 МПа (= 250—400 Бар = 254,9—407,9 кгс/см²). Впоследствии распространение получил синтез метанола на медьсодержащих катализаторах (медьцинкалюмохромовом, медь-цинкалюминиевом или др.) при 200—300°С и давлении 4—15 МПа (= 40—150 Бар = 40,79—153 кгс/см²).
Современный промышленный метод получения — каталитический синтез из оксида углерода(II) (CO) и водорода (2H2) при следующих условиях:
- температура — 250 °C,
- давление — 7МПа (= 70 Бар = 71,38 кгс/см²),
- катализатор — смесь ZnO (оксид цинка) и CuO (оксид меди(II)):
До промышленного освоения каталитического способа получения метанол получали при сухой перегонке дерева (отсюда его название «древесный спирт»). В данное время этот способ имеет второстепенное значение.
Также известны схемы использования с этой целью отходов нефтепереработки, коксующихся углей.
CO2 + 3H2 <--> CH3OH + H2O + 49.53 кДж/моль
H2O + CO <--> CO2 + H2 + 41.2 кДж/моль
Молекулярная формула — CH4O или CH3—OH, а структурная:
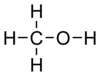 В настоящее время метиловый спирт добывают синтетическим способом из монооксида углерода и водорода при температуре 300—400°С и давления 300—500 атм в присутствии катализатора — смеси оксидов цинка, хрома и др. Сырьем для синтеза метанола служит синтез-газ (CO + H2), обогащенный водородом: :CO + 2 H2 → CH3OH[1]
В настоящее время метиловый спирт добывают синтетическим способом из монооксида углерода и водорода при температуре 300—400°С и давления 300—500 атм в присутствии катализатора — смеси оксидов цинка, хрома и др. Сырьем для синтеза метанола служит синтез-газ (CO + H2), обогащенный водородом: :CO + 2 H2 → CH3OH[1]Производство метанола (в тыс. тон):
год США Германия Мир Продажная цена ($/т) 1928 24 18 нет данных нет данных 1936 97 93 нет данных нет данных 1950 360 120 нет данных нет данных 1960 892 297 нет данных 99,7 1970 2238 нет данных 5000 89,7 1980 3176 870 15000 236,1 2004 3700 2000 32000 270 Применение
В органической химии метанол используется в качестве растворителя.
Метанол используется в газовой промышленности для борьбы с образованием гидратов (из-за низкой температуры замерзания и хорошей растворимости). В органическом синтезе метанол применяют для выпуска формальдегида и формалина, уксусной кислоты, ряда эфиров (например, МТБЭ и ДМЭ), изопрена и др.
Наибольшее его количество идёт на производство формальдегида, который используется для производства фенолформальдегидных смол. Значительные количества CH3OH используют в лакокрасочной промышленности для изготовления растворителей при производстве лаков. Кроме того, его применяют (ограниченно из-за гигроскопичности и отслаивания) как добавку к жидкому топливу для двигателей внутреннего сгорания. Используется в топливных элементах.
Благодаря высокой скорости распространения пламени воздушной смеси и высокой теплоте испарения используется для заправки гоночных мотоциклов и автомобилей. Метанол горит в воздушной среде и при его окислении образуется двуокись углерода и вода:
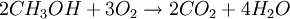
Для получения биодизеля растительное масло переэтерифицируется метанолом при температуре 60 °C и нормальном давлении приблизительно так: 1 т масла + 200 кг метанола + гидроксид калия или натрия.
Во многих странах метанол применяется в качестве денатурирующей добавки к этанолу при производстве парфюмерии. В России использование метанола в потребительских товарах запрещено.
При добыче газа гидраты могут образовываться в стволах скважин, промысловых коммуникациях и магистральных газопроводах. Отлагаясь на стенках труб, гидраты резко уменьшают их пропускную способность. Для борьбы с образованием гидратов на газовых промыслах вводят в скважины и трубопроводы различные ингибиторы (метиловый спирт, гликоли).
Работа топливных элементов основаны на реакции окисления метанола на катализаторе в диоксид углерода. Вода выделяется на катоде. Протоны (H+) проходят через протонообменную мембрану к катоду где они реагируют с кислородом и образуют воду. Электроны проходят через внешнюю цепь от анода к катоду снабжая энергией внешнюю нагрузку.
Реакции:
На аноде CH3OH + H2O → CO2 + 6H+ + 6e-
На катоде 1.5O2 + 6H+ + 6e- → 3H2O
Общая для топливного элемента: CH3OH + 1,5O2 → CO2 + 2H2O
Получение муравьиной кислоты окислением метанола:

Получение диметилового эфира дегидратацией метанола при 300-400 °С и 2-3 МПа в присутствии гетерогенных катализаторов - алюмосиликатов - степень превращения метанола в диметиловый эфир - 60% или цеолитов - селективность процесса близка к 100%. Диметиловый эфир (C2H6O) — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90% меньше, чем у бензина. Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53.
Метил-трет-бутиловый эфир получается при взаимодействии метанола с изобутиленом в присутствии кислых катализаторов (например, ионообменных смол).
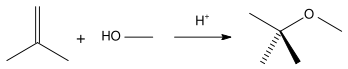
Метил-трет-бутиловый эфир (C5H12O) применяется в качестве добавки к моторным топливам, повышающей октановое число бензинов (антидетонатор). Максимальное законодательное содержание МТБЭ в бензинах Европейского союза — 15%, в Польше — 5%. В России в среднем составе бензинов содержание МТБЭ составляет до 12% для АИ92 и до 15% для АИ95, АИ98.
Биометанол
Промышленное культивирование и биотехнологическая конверсия морского фитопланктона рассматривается как одно из наиболее перспективных направлений в области получения биотоплива.[2]
В начале 80-х рядом европейских стран совместно разрабатывался проект, ориентированный на создание промышленных систем с использованием прибрежных пустынных районов. Осуществлению этого проекта помешало общемировое снижение цен на нефть.
Первичное производство биомассы осуществляется путём культивирования фитопланктона в искусственных водоёмах, создаваемых на морском побережье.
Вторичные процессы представляют собой метановое брожение биомассы и последующее гидроксилирование метана с получением метанола.
Основными доводами в пользу использования микроскопических водорослей являются следующие:
- высокая продуктивность фитопланктона (до 100 т/га в год);
- в производстве не используются ни плодородные почвы, ни пресная вода;
- процесс не конкурирует с сельскохозяйственным производством;
- энергоотдача процесса достигает 14 на стадии получения метана и 7 на стадии получения метанола;
С точки зрения получения энергии данная биосистема имеет существенные экономические преимущества по сравнению с другими способами преобразования солнечной энергии.
Метанол в качестве топлива
При применении метанола в качестве топлива следует отметить, что объемная и массовая энергоемкость (теплота сгорания) метанола на 40-50% меньше, чем бензина, однако при этом теплопроизводительность спиртовоздушных и бензиновых топливовоздушных смесей при их сгорании в двигателе различается незначительно по той причине, что высокое значение теплоты испарения метанола способствует улучшению наполнения цилиндров двигателя и снижению его теплонапряженности, что приводит к повышению полноты сгорания спиртовоздушной смеси. В результате этого рост мощности двигателя повышается на 10-15%. Двигатели гоночных автомобилей работающих на метаноле с более высоким октановым числом чем бензин имеют степень сжатия, превышающую 15:1, в то время как в обычном карбюраторном ДВС степень сжатия для неэтилированного бензина как правило не превышает 10.1:1. Метанол может использоваться как в классических двигателях внутреннего сгорания, так и в специальных топливных элементах для получения электричества.
Недостатки:
- метанол травит алюминий. Проблемным является использование алюминиевых карбюраторов и инжекторных систем подачи топлива в ДВС.
- гидрофильность. Метанол втягивает воду, что является причиной засорения систем подачи топлива в виде желеобразных ядовитых отложений.
- метанол, как и этанол, повышает пропускную способность пластмассовых испарений для некоторых пластмасс (например плотного полиэтилена). Эта особенность метанола повышает риск увеличения эмиссии летучих органических веществ, что может привести к повышению концентрации озона и возможно усилению солнечной радиации.
- уменьшенная летучесть при холодной погоде: Моторы, работающие на метаноле могут иметь проблемы с запуском и отличатся повышенным расходом топлива до достижения рабочей температуры.
- метанол может сравнительно быстро попасть в источники питьевой воды и отравить её. Этот сценарий исследован пока недостаточно, но к сожалению существует опыт утечки Метил-трет-бутилового эфира и загрязнения воды.
Свойства М. спирта и его реакции.
При написании этой статьи использовался материал из Энциклопедического словаря Брокгауза и Ефрона (1890—1907).М. спирт есть бесцветная жидкость с запахом, напоминающим запах этилового спирта. Температура кипения 66,78° (Renault); 64,8° (Vincent и Delachanal); 65,75-66,25° (Grodzki и Kr ä mer); 65,8-66° (Perkin); 64,96° при 760 мм (Dittmar и Fawsitt); 64,8° при 763 мм (Schiff). Удельный вес при 0°/0° = 0,8142 (Kopp); при 15°/15° = 0,79726; при 25°/25° = 0,78941 (Perkin); при 64,8°/4° = 0,7476 (Schiff); при 0°/4° = 0,81015; при 15,56°/4° = 0,79589 (Dittmar и Fawsitt). Капиллярная постоянная при температуре кипения a 2 =5,107 (Шифф); Критическая температура 241,9° (Шмидт). Упругость пара при 15° = 72,4 мм; при 29,3° = 153,4 мм; при 43° = 292,4 мм; при 53° = 470,3 мм; при 65,4° = 756,6 мм (Д. Коновалов). Теплота горения равна 170,6, теплота образования 61,4 (Штоман, Клебер и Лангбейн). М. спирт смешивается во всех отношениях с водой, этиловым спиртом и эфиром; при смешении с водой происходит сжатие и разогревание. Горит синеватым пламенем. Подобно этиловому спирту - сильный растворитель, вследствие чего во многих случаях может заменять этиловый спирт. В крепких водных растворах М. спирт, принятый внутрь, ядовит. Безводный М. спирт, растворяя небольшое количество медного купороса, приобретает голубовато-зеленое окрашивание, поэтому безводным медным купоросом нельзя пользоваться для открытия следов воды в М. спирте; но он не растворяет CuSO 4.7H2 O (Клепль). М. спирт дает со многими солями соединения, подобные кристаллогидратам, например: CuSO 4.2СН 3 ОН; LiCl.3СН 3 ОН; MgCl 2.6СН 3 ОН; CaCl 2.4СН 3 ОН представляет собой шестисторонние таблицы, разлагаемые водой, но не разрушаемые нагреванием до 100° (Kane). Соединение ВаО.2СН 3 ОН.2Н 2 О получается в виде блестящих призм при растворении ВаО в водном М. спирте и испарении на холоде полученной жидкости при комнатной температуре (Форкранд). С едкими щелочами М. спирт образует соединения 5NaOH.6СН 3 ОН; 3KOH.5СН 3 OH (Геттиг). При действии металлических калия и натрия легко дает алкоголяты, присоединяющие к себе кристаллизационный М. спирт и иногда воду. При пропускании паров М. спирта через докрасна накаленную трубку получается C 2H2 и др. продукты (Бертело). При пропускании паров М. спирта над накаленным цинком получается окись углерода, водород и небольшие количества болотного газа (Jahn). Медленное окисление паров М. спирта при помощи раскаленной платиновой или медной проволоки представляет лучшее средство для получения больших количеств формальдегида: 2СН 3 ОН+О 2 =2НСНО+2Н 2 О. При действии хлористого цинка и высокой температуры М. спирт дает воду и углеводороды формулы С n Н 2n+2, а также небольшие количества гексаметилбензола (Лебедь и Грин). М. спирт, нагретый с нашатырем в запаянной трубке до 300°, дает моно-, ди- и триметиламины (Бертело). С белильной известью не дает хлороформа (Гольдберг). При пропускании паров М. спирта над едким кали при высокой температуре выделяется водород и образуются последовательно муравьинокислый, щавелевокислый и, наконец, углекислый калий; концентрированная серная кислота дает метилсерную кислоту CH 3HSO4, которая при дальнейшем нагревании с М. спиртом дает метиловый эфир (см.). При перегонке М. спирта с избытком серной кислоты в отгон переходит диметилсерная кислота (CH 3)2SO4. При действии серного ангидрида SO 3 получается CH(OH)(SO 3H)2 и CH 2(SO3H)2 (см. Метилен). М. спирт при действии соляной кислоты, пятихлористого фосфора и хлористой серы дает хлористый метил СН 3 Cl. Действием HBr и H 2SO4 получают бромистый метил. Подкисленный 5%-й серной кислотой и подвергнутый электролизу, М. спирт дает СО 2, СО, муравьинометиловый эфир, метилсерную кислоту и метилаль СН 2 (ОСН 3)2 (Ренар). При нагревании М. спирта с хлористо-водородными солями ароматических оснований (анилином, ксилидином, пиперидином) легко происходит замещение водорода в бензольном ядре метилом (Гофман, Ладенбург); реакция имеет большое техническое значение при приготовлении метилрозанилина и др. искусственных пигментов.
Здравоохранение

Метанол — яд, действующий на нервную и сосудистую системы. Токсическое действие метанола обусловлено так называемым «летальным синтезом» — метаболическим окислением в организме до очень ядовитого формальдегида. Приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению (одно из последствий — слепота), а 30 мл и более — к смерти.
Особая опасность метанола связана с тем, что по запаху и вкусу он неотличим от этилового спирта, из-за чего и происходят случаи употребления метанола внутрь.
Как указано в электронном справочном руководстве для врача скорой медицинской помощи, при отравлении метанолом антидотом является этанол, который вводится внутривенно в форме 10 % раствора капельно или 30—40 % раствора перорально из расчёта 1—2 грамма раствора на 1 кг веса в сутки.[3] Полезный эффект в этом случае обеспечивается отвлечением АДГ I на окисление экзогенного этанола.[4]
Следует учесть, что при недостаточно точном диагнозе за отравление метанолом можно принять алкогольную интоксикацию, отравление дихлорэтаном или четырёххлористым углеродом — в этом случае введение дополнительного количества этилового спирта опасно.[3]
Интересные факты
Изабелла американский сорт винограда. В последнее время, под предлогом о повышенном содержаниии метанола в винах, получаемых из данного сорта, запрещен к использованию в коммерческом виноделии в США и странах Евросоюза. Вероятная причина запрета - очень дешевые в производстве вина по сравнению с винами из винограда столовых сортов.
См. также
Железо- Комплексы железа, встречаются, в ферменте метан-моноксигеназе, окисляющем метан в метанол, в важном ферменте рибонуклеотид-редуктазе, который участвует в синтезе ДНК.
Примечания
- ↑ Рябчиков (1953 г.), «Общая химия», стр.253
- ↑ Waganer K. Mariculture on land. — Biomass, 1981
- ↑ 1 2 Острые отравления — Электронное справочное руководство для врача скорой медицинской помощи. Глава 15
- ↑ [1]
Ссылки
- Метанол убивает человека и природу (статья на сайте экологический правозащитного центра «Беллона»)
- ГОСТ 2222-95 «Метанол технический» (взамен ГОСТ 2222-78)
Примечания
Удельная теплота сгорания веществ, Дж/кг Порох 3.8·106 [2] Торф 8.1·106 [1], 15·106 [4] Дрова (березовые, сосновые) 10.2·106 [1] Бурый уголь 15·106 [1], 14,7·106 [4] Бытовой газ 13.25·106 [3] Каменный уголь 22·106 [1], 29,3·106 [4] Спирт этиловый 25·106 [4] Метанол 22.7·106 [4] Условное топливо 29.308·106 (7000 ккал/кг) [1] Древесный уголь 31·106 [4] Метан 50.1·106 [3] Мазут 39.2·106 [1] Дизельное топливо 42.7·106 [4] Нефть 41·106 [4] Бензин 44·106 [1], 42·106 [4] Керосин 40,8·106 [4] Этилен 48.0·106 [3] Пропан 47.54·106 [3] Водород 120.9·106 [3] Спирты (0°) Метанол Первичные спирты (1°) Этанол · Пропанол · Бутиловый спирт/Изобутанол · Пентанол · Гексанол · Гептанол
Жирные спирты: Октанол (C8) · Нонанол (C9) · Деканол (C10) · Ундеканол (C11) · Додеканол (C12) · Тетрадеканол (C14) · Цетиловый спирт (C16)Вторичные спирты (2°) Изопропиловый спирт · 2-Бутанол · 2-Гексанол Третичные спирты (3°) трет-Бутанол · 2-Метил-2-бутанол
Wikimedia Foundation. 2010.