- супрамолекулярная химия
-
- Термин
- супрамолекулярная химия
- Термин на английском
- supramolecular chemistry
- Синонимы
- Аббревиатуры
- Связанные термины
- биомиметика, ван-дер-ваальсово взаимодействие, водородная связь, гидрофобное взаимодействие, донорно-акцепторное взаимодействие, искусственный фотосинтез, клатратная структура, клатрат, молекулярный переключатель, ротаксаны, супрамолекулярная фотохимия, супрамолекулярные гели, супрамолекулярный катализ, темплат, темплатный эффект, хелаты, нанодиапазон
- Определение
- область химии, исследующая супрамолекулярные структуры (ансамбли, состоящие из двух и более молекул, удерживаемых вместе посредством межмолекулярных взаимодействий); "химия молекулярных ансамблей и межмолекулярных связей" (определение Ж.-М. Лена).
- Описание
Традиционная химия основана на ковалентных связях между атомами. В то же время для синтеза сложных наносистем и молекулярных устройств, используемых в нанотехнологиях, возможностей одной ковалентной химии недостаточно, ведь такие системы могут содержать несколько тысяч атомов. На помощь приходят межмолекулярные взаимодействия – именно они помогают объединить отдельные молекулы в сложные ансамбли, называемые супрамолекулярными структурами.
Простейший пример супрамолекулярных структур – это комплексы типа «хозяин-гость». Хозяином (рецептором) обычно выступает большая органическая молекула с полостью в центре, а гостем – более простая молекула или ион. Например, циклические полиэфиры различного размера (краун-эфиры) довольно прочно связывают ионы щелочных металлов (рис. 1).
Для супрамолекулярных структур, характерны следующие свойства: 1) наличие не одного, а нескольких связывающих центров у хозяина. В краун-эфирах эту роль выполняют атомы кислорода, обладающие неподеленными электронными парами. 2) Комплементарность: геометрические структуры и электронные свойства хозяина и гостя взаимно дополняют друг друга. В краун-эфирах это проявляется в том, что диаметр полости должен соответствовать радиусу иона. Комплементарность позволяет хозяину осуществлять селективное связывание гостей строго определенной структуры. В супрамолекулярной химии это явление называют «молекулярное распознавание» (англ. – molecular recognition) (рис. 2). 3) Комплексы с большим числом связей между комплементарными хозяином и гостем обладают высокой структурной организацией.
Супрамолекулярные структуры очень широко распространены в живой природе. Все реакции в живых организмах протекают с участием ферментов – катализаторов белковой природы. Ферменты – идеальные молекулы-хозяева. Активный центр каждого фермента устроен таким образом, что в него может попасть только то вещество (субстрат), которое соответствует ему по размерам и энергии; с другими субстратами фермент реагировать не будет. Другим примером супрамолекулярных биохимических структур служат молекулы ДНК, в которых две полинуклеотидные цепи комплементарно связаны друг с другом посредством множества водородных связей. Каждая цепь является одновременно и гостем, и хозяином для другой цепи.
Основные типы нековалентных взаимодействий, формирующих супрамолекулярные структуры: ионные, ион-дипольные, ван-дер-ваальсовы, гидрофобные взаимодействия и водородные связи. Все нековалентные взаимодействия слабее ковалентных - их энергия редко достигает 100 кДж/моль, однако большое число связей между хозяином и гостем обеспечивает высокую устойчивость супрамолекулярных ансамблей. Нековалентные взаимодействия слабы индивидуально, но сильны коллективно.
Формирование супрамолекулярных ансамблей может происходить самопроизвольно – такое явление называют самосборкой. Это – процесс, в котором небольшие молекулярные компоненты самопроизвольно соединяются вместе, образуя намного более крупные и сложные супрамолекулярные агрегаты. При самосборке энтропия системы уменьшается, ?S < 0, поэтому для того, чтобы процесс был самопроизвольным, то есть имел отрицательную энергию Гиббса:
?G = ?H – T?S < 0
необходимо, чтобы ?H < 0, и |?H| > |T?S|. Это означает, что самосборка происходит с выделением большого количества теплоты. Главной движущей силой самосборки служит стремление химических систем к понижению энергии Гиббса путем образования новых химических связей, энтальпийный эффект здесь преобладает над энтропийным.
Основные классы супрамолекулярных соединений - кавитанды, криптанды, каликсарены, комплексы "гость-хозяин", ротаксаны, катенаны, клатраты. К супрамолекулярным структурам можно также отнести мицеллы, липосомы, жидкие кристаллы.
Методы супрамолекулярной химии находят широкое применение в химическом анализе, медицине, катализе, фотохимии. Супрамолекулярные структуры - основа многих современных технологий, таких как экстракция биологически активных веществ, создание фото- и хемосенсоров, молекулярных электронных устройств, разработка нанокатализаторов, синтез материалов для нелинейной оптики, моделирование сложных биологических процессов (биомиметика).
- Авторы
- Еремин Вадим Владимирович, д.ф.-м.н.
- Ссылки
- Лен Ж.-М. Супрамолекулярная химия. Концепции и перспективы. - Новосибирск: Наука, 1998 - 334 с.
- Стид Дж.В., Этвуд Дж.Л. Супрамолекулярная химия. - В 2-х тт. - М.: Академкнига, 2007
- Иллюстрации
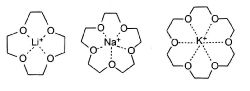
Рис. 1. Комплексы типа «хозяин-гость», образованные краун-эфирами и ионами щелочных металлов
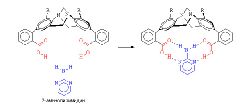
Рис. 2. Молекулярное распознавание с помощью водородных связей
- Теги
- Разделы
- Нанокапсулирование лекарственных препаратов
Элементы солнечной энергетики
Органические светодиоды
Элементы или наборы элементов, контролируемо модифицированные функциональными молекулами, мицеллами или биологическими объектами субмикронных размеров
Нанотехнологии и наноматериалы в медицине (диагностика, системы доставки лекарств, эксипиенты, восстановление тканей и органов, другое)
Бионанотехнологии, биофункциональные наноматериалы и наноразмерные биомолекулярные устройства
Органические и полимерные наноматериалы и волокна
Молекулярная электроника и устройства на ее основе
Наноструктуры
(Источник: «Словарь основных нанотехнологических терминов РОСНАНО») - Термин
Энциклопедический словарь нанотехнологий. — Роснано. 2010.
